Кинетика простейших ферментативных реакций. Уравнение Михаэлиса-Ментен. Влияние ингибиторов на кинетику ферментативных реакций.
Рассмотрим реакцию
E + S k-1↔ k1 (ES) →k2 E + P
где S – субстрат, P – продукт, E – фермент, ES – фермент-субстратный комплекс; k1 k-1 – константы прямой и обратной реакций образования комплекса, k2 – константа скорости образования продукта (при малых концентрациях Р эта реакция необратима). k2 показывает число актов катализа в единицу времени – число оборотов фермента.
Эта система описывается следующими уравнениями:
dS/dt = – k1 (S)(E) + k-1 (ES)
dE/dt = – k1 (S)(E) + k-1 (ES) + k2 (ES)
d(ES)/dt = k1 (S)(E) – k-1 (ES) – k2 (ES)
dP/dt = k2 (ES) = υp
Сложим второе и третье уравнения системы. Получим, что d(E + ES)/dt = 0=> в любой момент времени (E) + (S) = Eo (общая концентрация фермента) и что dE/dt = – d(ES)/dt. Можем выразить Е = Ео – (ES). Заметим, что четвёртое уравнение определяется переменной ES. Значит, можем решать систему из двух уравнений:
dS/dt = – k1 [Ео – (ES)] + k-1 (ES)
d(ES)/dt = k1 (S) [Ео – (ES)] – k-1 (ES) – k2 (ES)
Посмотрим, можно ли разделить переменные на медленные и быстрые. Характерное время изменения субстрата τs = S/υp (υp - скорость ферментативной реакции) Скорость становится максимальной, когда весь фермент (Ео) находится в связанном состоянии: υpmax = k2 Eo. При этом время убыли S будет минимальным: τsmin = S/( k2 Eo). Характерное время оборота фермента определяется в основном реакцией распада ES и константой k2 (k2>> k1). Оно равно τE = 1/k2.
В обычных условиях концентрация субстрата во много раз больше концентрации фермента (обычно Eo = 10-6M, S = 10-2M). Значит, Eo/S = 10-4<<1, Следовательно, τsmin=τE/(10-4) = τE*104
Отсюда τs>> τE => переменная S меняется медленнее, чем ES => скорость изменения субстрата мала по сравнению со скоростью изменения комплекса. Значит, при рассмотрении системы на больших отрезках времени можно считать, что d(ES)/dt = 0. Получаем алгебраическое уравнение:
k1 (S) [Ео – (ES)] – k-1 (ES) – k2 (ES) = 0
Отсюда
ES = (k1*S*Ео)/(k1*S + k-1+ k2) ó
ó υp = k2*ES = (k1*k2*S*Ео)/(k1*S + k-1+ k2)
Поделим числитель и знаменатель правой части на k1:
υp = (k2*S*Ео)/(S + [k-1+ k2]/ k1) = (k2*S*Ео)/(S + Km) – уравнение Михаэлиса-Ментен
Методы определенияυpmax и Km(в биофизике этого толком нет, так что взял из биохимии)
1. При S→∞, υ→ υpmax = k2 Eo (оптимальная концентрация S для данного способа – 10Km). При Km=S, υ= υpmax/2
Рисунок 1
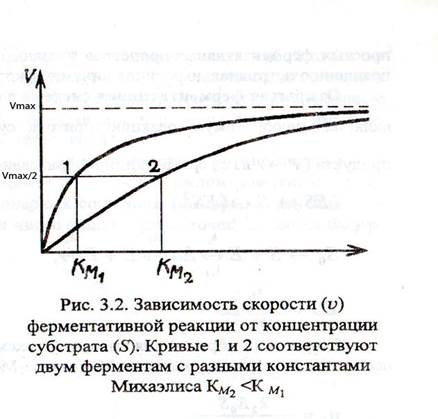
2. Линеаризация уравнения:
1/ υ = (S + Km)/( υpmax*S) = 1/ υpmax +(Km/ υpmax)*(1/S)
Рисунок 2
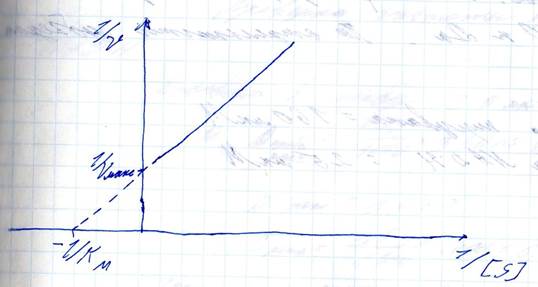
При S→∞, 1/S→0 => 1/υ=1/ υpmax
При 1/ υ=0, 1/ υpmax= – (Km/ υpmax)*(1/S) => S= - Km
Дата добавления: 2016-04-11; просмотров: 1417;
