Методы выявления возбудителя
ОСОБЕННОСТИ МИКРОБИОЦЕНОЗА
ГЕНИТАЛЬНОГО ТРАКТА
ПРИ БЕРЕМЕННОСТИ
Генитальный тракт женщин с точки зрения биологии можно представить как совокупность нескольких биотопов. Биотоп, или экологическая ниша (система), — это среда обитания одного или нескольких видов микроорганизмов, характеризующаяся определенными параметрами: типом и концентрацией питательных веществ, рН, окислительно-восстановительным потенциалом, температурой, гидрацией, уровнем гормонов, кислорода и другими параметрами.
Влагалище, вагинальная микрофлора и влагалищная среда у женщин образуют единый гармоничный биотоп, который обеспечивает защиту от внедрения патогенных возбудителей в половую систему и предотвращает распространение инфекционного процесса во внутренние половые органы.
Влагалище покрыто многослойным неороговевающим плоским эпителием, который подвержен циклическим изменениям в ответ на действие половых гормонов. Важным показателем резистентности вагинального эпителия является количество гликогена, который содержится преимущественно в поверхностных клетках. Поскольку эти клетки постоянно слущиваются и подвергаются цитолизу, гликоген освобождается, обеспечивая питательный субст-
--------------------------------------- Глава 1 -------------------------------------------
рат для нормальной микрофлоры. Установлено, что у женщин репродуктивного возраста на содержание гликогена и его ферментацию оказывает влияние гормональный статус в различные фазы менструального цикла. Большое количество гликогена в вагинальном эпителии — это результат влияния циркулирующих эстрогенов. Максимальное накопление гликогена приходится на момент овуляции. Гликоген метаболизируется лактобациллами до молочной кислоты, что и определяет низкий рН (3,8-4,5) вагинального содержимого и обеспечивает защиту этого биотопа, а также обусловливает микроэкосистему влагалища.
Основное свойство нормальной флоры каждого биотопа — ее способность к самовосстановлению. Так, при изучении микробного пейзажа влагалища до и через 24 часа после обработки влагалища йодоформом отмечается ее полное восстановление.
Микрофлора влагалища функционирует в вагинальном секрете (ВС). Вагинальный секрет состоит из транссудата, который освобождается из капилляров слизистой влагалища, секрета желез слизистой канала шейки матки и бартолиниевых желез, лейкоцитов и клеток слущенного эпителия. Вагинальный секрет содержит воду, неорганические соли, муцин, белки, углеводы, жирные кислоты, мочевину, лизоцим. Среди протеинов преобладают альбумины и иммуноглобулины. Количество секрета влагалища варьирует на протяжении менструального цикла, зависит от влияния эстрогенов и становится максимальным (до 5 мл в сутки) в период овуляции. В секреторную фазу (фазу желтого тела), когда преобладает прогестерон и тормозится образование цервикальной слизи, количество вагинального секрета уменьшается.
Вагинальная микрофлора включает в себя как микроорганизмы, формирующие нормальную резидентную микрофлору, так и случайно занесенные из окружающей среды (транзиторные) непатогенные, условно-патогенные, патогенные бактерии. Эти транзиторные микроорганизмы, как правило, не способны к длительному пребыванию в генитальном тракте и не вызывают развития патологического синдрома до тех пор, пока неиммунные и иммунные защитные механизмы способны обеспечить свою барьерную функцию. Защитные механизмы препятствуют избыточному размножению экзогенных микроорганизмов и внедрению их в слизистую оболочку стенки влагалища с последующим распространением в мочеполовые и в другие органы и ткани.
В настоящее время установлено, что вагинальная микрофлора включает в себя как аэробные, так и анаэробные микроорганизмы. Видовой состав микрофлоры генитального тракта здоровых жен-
--------------------------------------- Глава 1 -------------------------------------------
щин репродуктивного возраста представлен в таблице 1.1. При этом различают два вида анаэробов: факультативные, способные существовать как при отсутствии, так и при доступе кислорода воздуха, и облигатные, которые могут существовать только в бескислородной среде. К резидентной микрофлоре относятся микроорганизмы, постоянно входящие в состав нормальной микрофлоры влагалища и играющие важную роль в метаболизме, они обеспечивают определенный уровень колонизационной резистентности, защищая от возбудителей инфекционных заболеваний.
Представители транзисторной части микрофлоры достаточно часто, но не постоянно, встречаются у здоровых женщин. Среди бактерий, относящихся к обеим составным частям микрофлоры, возможны межвидовые замещения.
Отделяемое влагалища женщин репродуктивного возраста в норме содержит 108-1010 микроорганизмов в 1 мл, при этом соотношение анаэробных и аэробных бактерий составляет от 2:1 до 10:1. Доминируют в микробиоценозе влагалища лактобактерии и бифидобактерии, из них преобладают продуцирующие Н202, и составляют 90-95% всех микроорганизмов.
Ведущее место в вагинальном микробиоценозе женщин занимают различные лактобациллы (табл. 1.2). До недавнего времени наиболее распространенным видом в вагинальном микробиоценозе считались L. acidophilus. Однако исследования последних лет свидетельствуют о том, что вагинальные лактобациллы представлены большим количеством видов. P. Mardh выделил из вагинального отделяемого здоровых женщин 9 видов лактобактерии. По данным А.С. Анкирской (1999) и В.В. Муравьевой было обнаружено 7 видов лактобацилл, при этом преобладал вид L. acidophilus (52,5%). Однако, несмотря на разнообразие видового состава лактобацилл, выделяемых из влагалища здоровой женщины, наиболее часто встречаются L. Jensenii, L. fermentum crispatus, L. gas-seri, L. acidofilus, L. plantarum и др. Таким образом, слизистые генитального тракта у здоровых женщин репродуктивного возраста обсеменены преимущественно Lactobacillus spp., в 95-98% случаев их концентрация составляет 106-109 КОЕ/мл.
С момента первого описания этих бактерий Додерлейном всеми исследователями было признано, что лактобациллы действуют как защитные факторы против размножения патогенных бактерий.
Выделяют несколько механизмов контроля лактобацилл вагинальной экосистемы. Один из них связан с образованием молочной кислоты и ряда других органических кислот, поддерживающих низ-
------------------------------------- Глава 1 -----------------------------------------
Таблица 1.1. Видовой состав микрофлоры генитального тракта здоровых женщин репродуктивного возраста
| Облигатные анаэробные микроорганизмы | Факультативно-анаэробные и аэробные микроорганизмы | ||
| Грамположительные | па ло чки | Lactobacillus spp. Bifidobacterium spp. Eubacterium spp. Clostridium spp. Propionibacterium spp. | Corynebacterium spp. Acinetobacter spp. Mobiluncus spp. Gardnerella vaginalis |
| ко кки | Peptococcus spp. Peptostreptococcus spp. | Staphylococcus: S. epidermidis S. aureus Streptococcus: S. agalactiae (rp. B) Enterococcus | |
| Грамотрицательные | па ло чки | Bacteroides spp. Prevotella spp. Fusobacterium spp. Campylobacter spp. | Enterobacteriaceae: Echerichia Klebsiella spp. Enterobacter Proteus Acinetobacter Pseudomonas |
| ко кки | Veillonella spp. | — | |
| Другие представители микромира | Candida spp. M. hominis M. fermentas M. genitalium U. urealyticum |
---------------------------------- Глава 1 --------------------------------------
Таблица 1.2. Микроорганизмы, составляющие микрофлору
генитального тракта здоровых женщин
репродуктивного возраста
| Микроорганизмы | Частота встречаемости (%) | Концентрация в КО единицах (КОЕ/мл) |
| Lactobacillus spp. | 95-98 | 105,34-108 |
| Bifidobacterium spp. | <10 | 105,45 |
| Eubacterium spp. | + | 103 |
| Clostridium spp. | < 10 | 103 |
| Propionibacterium spp. | 103 | |
| Corynebacterium spp. | 6-7 | 103-104 |
| Bacteroides spp. | до104 | |
| Prevotella spp. | 55-61 | до104 |
| Fusobacterium spp. | <10 | 103 |
| Leptotrix spp. | + | |
| Campylobacter spp. | + | |
| Enterobacteriaceae: | 103,57 | |
| E. coli | < 10 | 103 |
| Klebsiella spp. | + | 103 |
| Enterobacter spp. | + | 103 |
| Proteus spp. | + | 103 |
| Acinetobacter spp. | + | 103 |
| Mobiluncus spp. | + | 103 |
| Pseudomonas | + | 103 |
| Gardnerella vaginalis | < 10 | |
| Staphylococcus spp.: | 103,94-103,57 | |
| Staphylococcus epidermidis | + | + |
| Staphylococcus aureus | < 10 | + |
Глава 1 --------------------------------------
Окончание табл. 1.2
| Micrococcus spp. | + | |
| Enterococcus spp. | 103,67-104 | |
| Streptococcus spp. | < 10 | 105-105,2 |
| Streptococcus гр. В | 5-25 | 104-105 |
| Peptococcus spp. | 40-90 | 103-104 |
| Peptostreptococcus spp. | < 10 | 104 |
| Veillonella spp. | 5-25 | 103 |
| Candida spp. | < 10 | 104 |
| M. hominis | 104 | |
| M. fermentas | <10 | 103 |
| M. genitalium | <10 | 103 |
| U. urealyticum | < 10 | 103 |
| Actinomyces spp. | <10 | 102 |
Примечание.(+) — процент выделения микроорганизма в литературе не указан.
кий РН влагалищной среды, что приводит к повышению редокс-по-тенциала и контролю за размножением анаэробов.
Вторым механизмом регуляции микрофлоры влагалища является образование лактобактериями перекиси водорода, и это тоже подавляет колонизацию биотопа патогенной микрофлорой.
Еще один механизм обусловлен высокой адгезивной способностью лактобактерий к поверхности эпителиальных клеток. Адгези-ном лактобактерий является липотейхоевая кислота или лектин. Прикрепляясь к эпителиоцитам, лактобактерий покрывают стенку влагалища сплошным слоем и препятствуют адгезии других микробов к рецепторам эпителия, обеспечивая тем самым колонизационную резистентность.
Лактобактерий имеют еще один механизм контроля за микрофлорой влагалища путем воздействия на различные звенья иммунной системы, регулируя неспецифический и специфический
_------------------------------------- Глава 1 ---------------------------------------
клеточный и гуморальный иммунитет. Отмечено повышение фагоцитарной активности макрофагов и нейтрофилов, их перекислых систем с увеличением фагоцитоза под воздействием различных видов лактобацилл.
Очень важным моментом является стимуляция секреторных иммуноглобулинов класса А в биотопе влагалища, играющих большую роль в обеспечении колонизационной резистентности слизистых оболочек. Получены данные об усилении лактобациллами антиинфекционной резистентности и повышении противовирусной и антибактериальной защиты путем индукции ими альфа-, бета- и гамма-интерферонов.
Кроме того, лактобактерии вырабатывают протеиноподобные бактериальные субстанции — бактериоцины, которые также участвуют в регуляции колонизационной резистентности влагалищного микробиоценоза, подавляя рост других микроорганизмов.
Бифидобактерии являются еще одной важной составляющей в защите генитального тракта от агрессии внешней среды. Бактерии, принадлежащие к строгим анаэробам, находят у здоровых женщин с частотой 10%, а во время беременности — от 20 до 62% в концентрациях от 103 до 107 КОЕ/мл исследуемого материала. Наиболее часто встречаются B.biiidum, B.breve, B.adolescenties и B.longum, которые ингибируют рост таких микроорганизмов, как эшерихии, клебсиеллы, гарднереллы, стрептококки, за счет выраженной кислотообразующей способности и активной адгезии к эпителиоцитам стенок генитального тракта. Бифидобактерии способны продуцировать бактериоцины, лизоцим, аминокислоты и витамины, которые активно используются в биотопе нижних половых путей здоровой женщины для поддержания нормального микробиоценоза.
Другими представителями нормальной микрофлоры полового тракта здоровой женщины являются пептострептококки (Pepto-coccus spp. и Peptostreptococcus spp), которые ообнаруживают с частотой от 40% до 90% в количестве 103-104 КОЕ/мл. Эти грам-положительные анаэробные кокки выделяются на протяжении всех периодов жизни. Наиболее часто встречаются P. asaccharolyti-cus, которые определяются в вагинальной среде у здоровых женщин в 80% случаев. Несмотря на то, что пептострептококки составляют часть нормальной микрофлоры генитального тракта, их обнаруживают также при различных гнойно-воспалительных процессах в женских половых органах. В ассоциации с другими анаэробными бактериями их выделяют при бактериальном вагино-зе, при этом их концентрация составляет 105 КОЕ/мл и выше.
--------------------------------------- Глава 1 -------------------------------------------
Типичными представителями нормальной микрофлоры полового тракта у женщин из пропионобактерий являются P. acnes, которые выделяются с частотой до 25% и в количествах, не превышающих в норме 104 КОЕ/мл исследуемого материала. Это грампо-ложительные неспорообразующие полиморфные палочки, которые являются анаэробами. За счет вырабатываемых ими органических кислот они участвуют в поддержании колонизационной резистентности и обладают иммуномодулирующими свойствами.
Во влагалище здоровых женщин редко определяются представители рода клостридий (Clostridium spp.) — с частотой не более 10%.
Мобилункус (Mobiluncus spp.) — микроорганизмы, выделяемые у 5% здоровых женщин. Наиболее часто встречаются М. curtisii subsp. и М. mulieris, основное значение они приобретают при бактериальном вагинозе. Эти микроорганизмы обладают способностью к адгезии к стенкам слизистых генитального тракта и производят муколитические ферменты: муциназу и сиалазу. Повышение активности этих ферментов в вагинальном секрете может сопровождаться разрывом плодных оболочек и развитием преждевременных родов.
В состав вагинальной флоры, кроме классической флоры Do-derlein (лактобактерии, бифидобактерии и пептострептококки), входят облигатно-анаэробные грамотрицательные палочки, относящиеся к родам Bacteroides, Prevotella, Fusobacterium и Porphy-romonas.
Анаэробно-облигатные грамотрицательные бактерии выделяют у 85-90% здоровых женщин в количествах 103-104 КОЕ/мл исследуемого материала. Роль этих микроорганизмов до конца не изучена, но известно, что некоторые виды обладают патогенными свойствами. В норме являясь частью вагинальной флоры, они могут быть ответственны за развитие острых воспалительных заболеваний гениталий и обнаруживаются в высоких концентрациях при бактериальном вагинозе.
Наиболее часто встречающимся во влагалище видом из бактероидов являются Bacteroides urealyticum, которые выделяются у здоровых женщин с частотой до 55%. Бактероиды В. fragilis, выявляются у здоровых женщин. В норме их количественные концентрации не превышают 103-104 КОЕ/мл исследуемого материала.
Частота обнаружения представителей рода превотеллы (Prevotella) в вагинальном тракте здоровых женщин достигает 60% случаев, а их количество не превышает 104 КОЕ/мл исследуемого
______________________ Глава 1 -------------------------------------------
материала. Из вагинального тракта здоровых женщин наиболее часто выделяют P.bivia и P. disiens (61%).
Типичным представителем рода Porphyromonas в вагинальном секрете является Porphyromonas asaccharolitica. Количественный уровень этих бактерий не превышает 103 КОЕ/мл исследуемого материала, а частота выделения достигает 31% случаев.
По сравнению с другими, строго анаэробными бактериями, колонизирующими влагалище женщины, фузобактерии (Fusobacterium spp.) в норме встречаются редко — до 8% и в концентрациях, не превышающих 103 КОЕ/мл исследуемого материала. Наиболее часто обнаруживают F. nucleatum.
Вейлонеллы (Veillonella) — это грамотрицательные кокки, которые выделяют в количестве 103 КОЕ/мл исследуемого материала в норме, с частотой 5-25%.
Гарднереллы — факультативно-анаэробные бактерии. G.vaginalis — единственный представитель этого рода, который встречается у 50% сексуально активных женщин, нередко достигая 106 КОЕ/мл исследуемого материала. Эти микроорганизмы обладают выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. Они могут продуцировать муколитические ферменты и гемолизины и играют существенное значение в развитии бактериальных вагинозов.
Коринебактерии — грамположительные аэробные или факуль-тивно анаэробные полиморфные бактерии. Во влагалище здоровых женщин обнаруживаются в 6-7% случаев в количестве 103-104КОЕ/мл влагалищного секрета. Наиболее часто выделяют С. minutissimum, С. egui, С. aguaticum, С. xerosis. Другие коринебактерии в норме обнаруживаются крайне редко.
У сексуально активных женщин из микоплазм чаще выделяют М. hominis, M. genitalium, U. urealyticum, которые считаются условно-патогенными микроорганизмами.
В норме Ureaplasma urealyticum выделяют у 6-7% женщин в количестве 103-104 КОЕ/мл, М. hominis — у 2-15% женщин в количестве 103 КОЕ/мл исследуемого материала. При бактериальном вагинозе основное значение придается М. hominis, частота определения которой достигает 30%, а количественный уровень возрастает до 105КОЕ/мл исследуемого материала и ассоциируется с другими облигатными анаэробами, гарднереллами.
Стафилококки — грамположительные факультативно-анаэробные кокки. К видам, наиболее часто встречающимся во влагалище у здоровых женщин, относятся эпидермальные стафилококки (S. epidermidis). Их количество в исследуемом материале
--------------------------------------- Глава 1 --------------------------------------------
варьирует — 103-104 КОЕ/мл. Золотистые стафилококки коагула-зоположительные (S.aureus) обычно колонизируют влагалище транзиторно и обнаруживаются лишь в 5% случаев. Микроорганизмы последнего вида способны вырабатывать токсин, результатом действия которого может быть синдром токсического шока.
Стрептококки — грамположительные факультативно-анаэробные кокки. В норме во влагалище здоровых женщин выделяют следующие стрептококки: стрептококки viridans («зеленящие» стрептококки или а-гемолитические), стрептококки серологической группы В — S. agalactiae и представители рода Еп-terococcus. Частота обнаружения и количество стрептококков, принадлежащих к этим группам, значительно варьирует и по различным данным составляет для стрептококков viridans от 1 до 55% и 104-10° КОЕ/мл исследуемого материала. Для стрептококков группы В — от 5 до 25% и 104-105 КОЕ/мл исследуемого материала, для энтерококков — от 9 до 10% и 104-105 КОЕ/мл исследуемого материала.
В последние годы в генезе послеродовой и перинатальной инфекции увеличилась роль стрептококков группы В (особенно S. agalactiae), а также повысилась частота носительства этих микроорганизмов в половых путях здоровых женщин (от 5 до 25%). Следует отметить, что у беременных носительство обнаруживается чаще — в 20,4%, а у небеременных — в 9,4% случаев.
Из кишечного тракта новорожденных Streptococcus agalactiae может быть выделен в 10-20% случаев. Считается, что дети инфицируются от матери во время родов при прохождении через родовые пути, причем в случае преждевременного разрыва плодных оболочек или при акушерских манипуляциях, сопровождающих роды, риск контаминации плода повышается. Стрептококки этого вида способны вызывать тяжелые заболевания органов дыхания, менингиты, септицемии, которые нередко приводят к летальному исходу.
Энтеробактерии — грамотрицательные факультативно-анаэробные палочки. Наиболее часто встречающимся видовым представителем является Е. coli — представитель рода Escherichia. Частота их выделения варьирует от 9 до 25%, а количество — от 103 до 104 КОЕ/мл исследуемого материала. Среди других бактерий семейства Enterobacteriaceae, Klebsiella и Enterobacter также могут быть выделены из влагалища здоровых женщин, однако значительно реже — 2-4% случаев. Энтеробактерии могут вызывать воспалительные процессы урогенитального тракта.
--------------------------------------- Глава 1 -------------------------------------------
Дрожжевые грибы рода Candida присутствуют во влагалище здоровых женщин с частотой до 10% и в количестве до 104 КОЕ/мл исследуемого материала. При этой концентрации они не вызывают развития патологического процесса и не способны нарушать жизнеспособность и функцию лейкоцитов. Наиболее часто обнаруживается С. albicans.
Таким образом, нормальная микрофлора женских половых органов включает сапрофитные и условно-патогенные аэробные и анаэробные микроорганизмы, которые находятся в биологическом равновесии друг с другом и являются одним из факторов неспецифической резистентности организма. Условно-патогенные микроорганизмы (УПМ) в определенных условиях (присоединение других инфекционных агентов, изменение физиологического и иммунного статуса и т. д.) могут реализовать свои патогенные свойства и стать возбудителями воспалительных заболеваний женских половых органов, а также послеродовых и послеоперационных осложнений.
Эндоцервикс (слизистая оболочка цервикального канала) покрыт высоким однорядным цилиндрическим эпителием с базаль-но-расположенными ядрами. Продолжительность созревания клеток плоского эпителия эндоцервикса составляет около четырех дней. Слизистая оболочка цервикального канала представляет собой щели и углубления, выстланные цилиндрическим эпителием, которые называют цервикальными железами (в отличие от трубчатых и гроздевидных желез). Циклические изменения в эпителии эндоцервикса выражены слабо. Обильная секреция слизи наблюдается во время фолликулярной фазы, особенно в предовулятор-ный период. После овуляции секреция изменяется, становится скудной.
Биохимические и электронно-микроскопические исследования показали сложное строение слизи. Она представляет собой мицел-лярную сеть гликопротеинов, межмицеллярные пространства которой заполнены цервикальной плазмой. Кристаллизации слизи способствуют ионы калия и хлорида натрия. Основная функция цилиндрического эпителия — секреторная. Количество и физико-химические свойства вырабатываемого слизистого секрета зависят от фазы менструального цикла.
Секрет имеет важное значение для оплодотворения и является барьером для инфекции. Слизистая пробка цервикального канала обладает бактерицидной, протеолитической активностью за счет присутствия в ней лизоцима и компонента лактоферрина. Кроме того, в слизи цервикального канала выявлены иммуноглобулины
--------------------------------------- Глава 1 -------------------------------------------
всех классов, которые играют важную роль в местной защите от инфекций. Содержимое цервикального канала в физиологических условиях обычно стерильное; рН цервикального канала выше, чем во влагалище.
Верхние отделы генитального тракта в норме стерильны, но бактерии могут попадать восходящим путем в полость матки, фаллопиевы трубы, в полость малого таза при менструации, инструментальных вмешательствах, других воздействиях.
Обнаружение отдельных видов микроорганизмов в составе вагинальной и цервикальной микрофлоры не позволяет дать объективную оценку состояния микробиоценоза. Только количественные исследования, определяющие соотношение отдельных видов микроорганизмов, в полной мере характеризуют генитальный микробиоценоз.
Состав микрофлоры зависит от физиологического состояния женщины и изменяется в зависимости от возраста, фазы менструального цикла, при беременности и в послеродовом периоде. Имеют значение климатические условия проживания, сексуальная активность, уровень личной гигиены, применение лекарственных препаратов (контрацептивов, антибиотиков и др.), характер заболевания.
В норме влагалище у новорожденных девочек в первые часы жизни стерильно. Однако уже к концу первых суток после рождения оно колонизируется аэробными, факультативно-анаэробными и анаэробными микроорганизмами. В последующем (через несколько дней) в вагинальной микрофлоре у новорожденных начинают преобладать лактобактерии, их количество возрастает в репродуктивном периоде и уменьшается в менопаузе.
Преобладание лактобактерии в микрофлоре новорожденных связано с влиянием эстрогенов, полученных трансплацентарно от матери. Эстрогены индуцируют накопление в вагинальном эпителии гликогена, являющегося субстратом роста для лактобактерии. Последние расщепляют гликоген до образования молочной кислоты, что приводит к сдвигу рН в кислую сторону (до 4,4-4,6) и ограничению роста и размножения микроорганизмов, чувствительных к кислой среде.
В этот возрастной период видовой состав микрофлоры у новорожденных почти соответствует параметрам влагалища взрослых здоровых женщин. Однако через три недели после рождения материнские эстрогены метаболизируются, эпителий становится тонким, «незрелым», содержание гликогена в нем уменьшается, снижается содержание органических кислот, продуцируемых бак-
--------------------------------------- Глава 1 -------------------------------------------
териями. РН влагалищного содержимого возрастает с 4,5 до 7,0, что способствует снижению количества лактобактерий и окислительно-восстановительного потенциала, а в микрофлоре начинают доминировать другие микроорганизмы. Общее количество микроорганизмов во влагалище у девочек со второго месяца жизни значительно ниже, чем в первый месяц после рождения.
В пубертатный период с началом менструальной функции под влиянием эстрогенов утолщается эпителиальный слой, на поверхности влагалищных эпителиоцитов увеличивается количество рецепторных участков для адгезии лактобактерий, в вагинальном эпителии повышается содержание гликогена, и с этого момента лактобактерий вновь доминируют во влагалище. Метаболизм лактобактерий способствует сдвигу рН в кислую сторону (3,8-4,5),повышение окислительно-восстановительного потенциала создает неблагоприятные условия для роста и размножения представителя патогенной микрофлоры.
У здоровых женщин репродуктивного возраста эстрогены воздействуют на эпителий влагалища в фолликулярную или про-лиферативную фазу менструального цикла, а прогестерон — в лю-теиновую или секреторную фазу. Поэтому микрофлора влагалища изменяется в разные фазы менструального цикла. Наименьшее количество микроорганизмов определяется в период менструации. Частота высеваемости и количество строго анаэробных и большинства аэробных представителей нормальной микрофлоры выше в пролиферативную фазу, чем в секреторную. На 2-14-й дни менструального цикла во влагалище аэробные бактерии преобладают над анаэробными микроорганизмами, а непосредственно перед менструацией количество строго анаэробных микроорганизмов в 100 раз выше, чем количество аэробных микроорганизмов. Уровень лактобацилл при этом остается постоянным.
При наступлении менопаузы в генитальном тракте снижается уровень эстрогенов в крови и количество гликогена в клетках многослойного плоского эпителия, понижается окислительно-восстановительный потенциал, уменьшается количество лактобактерий и бифидобактерий, рН среды приобретает нейтральное значение, обедняется качественный и количественный состав микрофлоры, преобладают другие представители облигатно-анаэробных бактерий.
Изменения вагинального микробиоценоза приводят к элиминации из влагалища основного компонента микрофлоры — лактобацилл, колонизации вагинального биотопа как транзисторными микроорганизмами, так и представителями патогенной микрофло-
--------------------------------------- Глава 1 -------------------------------------------
ры. Возрастает риск возникновения инфекционных заболеваний влагалища.
Знания о микрофлоре половых путей (ее регуляции, изменчивости) чрезвычайно важны для понимания сути процессов, происходящих при инфекционных болезнях. Это в значительной степени способствует выработке адекватных лечебно-профилактических мероприятий и снижению заболеваемости у беременных и новорожденных, уменьшению количества осложнений гестационного процесса.
Выводы
1.Влагалище, вагинальная микрофлора и влагалищная среда у женщин образуют единый гармоничный биотоп, который обеспечивает защиту от внедрения патогенных возбудителей в половую систему и предотвращает развитие инфекционного процесса во внутренних половых органах.
2. Вагинальная микрофлора включает в себя аэробные и фа-культативно-эробные, факультативные и облигатно-анаэробные микроорганизмы.
3. Отделяемое влагалища женщин репродуктивного возраста в норме содержит от 108до 1010 микроорганизмов в 1 мл, при этом соотношение анаэробов к аэробам составляет от 2:1 до 10:1.
3. Перекись продуцирующие лактобациллы занимают ведущее место в вагинальном микробиоценозе здоровых женщин репродуктивного возраста и составляют около 90-95% всех микроорганизмов.
4. Условно-патогенные микроорганизмы, концентрация которых в норме колеблется от 103 до 105 КОЕ/мл, составляют нормальную флору генитального тракта, но в определенных условиях могут реализовать свои патогенные свойства и стать причиной воспалительных заболеваний женских половых органов.
5. Состав микрофлоры зависит от физиологического состояния женщины, изменяется в зависимости от возраста, фазы менструального цикла, при беременности и в послеродовом периоде.
Особенности микробиоценоза генитального тракта при беременности
Во время физиологически протекающей беременности рН влагалища остается низким (3,8-4,4). Этому способствует эстрогенная активность, которая приводит к росту клеток влагалищного эпите-
----------------------------- Глава 1 -------------------------------------------------
лия и увеличению накопления в них гликогена. Последний является субстратом для жизнедеятельности лактобактерий, в процессе метаболизма которых происходит образование молочной кислоты. Молочная кислота, в свою очередь, поддерживает в норме гомео-стаз, при этом рН влагалища соответствует 3,8-4,4 и обеспечивает среду, необходимую для роста лактобактерий. Образуется замкнутый круг поддержки гомеостаза (схема 1.1).
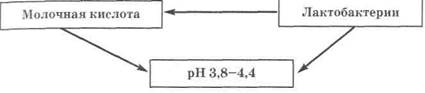
Схема 1.1
Перекись продуцирующие лактобактерии при взаимодействии с пероксидазой из цервикальной слизи и гаплоидными соединениями подавляют размножение патогенных бактерий. Лактобактерии при этом являются фактором неспецифической защиты. Их токсичность по отношению к патогенным микроорганизмам возникает при концентрации Н202-продуцирующих лактобактерии 106 КОЕ/мл.
Невосприимчивость организма беременной к повреждающим факторам и постоянство внутренней среды обеспечиваются микрофлорой, а также нервной, эндокринной и иммунными системами, действующими как единое целое.

|
| Схема 1.2 25 |
Известно, что иммунитет у беременных находится в состоянии супрессии. С другой стороны, увеличение эстрогенного фона поддерживает «систему самоочищения» влагалища, увеличивая его кислотность. Таким образом, возникает динамическое равновесие между состоянием двух систем (схема 1.2).
——-------------------------------- Глава 1 -------------------------------------------
На основе сравнительного анализа видового и количественного состава микрофлоры влагалища можно сказать, что в период геста-ции происходит уменьшение количества факультативно-анаэробных, грампозитивных палочек коринебактерий, стафилококков, стрептококков, энтерококков и грамнегативных палочек — энте-робактерий, анаэробных грампозитивных палочек. Количество КОЕ лактобактерий и бифидобактерий в одном миллилитре увеличивается.
В первом триместре беременности среди факультативных анаэробов в 79% случаев выделяются коринебактерий (103 КОЕ/мл) и стафилококки — в 53% случаев (102 КОЕ/мл). Стрептококки и энтеробактерии определяются редко и в незначительных количествах. Среди облигатных анаэробов в 96% случаев высеваются лактобактерий (108 КОЕ/мл) и в 80% — бифидобактерий (104 КОЕ/мл). В 35% случаев идентифицируются пептострептокок-ки (102 КОЕ/мл), а бактероиды — в 15% случаев. Грибы рода Candida высеваются в количестве 102 КОЕ/мл только в 9% случаев.
По мере увеличения срока беременности снижается численность некоторых групп микроорганизмов. Наблюдается тенденция к снижению как аэробных, так и анаэробных кокков и грамотрицатель-ных палочек, а количество лактобактерий увеличивается в 10 раз по сравнению с таковым у небеременных женщин. Вследствие этих изменений формируется микробная среда с низкой вирулентностью, что обеспечивает незначительную контаминацию плода при его прохождении через родовые пути.
Относительное постоянство состава нормальной микрофлоры обеспечивается комплексом гомеостатических механизмов макроорганизма. Характер взаимодействия микрофлоры и макроорганизма в значительной мере определяется состоянием специфичных и неспецифичных механизмов иммунитета. Гуморальные показатели (система комплимента, лизоцим, опсонины, фибронектин) в комплексе с клеточными (макрофаги, полиморфноядерные лейкоциты, Т-лимфоциты) и элементами местного иммунитета (IgA-ан-титела) формируют защитные барьеры, которые обеспечивают динамическое равновесие между макроорганизмом и нормальной микрофлорой.
Нарушения микрофлоры родовых путей беременных женщин представляют опасность, так как могут являться причиной прерывания беременности, преждевременных родов, внутриутробного инфицирования плода и послеродовых осложнений у матери.
У родильниц в норме существенно изменяется качественный и количественный состав микрофлоры, приблизительно ко вторым
______________________ Глава 1 -------------------------------------------
суткам после родов, увеличивается количество неспорообразую-щих грамотрицательных анаэробных микроорганизмов и снижается концентрация лакто- и бифидобактерий. На третьи сутки идет 100-кратное увеличение числа анаэробов. Микроэкология влагалища в послеродовом периоде характеризуется значительным увеличением численности представителей рода Bacteroides, E. coli, Streptococcus В, D и снижением количества лактобацилл. Данные изменения, возможно, обусловлены снижением уровня эстрогенов, травмой родового канала, другими факторами и могут способствовать развитию послеродового эндометрита. Эти изменения микрофлоры являются транзиторными, и восстановление вагинального микробиоценоза отмечается, как правило, к 6-10-й неделе послеродового периода.
Следует отметить, что микрофлора женщины в родах оказывает значительное влияние на формирование микрофлоры у новорожденных.
Первичная контаминация организма ребенка, в норме стерильного до рождения, осуществляется вагинальной микрофлорой в процессе прохождения через родовые пути матери. Состав микрофлоры кожных покровов, конъюнктивы, желудочного аспирата, кишечника новорожденного идентичен микрофлоре родового канала матери. Формирование микробиоценоза кишечника ребенка существенно влияет на течение периода новорожденности. Риск развития инфекционного процесса у новорожденных находится в прямой зависимости от степени обсемененности околоплодных вод и родовых путей.
Выводы
1.Микробиоценоз генитального тракта у беременных характеризуется увеличением лакто- и бифидобактерий и уменьшением численности других видов микроорганизмов по мере увеличения срока гестации.
2. Непатогенная и условно-патогенная микрофлора половых путей беременных женщин обеспечивает незначительную контаминацию плода при его прохождении через родовые пути.
3. Характер микрофлоры определяется состоянием специфичных и неспецифичных механизмов иммунитета.
4. Нарушения микрофлоры генитального тракта могут являться причиной прерывания беременности, преждевременных родов, внутриутробного инфицирования плода и послеродовых осложнений у матери, а также влияют на формирование микрофлоры у новорожденных.
------------------------------- Глава 1 ------------------------------
ЛИТЕРАТУРА
Краснополъский В.И. Патология влагалища и шейки матки — М.: Медицина, 1997. — С.105-111.
Лактобациллы в акушерстве и педиатрии / Под ред. В.Е. Радзин-ского. — Ашгабат, 1994. — 102 с.
Микроэкология влагалища. Коррекция микрофлоры при вагинальных дисбактериозах: Учеб. пособие / Под ред. В.М. Коршунова, Н.Н. Володина и др. — М., 2001.
Современные вопросы инфектологии в акушерстве и гинекологии / Под ред. проф. В.К. Чайки: Учеб. пособие. — Донецк, 1998. — 177 с.
Carson H.M., LaPoint P.G., Monif G.R.G. Interrelationships within the bacterial flora of the female genital tract // Infect Dis. Obstet. Gynecol. — 1997 — N5.— 305 p.
Chaisilwattana P., Monif G.R.G. In vitro ability of the group В streptococci to inhibit gram-positive and gram-variable constituents of the bacterial flora of the female genital tract // Infect. Dis. Obstet. Gynecol. — 1995. — N3. — 91 p.
Draper D.L., Landers D.V., Krohn MA., et al. Levels of vaginal secretory leukocyte protease inhibitor are decreased in women with lower reproductive tract infections. —Am. J. Obstet. Gynecol. — 2000. — N 183. — P. 1243-1248.
Larsen В., Monif G.R.G. Understanding the bacterial flora of the female genital tract. — Clin. Infect. Dis. — 2001. — N 32. — 69 p.
Infectious Diseases in Obstetrics and Gynecology / Gilles R.G. Monif David A. Baker. — 2004. — 760 p.
Obstetric and Gynecologic Infectious Disease / Joseph G.Pastorek. — New York: Raven Press, 1993. — 798 p.
ГЛАВА 2
ОБЩАЯ ХАРАКТЕРИСТИКА ИНФЕКЦИЙ ПРИ БЕРЕМЕННОСТИ
Т. В. Севастьянова, Ю.А. Батман
С общебиологических позиций под инфекцией понимают любое проникновение и размножение во внутренней среде человека различных микроорганизмов (вирусов, бактерий, простейших и др.). Само инфицирование («попадание») микроорганизмов в макроорганизм не обязательно сопровождается развитием патологических изменений. Следует отметить, что проникновение микроорганизма приводит к комплексу иммунологических, биохимических и иных реакций в макроорганизме, из которых складывается инфекционный процесс.
В зависимости от вирулентности возбудителя, массивности инфицирования и состояния макроорганизма результатом инфекционного процесса может явиться:
— элиминация возбудителя (ликвидация инфекции);
— носительство (латентная инфекция);
— инфекционная болезнь.
Инфекционный процесс в начальной стадии и латентная инфекция обычно не сопровождаются клинически значимыми изменениями состояния здоровья и, как правило, могут быть выявлены при помощи специальных лабораторных методов.
Инфекционная болезнь всегда имеет клинические проявления; их выраженность и специфичность определяются свойствами возбудителя, реактивностью макроорганизма и временем, прошедшим с момента заражения.
В клинической медицине термины «инфекция» и «инфекционная болезнь», по сути, являются синонимами.
В развитии инфекционного процесса большую роль играет иммунитет. Роль иммунитета заключается в защите «своего» и устра-
—------------------------------------ Глава 2 -------------------------------------------
нении «чужого» методом деструкции. Под термином иммунитета подразумевается следующее: опознание «чужого» и немедленное его устранение (врожденный иммунитет) или процесс подготовки чужеродного материала для дальнейшей его элиминации (приобретенный иммунитет). Этот процесс эффективно осуществляется иммунной системой, мобильной и гетерогенной популяцией клеток, включая фагоциты и лейкоциты, которые осуществляют как процесс опознания, так и уничтожения чужеродных элементов. Система включает также память, которая обеспечивает быстрый ответ на повторное появление антигена.
У взрослого человека и ребенка старшего возраста благодаря высокой эффективности иммунного ответа значительно чаще наблюдается абортивное или латентное течение инфекции. У детей младшего возраста чаще развивается инфекционная болезнь.
Беременность является уязвимым периодом, способствующим приобретению инфекций и инфекционных заболеваний. Снижение физиологических адаптационных механизмов в период беременности приводит к повышению риска инфицирования. При этом может быть инфицирована не только беременная женщина, но также возможна трансмиссия инфекционных агентов плоду или новорожденному. Риск инфицирования плода зависит от воздействующего микроорганизма, пути передачи, потенциала прохождения плацентарного барьера, времени воздействия и иммунного статуса матери/плода.
Важным звеном в понимании влияния инфекций во время беременности или в неонатальный период, а также обеспечения профилактических мероприятий по предотвращению трансмиссии от матери к ребенку являются пути передачи инфекции плоду или новорожденному. Инфекции плоду/новорожденному могут передаваться in utero (врожденные инфекции), во время родов или в неонатальный период (послеродовая инфекция) (табл. 2.1).
Следует отметить, что большинство инфекций не проходят через плаценту или это происходит крайне редко.Многие микроорганизмы могут инфицировать плод/новорожденного во время родов и после родов (табл. 2.2). Опосредованное влияние на плод могут оказывать инфекции репродуктивного тракта, такие как условно-патогенные микроорганизмы (эндогенные инфекции), атакже инфекции, передающиеся половым путем (ИППП), которые могут быть причиной хориоамнионита, преждевременных родов, инфекционных заболеваний у новорожденного.
Группа инфекций, которые могут проникать через плаценту и непосредственно воздействовать на плод, представлена в таблице 2.3.
—-------------------- Глава 2 ----------------------------
Таблица 2.1. Пути распространения инфекций
| До родов | Трансплацентарный. Восходящая инфекция |
| Во время родов | Контакт с инфицированными выделениями гениталий/кровью/калом во время родов |
| После родов | Кормление молоком. Переливание крови. Нозокомиальная инфекция |
Воздействие материнской инфекции на плод проявляется в прямом воздействии токсинов или микроорганизмов или в опосредованном контакте в результате нарушения функции плаценты или матки.
Следует также отметить, что при инфекционном заболевании у женщины во время беременности на эмбрион и плод действуют не только возбудители, но и токсические продукты, образующиеся при их распаде. А гипертермия и гипоксия у матери, которая может иметь место при остром процессе (и как следствие этого — образование токсических веществ), также негативно влияют на развивающийся плод и течение беременности.
Но не всегда наличие инфекционного процесса у матери сопровождается инфекционным поражением плода. Важным условием для инфицирования плода является наличие бактеремии или ви-ремии у матери,а также длительность этой фазы, которая наиболее продолжительная при первичном инфицировании у матери, менее продолжительная — при рецидиве, и отсутствует при носи-тельстве.
Первичная инфекция в период беременности представляет более серьезную угрозу для плода или новорожденного, нежели рецидивирующая или вторичная инфекция.
Появление материнской виремии с последующим инфицированием плода характерно для первичной инфекции краснухи. ЦМВ, как и простому герпес-вирусу, характерна реактивация вируса в течение всей жизни с момента первичной инфекции, но рецидивирующие инфекции редко связаны с нежелательными последствиями для плода.
-------- —------------------------- Глава 2 ------------------------------------------
Таблица 2.2. Перинатальная трансмиссия патогенов человека3
| Материнская инфекция | Распространенность в США, % | Период трансмиссии | Инфицирование/колонизирование новорожденных, % | |
| при беременности | во время родов | |||
| Бактериальный вагиноз | 20,0 | - | - | |
| Хламидии | 5,0 | - | + | 50,0 |
| Вирус Коксаки | Неясна | + | - | +/- |
| цмв | 33,0 | + | + | 3,0 |
| Экховирус | Неясна | - | + | +/_ |
| Гонорея | 1,0 | - | + | 50,0 |
| СГВ | 20,0 | - | + | 50,0 |
| Гепатит А | 0,1 | - | - | - |
| Гепатит В | 1,0 | - | + | 30,0 |
| Гепатит С | 2,0 | - | + | 20,0 |
| Вирус простого герпеса | 20,0 | +/" | + | 50,0 |
| ВИЧ | 0,2 | + | + | 25,0 |
| ВПЧ | 5,0 | - | + | 5,0 |
| Грипп | 10,0 | + | - | +/- |
| Листериоз | 5,0 | + | - | +/- |
| Боррелиоз Лайма | 0,08 | + | - | +/- |
| Малярия | +/- | + | - | 4,0 |
| Корь | 0,04 | + | - | +/- |
| Паротит | 0,1 | + | - | +/- |
| Парвовирус | 1,0 | + | - | 20,0 |
| Краснуха | +/- | + | - | 50,0 |
| Сифилис | 0,2 | 4- | +/- | 40,0 |
— Глава 2 ------------------------------------------
Окончание табл. 2.2
| Токсоплазмоз | 1,0 | + | - | 30,0 |
| Трихомониаз | 2,0 | - | - | |
| Туберкулез | 0,1 | + | - | + 1— ' / |
| Ветряная оспа | 0,05 | + | + | 2,0 |
Примечание.«+/-» — возможно, но редко; «-» — не случается или очень редко; а — адаптировано (по Goldenberg et al., 1997, 1999).
Таблица 2.3. Инфекции периода беременности, способные повредить плод или новорожденного
| Вирусы | Простейшие |
| Краснуха | |
| Цитомегаловирус | |
| Вирус простого герпеса | |
| Вирус ветряной оспы | |
| Парвовирус В19 | Токсоплазмоз |
| Гепатиты В и С | Сифилис |
| Папилломавирус | Листериоз |
| Лимфоцитарный вирус хорименингита | |
| ВИЧ-1,2 | |
| HTLV-1,2 |
Рецидивирующая инфекция, вызванная вирусом herpes simplex, является довольно частой и представляет значительный риск для новорожденного.
До недавнего времени в англоязычной литературе упоминался термин «TORCH-синдром», который объединяет следующие внутриутробные инфекции:
Т — Toxoplasma (токсоплазмоз);
О — Others (другие):
• сифилис;
• энтеровирусные инфекции;
• листериоз;
--------------------------------------- Глава 2
• парвовирус В19;
• человеческий папилломавирус;
• ветряная оспа;
R — Rubella (краснуха);
С — Cytomegalovirus (цитомегаловирус);
Н — Herpes simplex virus (вирус простого герпеса).
В последнее время эта группа инфекций упоминается как «врожденные инфекции».
Возбудители данных инфекций вызывают у плода и новорожденных детей при внутриутробном заражении схожие клинические проявления, а впоследствии и стойкие структурные дефекты многих органов и систем, и особенно центральной нервной системы.
Наиболее распространенными клиническими признаками внутриутробной инфекции являются:
— задержка внутриутробного развития плода;
— гепатоспленомегалия;
— желтуха;
— сыпь;
— микроцефалия;
— гидроцефалия;
— тромбоцитопения;
— тяжелые неврологические нарушения.
Риск вертикальной трансмиссии и/или последствия для плода или новорожденного предопределяет гестационный срок беременности, в котором проявляется инфекция. Например, воздействие на плод краснухи в первый триместр беременности связано с высоким риском возникновения серьезных врожденных дефектов, таких как катаракта, аномалии сердца, сенсороневральная глухота, в то время как воздействие инфекции в более поздние сроки беременности или в послеродовом периоде создает меньшую угрозу. С другой стороны, воздействие на плод первичной цитомегаловирус-ной инфекции связано с риском возникновения нежелательных последствий в любом сроке беременности. В то же время проявление инфекции в период родов (при взаимодействии с инфицированными выделениями шейки матки) или в послеродовый период (через зараженное молоко матери) не связано с нежелательными последствиями, за исключением глубоко недоношенных или иммуноде-фицитных новорожденных.
Процент инфицирования плода в результате воздействия токсо-плазмоза матери зависит от времени проявления материнской инфекции: процент является низким (10%) при инфицировании в первые две недели после зачатия и увеличивается (более 90%),
______________________ Глава 2 ------------------------------------------
если инфицирование происходит в последние две недели беременности, а риск серьезных нежелательных последствий в результате токсоплазмоза намного выше при воздействии инфекции в ранние сроки беременности, нежели в поздние.
Появление генитальной герпесной инфекции в период родов создает риск неонатальной герпесной инфекции, заболеваемости и летальности новорожденных. С другой стороны, герпесная инфекция в ранние сроки беременности создает малую угрозу для плода. Проявление ветряной оспы в период родов или незадолго до них может быть причиной явной инфекции новорожденного, в то время как инфекция в первом и втором триместрах беременности связана с низким риском врожденного синдрома ветряной оспы (около 1%). Заболевание ветряной оспой во втором и третьем триместрах приводит к проявлению опоясывающего герпеса в детстве.
Некоторые перинатально приобретенные инфекции, такие как ВИЧ,не проявляются в форме острых инфекций в новорожденный период, а развиваются постепенно.
При развитии инфекции на ранних сроках гестации нередко формируются грубые пороки развития плода (эмбриопатия), несовместимые с жизнью; беременность часто заканчивается самопроизвольным выкидышем. При инфицировании после 8-12-й недели гестации эмбрио-/фетопатия может быть совместима с внутриутробной жизнью, однако до момента рождения в организме плода происходит ряд изменений, которые могут стать причиной мертво-рождения, тяжелого заболевания новорожденного или смерти в неонатальном периоде. При возникновении инфекции у плода во втором и третьем триместрах беременности могут выявляться как признаки инфекционного поражения отдельных органов плода (гепатит, миокардит, менингит/менингоэнцефалит, хориоретинит), так и симптомы генерализованной инфекции.
Исходы влияния инфекций на плод могут быть следующими:
— аборт или мертворождение;
— врожденные пороки развития;
— острое заболевание или летальность в неонатальный период;
— повреждения:
• очевидные при рождении;
• поздние проявления;
— бессимптомная инфекция.
Прерывание беременности. Большинство самопроизвольных прерываний беременностей в первом триместре является результатом хромосомных аномалий. Спонтанный выкидыш нормально развивающегося плода в первом триместре беременности происхо-
--------------------------------------- Глава 2-------------------------------------------------
дит редко. Причиной ранних спонтанных выкидышей могут быть такие инфекции у беременной, как токсоплазмоз, сифилис, паротит, листериоз и парвовирус.
В отличие от выкидышей первого триместра, прерывание беременности во втором триместре часто связано с потерей нормально развивающегося плода и в большинстве случаев происходит в результате спонтанных преждевременных родов, разрыва околоплодных оболочек или гипоксии плода с последующими преждевременными родами. При исследовании плодов после спонтанных абортов второго триместра часто обнаруживаются гистологический хориоамнионит или колонизация микроорганизмами по сравнению с материалами, взятыми у женщин при индуцированных абортах, что указывает на связь преждевременных родов со скрытой инфекцией верхнего генитального тракта.
Мертворождение. В США мертворождение осложняет около 1% родов. Около 80% мертворожденных наблюдается до 37-й недели беременности, а половина из них — до 28-й недели. Этиология мертворождаемости, однако, не всегда ясна. Многие плоды раннего гестационного периода погибают в результате спонтанных преждевременных родов или разрыва околоплодных оболочек. Гистологические изменения плаценты с хориоамнионитом часто обнаруживаются в ассоциации с ранним мертворождением. Кроме того, у пациенток с мертворожденным плодом наблюдается повышенный риск возникновения послеродового эндометрита. Полученные данные позволяют предположить, что внутриматочная инфекция является главным фактором большинства мертворожде-ний, связанных как с преждевременными родами или разрывами оболочек, так и вызывающими гибель плода, что неизбежно ведет к рождению мертвого ребенка. Сифилис, парвовирус, краснуха, токсоплазмоз, малярия, боррелиоз Lyme, листериоз и стрептококки группы В являются главными факторами мертворождаемости.
Врожденные аномалии. Частота врожденных аномалий в общей популяции составляет 1-3%. Многие инфекции связаны с врожденными аномалиями, однако для подтверждения причин существуют лишь немногие доказательства. Следует отметить, что только сифилис, ветряная оспа и краснуха связаны с повышенной частотой врожденных аномалий. Эмбриопатия в результате ветряной оспы, характеризующаяся рубцами кожи, атрофией мышц, гипоплазией конечностей, осложняет около 3% беременностей матерей с острой инфекцией (< = 20 неделям гестации). Врожденная краснуха, ны- не встречающаяся менее часто в районах с рутинной программой иммунизации, была наиболее частой причиной врожденных де-
______________________ Глава 2 -------------------------------------------
фектов сердца и глухоты. Врожденный сифилис, характеризующийся скелетными аномалиями, пневмонией, анемией, водянкой и т. д., может развиваться у 10-50% новорожденных инфицированных женщин в зависимости от стадии материнской инфекции.
Задержка внутриутробного развития плода. Классически такие инфекции, как краснуха, токсоплазмоз, цитомегаловирус, ветряная оспа, листериоз и сифилис, при инфицировании плода в ранние сроки беременности являются результатом врожденной инфекции и последующего нарушения развития. Во многих случаях задержка развития связана с повышенным риском возникновения неонатальной летальности и неврологических нарушений.
Летальность в период новорожденности. В большинстве западных стран неонатальная смертность наблюдается от 4 до 8 на 1000 новорожденных. 70% смертности связаны с преждевременными родами, 25% — с врожденными аномалиями, остальные — с асфиксией, сепсисом, аспирацией мекония, родовой травмой и редкими заболеваниями (иммунная или неиммунная водянка). Смертность новорожденного наблюдается при преждевременных родах. Часто инфекция является причиной заболеваний, связанных с недоношенностью, включая респираторный дистресс-синдром, внут-рижелудочковые кровотечения и некротизирующий энтероколит.
Стрептококки группы В и E.coli являются основной причиной сепсиса новорожденных. Однако большинство микроорганизмов, включая представителей нормальной микрофлоры влагалища, а также приобретенных госпитально, связаны с сепсис-зависимой смертностью новорожденных. Кроме того, такие инфекции как ЦМВ, простой герпес, краснуха, ветряная оспа, экховирус, корь, листериоз, туберкулез могут быть причиной неонатальной или постнатальной смертности даже среди доношенных\новорожденных.
Персистенция инфекции у детей. Такие инфекции как краснуха, цитомегаловирусная инфекция, токсоплазмоз, вирус простого герпеса вызывают острую инфекцию новорожденных, ассоциирующуюся с летальностью и последующей заболеваемостью. При некоторых инфекциях развиваются особенные проблемы из-за пер-систирования микроорганизмов в организме хозяина, где они продолжают реплицироваться, тем самым вызывая разрушение тканей после рождения. Другие инфекции, такие как корь, паротит и энтеровирусные инфекции, могут быть причиной внутрима-точной инфекции, но не персистируют. Хронические инфекции наблюдаются в случаях краснухи, цитомегаловируса, токсоплаз-моза, сифилиса, ВИЧ и HTLV-1. Проявление ветряной оспы во время беременности может быть результатом субклинической ин-
--------------------------------------- Глава 2 --------------------------------------------
фекции с реактивацией вируса в первые месяцы или годы жизни, манифестируя как опоясывающий герпес. Существует предположение, что синдром ветряной оспы, проявляющийся вследствие воздействия инфекции в ранние сроки беременности, является скорее результатом реактивации вируса в поздние сроки беременности, нежели следствием первичной инфекции.
Доказана трансплацентарная трансмиссия парвовируса человека (В19), но остается под вопросом возможность персистенции инфекции человека так, как это происходит у животных. Однако известно, что В19 персистирует у людей с иммунодефицитом, которые приобрели инфекцию после рождения, и существуют некоторые доказательства ограниченной пренатальной персистенции в организме плода или плаценте при гестационной инфекции. Многие клинические признаки, характерные для внутриутробного инфицирования, могут быть вызваны не только одной какой-либо врожденной инфекцией (табл. 2.4).
Поздние проявления. Они могут быть вызваны прямым необратимым повреждением при проявлении первичной инфекции или заболевания в результате персистирования инфекции или ее реактивации в детском или взрослом возрасте. Повреждения также могут быть результатом вторжения в процесс развития плода, вызывая нарушения структур, как в случае врожденной краснухи. Может наблюдаться снижение нормального числа или изменение формы клеток плода, что приводит к нарушению структуры или функции определенных органов или целых систем, либо изменения могут быть очень субтильными (например, изменения в мозге оказывают влияние на умственное развитие).
К поздним проявлениям относятся: (i) структурные врожденные аномалии с дефектами одного или более органов; (ii) структурные и функциональные нарушения мозга со сниженной когнитивной способностью, умственной отсталостью, (ііі) нарушение моторики со снижением навыков или повышенной спастичностью или атетозом, как в случаях церебрального паралича. Эти нарушения в дополнение к слепоте, глухоте и гидроцефалии связаны с инфекционными заболеваниями (табл. 2.5).
Установлена явная связь между внутриматочной инфекцией и дальнейшим развитием перивентрикулярной лейкомаляции, вну-трижелудочковых кровоизлияний и церебрального паралича.
Большинство случаев церебрального паралича не имеют специфической этиологии. Внутриматочная инфекция и множество воспалительных цитокинов повышают риск гибели клеток, приводя к «лейкомаляции» и перивентрикулярному кровоизлиянию и, в
--------------------------------------- Глав
Дата добавления: 2016-03-22; просмотров: 970;
