Принцип Ле Шательє - Брауна
Дія тиску, концентрації, температури та інших факторів на систему, що знаходиться в стані хімічної рівноваги, узагальнює принцип зсуву рівноваги, так званий принцип Ле Шательє - Брауна: Якщо на систему, що знаходиться в стані істинної рівноваги, чиниться зовнішній вплив, то в системі виникає самочинний процес, який компенсує даний вплив. Принцип Ле Шательє - Брауна є одним з наслідків другого начала термодинаміки і застосовний до будь-яких макроскопічних систем, що знаходяться в стані істинної рівноваги.
Ізотерма хімічної реакції (ізотерма Вант-Гоффа)
При самочинному протіканні хімічної реакції зміна вільної енергії системи відмінна від нуля (ΔG <0, ΔF <0) і дорівнює
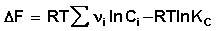 (3.7)
(3.7)
або
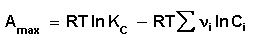 (3.8)
(3.8)
для ізохорно-ізотермічного процесу
та
 (3.9)
(3.9)
або
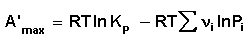 (3.10)
(3.10)
для ізобарно-ізотермічного процесу.
Ці рівняння називаються ізотермою хімічної реакції (ізотермою Вант-Гоффа). Рівняння ізотерми Вант-Гоффа дозволяє розрахувати максимальну роботу хімічної реакції і тим самим визначити можливість її самовільного протікання в будь-яких конкретних умовах (при температурі Т і концентраціях реагентів Ci або парціальних тисках Pi).
Дата добавления: 2016-02-27; просмотров: 942;
