Теоретические основы. Термодинамическим процессом называется любое изменение состояния вещества, например, газа
Термодинамическим процессом называется любое изменение состояния вещества, например, газа. Вид процесса обычно определяется тем, что задано условие постоянства какой-либо функции состояния (например, и = idem, i = idem, s = idem и т. п.) или какого-либо параметра (например, P =idem, t=idem, υ=idem). В ряде случаев процесс может быть задан условием о равенстве нулю какого-либо эффекта в процессе (например, равенство нулю теплообмена, δq=0 ).
Большинство процессов описывается общим уравнением политропы с постоянным показателем
Соотношения между парамет
зависимости термодинами
| Наименова-ние процесса | Уравнение процесса | Показатель политропы | Связь между параметрами | Термодинами-ческая работа |
| Политропный | PVn=idem | 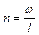
| 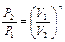
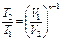
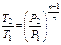
| 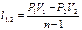 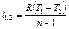
|
| Изобарный | P=idem | n = 0 | 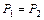
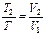
| 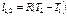
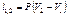
|
| Изохорный | V=idem | n = ±¥ | 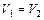
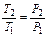
| 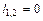
|
| Изотерми-ческий | PV=idem | n = 1 | 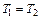
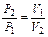
| 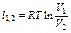
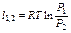
|
| Адиабатный | PVк=idem | n = к= 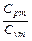
| 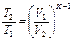
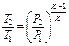
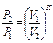
| 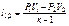 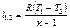
|
Таблица 3.1.3.
рами состояния, расчетные и проверочные
ческих величин в процессах
| Потенциальная работа | Теплоем-кость процесса | Количество тепла | Изменение энтропии |
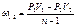
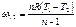
| 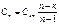
| 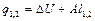
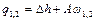
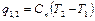
| 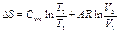 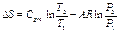 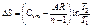
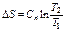
|
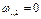
| Срm | 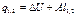 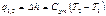
| 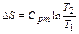
|
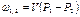
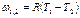
| Cvm | 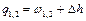 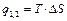 q1,2=Сvm(T2-T1)
q1,2=Сvm(T2-T1)
| 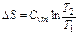
|
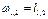
| ¥ | 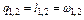
| 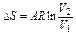
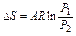
|
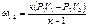 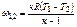
| 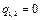
| 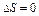
|
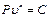 (3.1.29).
(3.1.29).
или
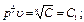 (3.1.30).
(3.1.30).
где n - показатель политропы, являющийся постоянной величиной для данного процесса, который может в зависимости от вида процесса иметь численные значения от - ∞ до 0 и от 0 до + ∞. С и С1 - постоянные, характеризующие прохождение процесса через какую-либо точку процесса, например, точку 1, 2 . . .n.
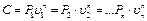 (3.1.31).
(3.1.31).
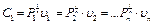 (3.1.32).
(3.1.32).
Из уравнения (3.1.29) и (3.1.30) следуют различные простейшие процессы: Р=idem (изобарический) при n = 0 из уравнения (3.1.29); υ=idem (изохорический) при n=±∞ из уравнения (3.1.30); Рυ=idem (изопотенциальный, а для идеальных газов Рυ=RT, изотермический, t=idem) при n=1 из уравнений (3.1.29) либо (3.1.30) и т.п.
Следовательно, политропический процесс это любой процесс и он становится определенным только после того, как задано значение показателя п.
Решение задач на процессы обычно сводится к нахождению численных значений Р, υ, t в характерных точках, процесса (1,2), определению эффекта процесса (величины работы, подведенного или отведенного тепла и т. п.).
Основные соотношения между параметрами состояния, расчетные и проверочные зависимости термодинамических величин в процессах указаны в табл. 3.1.3.
Дата добавления: 2016-02-27; просмотров: 870;
