Примеры решения задач. Пример 3.1.11. 1 кг метана при постоянной температуре t1=+15°С и начальном давлении P1=3,5 МПа сжимается до давления P2=5,5 МПа
Пример 3.1.11. 1 кг метана при постоянной температуре t1=+15°С и начальном давлении P1=3,5 МПа сжимается до давления P2=5,5 МПа. Определить удельный конечный объем и количество тепла, отводимого в процессе сжатия, затрачиваемую работу.
Решение
1. Процесс изотермический, то есть по условию задачи температура газа в процессе сжатия остается неизменной t = + 15°С = idem.
2. Удельный начальный объем газа определяют из уравнения состояния
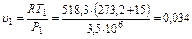 м3/кг,
м3/кг,
где R — газовая постоянная метана
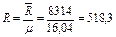 Дж/(кг∙К).
Дж/(кг∙К).
Так как в изотермическом процессе, когда n = 1
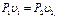 (3.1.33)
(3.1.33)
то конечный объем газа равен
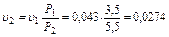 м3/кг.
м3/кг.
3. Работа, затрачиваемая на сжатие 1 кг метана, определяется из уравнения
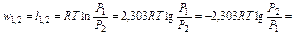
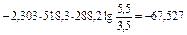 кДж/кг.
кДж/кг.
4. Количество тепла, отводимого от газа, численно равно работе, затраченной на сжатие. Следовательно
q = - 67,527 кДж/кг.
Пример 3.1.12. Метан массой 1 кг адиабатически расширяется с давления Р1=5,5 МПа и температуры 50°С до давления Р2=1 МПа. Найти конечные объем, температуру, потенциальную и термодинамическую работу, изменение внутренней энергии и энтальпии. Показатель процесса расширения принять равным k = 1,4.
Решение
1.Начальный удельный объем находится из уравнения Клапейрона. Газовая постоянная для метана 518,3 Дж/кг∙К.
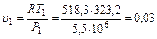 м3/кг.
м3/кг.
2. Для адиабатического процесса справедливы уравнения вида
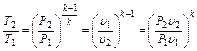 .
.
Отсюда
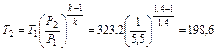 К;
К;
t2=T2-273,2≈75 oC.
3. Конечный объем в процессе расширения равен
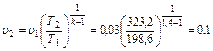 м3/кг.
м3/кг.
4. Определение удельных значений работ осуществляется с помощью следующих уравнений
Термодинамическая работа
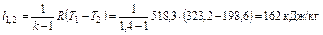
Потенциальная работа
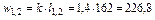 кДж/кг.
кДж/кг.
5. Изменение внутренней энергии и энтальпии в обратимом адиабатическом процессе соответственно равно термодинамической и потенциальной работам.
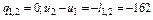 кДж/кг;
кДж/кг;
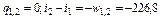 кДж/кг.
кДж/кг.
Дата добавления: 2016-02-27; просмотров: 3358;
