Предмет химии. Основные химические понятия.
Современная химия - одна из естественных наук и представляющая собой систему отдельных научных дисциплин: общей и неорганической, аналитической, органической, физической и коллоидной, геохимии, космохимии и т.д.
Химия изучает материальный мир во всем многообразии форм его существования и превращений.
Материя – это объективная реальность, существующая независимо от нашего сознания и данная нам в ощущениях.
Известны две формы существования материи – вещество и поле.
Вещество - материальное образование, состоящее из элементарных частиц, имеющих собственную массу или массу покоя. К элементарным частицам с конечной массой покоя относятся электроны и позитроны (лептоны), протоны и нейтроны (нуклоны), промежуточные по массе между лептонами и нуклонами – мезоны, гипероны и другие тяжелые частицы - барионы.
Все вещества состоят из атомов, следовательно, из электронов, протонов и нейтронов. Химия изучает первую форму существования материи - вещество. Химия- это наука, изучающая свойства и превращения веществ, сопровождающиеся изменением состава и строения (наука о веществах и их превращениях).
Вторая форма существования материи – физическое поле – материальная среда, в которой осуществляется взаимодействие частиц, не является непосредственным объектом химии. Специфика химической формы движения материи – изменение состава вещества.
«Химию называют наукой о качественных изменениях тел, происходящих под влиянием изменения количественного состава» (Энгельс).
Химия тесно связана с другими естественными науками – физикой, биологией, математикой, геологией.
На границе между геологией и химией возникла геохимия, изучающая распространенность и миграцию химических элементов на Земле. На стыке химии, биологии и геологии возникла биогеохимия, изучающая геохимические процессы с участием живых организмов.
Основатель научной химии М.В.Ломоносов говорил: «Химик без знания физики подобен человеку, который всего должен искать ощупом. И сии две науки так соединены между собою, что одна без другой в совершенстве быть не могут».
Доказательство этому – процветание в наше время физической химии и химической физики. Тесно соприкасается химия с биологией. На уровне молекулярной биологии целиком и полностью оправдываются слова Энгельса о том, что биология – химия белка. Яркое доказательство взаимосвязи – зарождение и бурное развитие биохимии, бионеорганической химии, биоорганической химии и др.
Основные понятия химии даны в атомно-молекулярной теории, создателем которой является М.В. Ломоносов (1742г) и он по праву считается основателем научной химии.
Основные положения атомно-молекулярной теории:
1.Все вещества состоят из молекул, атомов или ионов. Молекула – это наименьшая частица вещества, обладающая его химическими свойствами.
2. Молекулы находятся в постоянном хаотическом движении, называемом тепловым и с повышением температуры скорость движения молекул увеличивается.
3. Молекулы различных веществ отличаются друг от друга массой, размерами, составом, строением и химическими свойствами.
4.Молекулы простых веществ состоят из одинаковых атомов
( Fe, Si, H2 , F2 , N2), молекулы сложных веществ – из различных атомов(CO2, C6H6, NaCI) . Простые вещества – гомосоединения, сложные – гетеросоединения в агрегатном состоянии устойчивом при стандартных условиях .
5.Атомом называется наименьшая частица химического элемента.
Химический элемент – совокупность атомов с одинаковым зарядом ядра и электронной оболочкой.
В настоящее время известно около 120 элементов, из них в природе существует 88, а остальные получены искусственным путем. Число существующих простых веществ около 400, больше числа элементов, что объясняется явлением аллотропии.
Аллотропия – явление образования нескольких простых веществ одним элементом. Простые вещества, образованные одним и тем же элементом называются аллотропными видоизменениями(модификациями). Они могут отличаться составом молекул О2 – кислород, О3 – озон или структурой – алмаз, графит, карбин.
6. Ионами называются заряженные частицы, состоящие из отдельных атомов или групп химически связанных атомов, имеющих избыток или недостаток электронов. Для атомов элементов–металлов характерно образование положительно заряженных ионов т.е. катионов.
Na0 – 1e- = Na+
Для атомов элементов-неметаллов характерно образование отрицательно заряженных ионов т.е. анионов.
Cl0 + 1e- = Cl-
Атом– это электронейтральная частица, состоящая из положительно заряженного атомного ядра и отрицательно заряженных электронов (суммарный заряд которых равен нулю).
Массы атомов химических элементов чрезвычайно малы–от 1,674 ∙ 10-27 до 4,27 ∙ 10-25кг
m (H ) = 1,67 ∙ 10-27 кг
m (O) = 2,66 ∙ 10-26 кг
m (C) = 1,993 ∙ 10-26 кг
В химии пользуются не их абсолютными значениями масс (mа), а относительными (Аr, где r означает «относительный» - от английского relative).
Относительной атомной массой химического элемента называется отношение массы его атома к 1/12 массы изотопа углерода – 12С.
1/12 массы атома изотопа 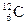 принята за атомную единицу массы (а. е. м.).
принята за атомную единицу массы (а. е. м.).
1а.е.м. = 1/12mа(С) = 1,993 ∙ 10-26/12 =1,667х10-27кг
В соответствии с этим:
ma(H) 1,674 ∙ 10-27 кг
Ar (Н) = ———— = —————— = 1,0079
1/12ma(C) 1,667 ∙ 10-27 кг
Относительная атомная масса – величина безразмерная.
ma(O) 2,66 ∙ 10-26
Аr (О) = ————— = ———— = 15,999
1/12ma(C) 1,667 ∙ 10-27
Относительная атомная масса показывает во сколько раз масса атома данного элемента больше 1/12 массы изотопа углерода. 12С. Например, относительная масса железа равна 56. Это означает, что атом железа 56Fе в 56 раз тяжелее 1/12 массы атома углерода.
Единицей измерения количества вещества является Моль.
Моль– это количество вещества, содержащее столько структурных единиц (молекул, атомов, ионов, электронов, эквивалентов и т.д.), сколько содержится атомов в 0,012 кг изотопа углерода 12С.
Число атомов (NА)в 0,012 кг углерода (т.е. в 1 моль) легко определить, зная массу атома углерода – 1,993х10-26 кг
Кг/моль
NА = ———————— = 6,02 ∙ 10 23 моль-1
Кг
Эта величина называется постоянной Авогадро.
Масса 1 моль вещества называется молярной массой(М) и она равна отношению массы этого вещества m к его количеству n.
M
M = —— г/мольили кг/моль
N
Численное значение молярной массы (в г/моль) совпадает с относительной молекулярной, атомной или формульной массой данного вещества. Например,
масса относительная молярная
Н2 — 2,0158 2,0158 г/моль
( NH4)2CO3 — 96,086 96,086 г/моль
Дата добавления: 2016-02-24; просмотров: 3494;
