БИОТЕХНОЛОГИЧЕСКИЕ ПРОЦЕССЫ В ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ 17 страница
На второй стадии (ацидогенез) в процессе ферментации участвуют две группы микроорганизмов: ацетогенные и гомоацетат- ные. Ацетогенные Н2-продуцирующие микроорганизмы ферментируют моносахариды, спирты и органические кислоты с образованием Н2, С02, низших жирных кислот, в основном ацетата, спиртов и некоторых других низкомолекулярных соединений. Деградация бутирата, пропионата, лактата с образованием ацетата происходит при совместном действии ацетогенных ^-продуцирующих и Н2-утилизирующих бактерий. Гомоацетатные микроорганизмы усваивают Н2 и С02, а также некоторые одноуглеродные соединения через стадию образования ацетил-КоА и превращения его в низкомолекулярные кислоты, в основном в ацетат.
На заключительной третьей стадии анаэробного разложения отходов образуется метан. Он может синтезироваться через стадию восстановления С02 молекулярным водородом, а также из метильной группы ацетата. Некоторые метановые бактерии способны использовать в качестве субстрата формиат, С02, метанол, метиламин и ароматические соединения:
4Н2 + С02---------- СН4 + 2Н20
ЗН2 + СО--------- СН4 + Н20
2Н20 + 4СО---------- СН4 + ЗС02
4НСООН --------- СН4 + ЗС02 + 2Н20
4СН3ОН --------- ЗСН4 + С02 + 2Н20
CHjCOOH------- СН4 + С02
Особое место в утилизации отходов занимает метановое сбраживание. Оно позволяет получать из местного сырья биогаз как локальный источник энергии, а также улучшать качество органического удобрения и защищать окружающую среду от загрязнений. Экологически чистые источники энергии не влияют отрицательно на окружающую среду. Современные источники энергии — ГЭС, ТЭС, АЭС — вызывают серьезные нарушения во внешней среде. ГЭС (гидроэлектростанции) служат причиной затопления территорий, изменения ландшафта, гибели биоценозов. ТЭС (теплоэлектростанции) загрязняют атмосферу, нарушают альголо- гический баланс, вызывают отчуждение земель. АЭС (атомные электростанции) создают угрозу радиационного загрязнения. Сжигание нефти и газа вызывает повышение концентрации С02, образование смога и, кроме того, уменьшение ресурсов нефти и газа.
90 —95 % используемого углерода метанообразующие бактерии превращают в метан и лишь 5—10% углерода превращаются в биомассу. В литературе имеются данные о способности метанооб- разующих бактерий в анаэробных условиях одновременно синтезировать и окислять метан.
В зависимости от температуры протекания процесса метановые бактерии разделяют на мезо- и термофильные. Оптимальная температура для мезофильных бактерий от 30 до 40 °С, а для термофильных от 50 до 60 °С. В целом термофильный процесс метаноге- неза идет интенсивнее мезофильного, притом в этих условиях анаэробной переработки отходов субстрат обеззараживается от патогенной микрофлоры и гельминтов. При анаэробной переработке отходов животноводческих ферм микрофлора метантенков (анаэробных ферментеров) формируется преимущественно из микрофлоры желудочно-кишечного тракта данного вида животных и микрофлоры окружающей среды. Из наиболее часто встречающихся культур следует отметить Lactobacillus acidophilus, Butyrivibrio Jibrisolvens, Peptostreptococcusproductus, Bacteroides uniformis, Eubacterium aerofa- ciens. К числу целлюлозоразлагающих бактерий микрофлоры жвач
ных относятся Bacteroides succinoqenes и Ruminococcus flavefaciens. 0з рубиа и навоза жвачных были изолированы такие метанообразующие бактерии, как Methanobacterium mobile, Methanobrevibacter rumi- nantium и Methanosarcina ssp. После определенного срока работы метантенка при установленном температурном режиме и на постоянном субстрате образуется сравнительно стабильный консорциум микроорганизмов. В ходе изучения микрофлоры свиного навоза при метановом брожении выделено около 130 различных бактерий.
Первую стадию разрушения сложных органических полимеров осуществляют бактерии из родов Clostridium, Bacteroides, Ruminococcus, Butyrivibro. Главные продукты ферментации — ацетат, про- пионат, сукцинат, Н2 и С02. Конечными продуктами ферментации целлюлозы и гемицеллюлозы под действием бактерий, выделенных из рубца жвачных и кишечника свиней, являются различные летучие жирные кислоты.
Бактерии второй, или ацетогенной, фазы, относящиеся к родам Syntrophobacter, Syntrophomonas и Desulfovibrio, вызывают разложение пропионата, бутирата, лактата и пирувата до ацетата, Н2 и С02 — предшественников метана. Ряд микроорганизмов способны синтезировать ацетат из С02 в термофильных условиях, к их числу принадлежат Clostridium formicoaceticum, Acetobacterium woodii, метановые бактерии из родов Methanothrix, Methanosarcina, Methanococcus, Methanogenium и Methanospirillum.
 отходов
Рис. 2.6. Схема устройства реактора для обработки сельскохозяйственных отходов
отходов
Рис. 2.6. Схема устройства реактора для обработки сельскохозяйственных отходов
|
Для получения биогаза можно использовать отходы сельского хозяйства, испорченные продукты, стоки крахмалперерабатыва- юших предприятий, жидкие отходы сахарных заводов, бытовые отходы, сточные воды городов и спиртовых заводов. Процесс ведется при температуре 30 — 60 °С и рН 6 —8. Этот способ получения биогаза широко применяют в Индии, Китае, Японии. В настоящее время для производства биогаза чаще используют вторичные отходы (отходы животноводства и сточные воды городов), чем первичные (отходы зерноводства, полеводства, хлопководства, пищевой, легкой, микробиологической, лесной и других отраслей), обладающие сравнительно низкой реакционной способностью и нуждающиеся в предварительной обработке. На рис. 2.6 представлена схема устройства реактора (метантенка) для обработки сельскохозяйственных отходов (навоз, остатки растениеводства). Подача отходов (суб
страта) и отбор отработанного стока осуществляются в нижней части реактора. Режим его работы может быть как периодическим, так и полунепрерывным. Реактор обычно имеет две (или более) секции для разделения стадий процесса.
Современное состояние проблем и перспектив в области получения биогаза свидетельствует о том, что анаэробная конверсия органических отходов в метан — наиболее конкурентоспособная область биоэнергетики. Основное преимущество биогаза состоит в том, что он является возобновляемым источником энергии. Его производство будет так же длительно, как существование жизни на Земле.
2.4. ПРОИЗВОДСТВО ЭТАНОЛА
Энергию можно получать из растений, богатых углеводами, превращая их в спирт (этанол). К ним относятся меласса, картофель, маниок, стебли кукурузы, злаки, топинамбур (земляная груша). Большое количество этанола получают из гидролизатов древесины лиственных пород или из сульфитных щелоков — отходов бумажных фабрик. Полученный спирт можно смешивать с бензином в соотношении 1:9 (или даже 1:4) и заправлять им машины.
Рост производства этанола связан с широтой его применения в химической промышленности. Он прекрасный растворитель, антифриз, экстрагент. Этанол служит также субстратом для синтеза многих растворителей, красителей, лекарственных препаратов, смазочных материалов, клеев, моющих средств, пластификаторов, взрывчатых веществ и смол для производства синтетических волокон. Его используют в двигателях внутреннего сгорания либо в безводном виде, либо в форме гидратированного этанола. Среди растений, продуцирующих этиловый спирт, следует выделить маниок, злаки (особенно кукурузу) и топинамбур, у которого запасным углеводом является инулин. Используются также сахарный тростник, ананас, сахарная свекла, сорго, у которых основной углевод — сахароза. При переработке сахарного тростника его тщательно давят, целлюлозу (жом) отделяют от сладкого сока и сжигают, а сок концентрируют, стерилизуют и подвергают брожению. Этот раствор отделяют от твердых компонентов и далее из 8—10%-го спиртового раствора путем перегонки получают этанол. Из оставшейся жидкости (стиллаж) после соответствующей переработки извлекают компоненты удобрений с выходом 2—3 %. «Барду» (кубовой остаток) после перегонки используют в качестве корма для сельскохозяйственных животных. Крахмал при его переработке сначала гидролизуют в сбраживаемые сахара. Производство этанола из мелассы с использованием жома
Совершенно очевидно, что один из наиболее перспективных методов крупномасштабного преобразования солнечной энергии основан на использовании биосистем. Широкое применение биосистем для получения энергии способно обеспечить свыше 15 % производства энергии для экономически развитых стран. В последние 10 — 15 лет намечены новые пути биотрансформации солнечной энергии при фотосинтезе. Установлено, что некоторые микробиологические системы характеризуются высокой эффективностью фотосинтеза. Так, фоторазложение воды, осуществляемое суспензией хлореллы с образованием кислорода, в оптимальных условиях культивирования дает 130 — 140 л газа с 1 м2 освещаемой поверхности в сутки. Известно, что одна из особенностей процесса фотосинтеза — уменьшение эффективности преобразования солнечной энергии при высоких значениях интенсивности света. Новые технологии позволяют повысить эффективность фотосинтеза при высокой интенсивности света. Разрабатываются системы, эффективно поглощающие световой поток и обогащенные реакционными центрами по отношению к пигменту. Световые кривые фотосинтеза улучшаются также с увеличением скорости лимитирующей стадии электронного транспорта. Например, проведение процесса при повышенных температурах в системах термофильных микроорганизмов увеличивает эффективность преобразования солнечной энергии при высокой интенсивности света.
2.6. ФОТОПРОИЗВОДСТВО ВОДОРОДА
Известно, что хлоропласты (например, из шпината) в присутствии искусственного донора электронов и бактериального экстракта, содержащего фермент гидрогеназу, способны продуцировать водород:
донор электронов фотосистема I -^-переносчик ё —«-гидрогеназа —*- н2Т
Гидрогеназа получает электроны от ферредоксина. В качестве доноров электронов используются различные органические соединения. Процесс сопровождается облучением видимым светом. Эта форма получения энергии имеет ряд достоинств: избыток субстрата фотолиза (воды); нелимитированный источник энергии (солнечный свет); не загрязняющий атмосферу водород. Водород обладает более высокой теплотворной способностью по сравнению с углеводородами, кроме того, процесс получения водорода — возобновляемый процесс, зависящий в основном от стабильности выделенных хлоропластов. Водород можно получать в присутствии искусственного донора ё" (вместо воды) и поглощающих свет пигментов, а не мембран хлоропластов. Его способны выделять и некоторые микроорганизмы, например цианобактерии (аэробные фототрофы) и др. При этом микробиологическое образование водорода может идти из соединений углеводного характера, включая крахмал и целлюлозу, а также из амино- и кетокислот.
Основная проблема создания систем конверсии энергии биомассы в водород связана с превращением этих метаболитов в топливную форму. Для биотехнологии можно было бы воспользоваться и другими механизмами превращения энергии, выявленными у микроорганизмов. Например, галофильная бактерия Halobacterium halobium способна использовать световую энергию, улавливаемую пурпурным пигментом (бактериородопсином), вмонтированным в мембрану клетки. Молекула пигмента состоит из одной полипептидной цепи, к которой прикреплена молекула ретиналя, являющегося светочувствительной частью пигмента. Под влиянием солнечного света изменяется конформация пигмента, приводящая к переносу ионов водорода (Н+) через мембрану. Пигмент является как бы протонным насосом. Молекулы бактериородопси- на располагаются в мембране триадами, и перекачивание протонов через мембрану обеспечивает градиент концентрации Н+ (ДН+), вследствие чего они движутся к наружной стенке, у которой пространство подкисляется и возникает электрохимический градиент (Ам."н)-
Предприняты попытки встраивания молекул пигмента в искусственные системы и повышения эффективности их использования. В частности, растущие бактерии Н. halobium переносят в мелкие водоемы с высокой концентрацией NaCl и других минеральных солей, в которых исключается загрязнение. У некоторых штаммов половина клеточной мембраны покрыта пурпурным пигментом, и из 10 л бактериальной культуры можно получить 0,5 г пурпурных мембран. В таких биомембранах содержится до 100000 молекул родопсина. Биомембраны фиксируют на особой подложке, которая должна обладать всеми свойствами, необходимыми для обеспечения тока протонов, а не других ионов. В частности, для этих целей вполне пригодны пористые подложки, пропитанные липидами, которые, сливаясь с мембраной, сплошным слоем покрывают поверхность фильтра. Мембранные фрагменты можно смешивать и с акриламидом с образованием геля. Вместо создания плотных слоев молекул бактериородопсин и липиды могут создавать протеолипосомы, которые встраивают в структуры, обеспечивающие эффективное перекачивание протонов.
У Н. halobium имеется и другой тип насоса, который обеспечивает галородопсин, использующий световую энергию непосредственно для перекачивания ионов. Изучение систем энергоконверсии чрезвычайно перспективно с точки зрения разработки искусственных устройств, более эффективных, чем естественные.
2.7. ОЧИСТКА СТОЧНЫХ ВОД
Важнейшая проблема экологической биотехнологии — очистка сточных вод. Потребность в воде в связи с ростом городов, бурным развитием промышленности, интенсификацией сельского хозяйства огромна. Ежегодный расход воды на земном шаре по всем видам водоснабжения составляет 3300 — 3500 км3, при это\ в сельском хозяйстве — 70 % всего водопотребления. Для производств химической, целлюлозно-бумажной, энергетической промышленности, черной и цветной металлургии и бытовых нужд1 населения требуется также значительное количество воды. Большая часть этой воды после ее использования возвращается в реки и озера в виде сточных вод.
На современном этапе выделяются следующие направления рационального расхода водных ресурсов: более полное использова ние и расширение воспроизводства ресурсов пресных вод; разработка новых биотехнологических процессов, позволяющих предотвратить загрязнение водоемов и свести к минимуму потребление свежей воды.
Загрязнение поверхностных и подземных вод можно подразделить на несколько типов: механическое, сопровождающееся повышением содержания механических примесей и относящееся т основном к поверхностным видам загрязнений; химическое, обусловленное присутствием в воде органических и неорганических веществ токсического и нетоксического действия; биологическое, связанное с наличием в воде разнообразных патогенных микроорганизмов, грибов и мелких водорослей; радиоактивное; тепловое
Основные источники загрязнения и засорения водоемов — недостаточно очищенные сточные воды промышленных и комму нальных предприятий, крупных животноводческих комплексов отходы производства при разработке рудных ископаемых (водь шахт, рудников); сбросы водного и железнодорожного транспор та; пестициды и т.д. Загрязняющие вещества, попадая в природные водоемы, качественно изменяют их состав.
Сточные воды содовых, сульфатных, азотно-туковых заводов обогатительных фабрик свинцовых, цинковых, никелевых руд содержащие кислоты, щелочи, ионы тяжелых металлов, меняю физические свойства воды (появление неприятных запахов, при вкусов и т.д.). Сточные воды нефтеперерабатывающих, нефтехи мических заводов, предприятий органического синтеза содержа" различные нефтепродукты, аммиак, альдегиды, смолы, феноль и другие вредные вещества. Вследствие окислительных процессо уменьшается содержание в воде кислорода, ухудшаются ее органические показатели.
Нефть и нефтепродукты — основные загрязнители внутреннк водоемов, вод и морей Мирового океана — создают разные фог мы загрязнения: плавающую на воде нефтяную пленку, осевшие на дно водоемов тяжелые фракции. Вода приобретает токсические свойства и представляет собой угрозу для всего живого: 12 г нефти челают непригодной для употребления 1 т воды. Вредным загрязнителем промышленных вод является фенол, содержащийся в сточных волах многих нефтехимических предприятий. На жизнь населения водоемов пагубно влияют сточные воды целлюлозно-бумажной промышленности. Окисление древесной массы сопровождается поглощением значительного количества кислорода, что приводит к гибели икры, мальков и взрослых рыб. Сточные воды, имеющие повышенную радиоактивность (100 кюри на 1 л и более), подлежат захоронению в подземные бессточные бассейны и специальные резервуары.
В значительной степени загрязняют водоемы моющие синтетические средства, широко используемые в быту, промышленности и сельском хозяйстве и парализующие жизнедеятельность бактерий. Пестициды, попадая в водоемы, накапливаются в планктоне, бентосе, рыбе и по цепочке питания попадают в организм человека, действуя отрицательно как на отдельные органы, так и на организм в целом. Сточные воды, содержащие отходы кожевенной и целлюлозно-бумажной промышленности, сахарных и пивоваренных заводов, предприятий мясомолочной, консервной и кондитерской промышленности, служат причиной органических загрязнений водоемов. Нагретые сточные воды тепловых электростанций вызывают тепловое загрязнение, которое резко изменяет термический режим, отрицательно влияет на флору и фауну водоемов. Возникают благоприятные условия для массового развития в водохранилищах синезеленых водорослей (так называемое «цветение воды»).
Методы очистки сточных вод (механические, химические, физико-химические и биологические). Применение того или иного метода в каждом конкретном случае определяется характером и степенью вредности примесей.
1. Механические методы. Сущность этих методов состоит в том, что из сточных вод путем отстаивания и фильтрации удаляют механические примеси. Грубодисперсные частицы в зависимости от размеров улавливаются решетками, ситами, песколовками, наво- зоуловителями, нефтеловушками и т.д. Механическая очистка позволяет выделять из бытовых сточных вод до 60 — 75% нерастворимых примесей, а из промышленных — до 95 %, многие из которых как ценные примеси используются в производстве.
2. Химический метод. В сточные воды добавляют различные химические реагенты, которые вступают в реакцию с загрязнителями и осаждают их в виде нерастворимых осадков. Химическая очистка уменьшает количество нерастворимых примесей до 95 %, а Растворимых — до 25 %.
3. физико-химические методы используют для удаления тонкодисперсных и растворенных неорганических примесей, а также разрушения органических и плохо окисляемых веществ. В арсенал этих методов входят электролиз, окисление, сорбция, экстракция, ионообменная хроматография, ультразвук, высокое давление и др.
4. Биологический метод основан на использовании закономерностей биохимического и физиологического самоочищения рек и других водоемов. Для очистки сточных вод используют биофильтры, биологические пруды и аэротенки.
В биофильтрах сточные воды пропускают через слой крупнозернистого материала, покрытого тонкой бактериальной пленкой, благодаря которой интенсивно протекают процессы биологического окисления. В биологических прудах в очистке сточных вод принимают участие все организмы, населяющие водоем.
Аэротенки — огромные резервуары из железобетона, в которых очистка происходит с помощью активного ила из бактерий и микроскопических животных, которые бурно развиваются в этих сооружениях, чему способствуют органические вещества сточных вод и избыток кислорода, поступающего с потоком подаваемого воздуха. Бактерии, склеивающиеся в хлопья, выделяют в среду ферменты, разрушающие органические загрязнения. Ил с хлопьями оседает, отделяясь от очищенной воды. Инфузории, жгутиковые, амебы, коловратки и другие мельчайшие животные, пожирая бактерии, не слипшиеся в хлопья, тем самым омолаживают бактериальную массу ила. Сточные воды сначала подвергают механической, а после химической очистке для удаления болезнетворных бактерий путем хлорирования жидким хлором или хлорной известью. Для дезинфекции используют также ультразвук, озонирование, электролиз и другие методы.
Биологический метод дает существенные результаты при очистке коммунально-бытовых стоков, а также отходов предприятий нефтеперерабатывающей, целлюлозно-бумажной промышленности и производства искусственного волокна. Однако он разрушает только относительно простые органические и аммонийные соединения.
Отстой сточных вод и его использование. В зависимости от степени обработки отстой городских сточных вод обычно делят на первичный (необработанный), состоящий из твердых веществ; вторичный — твердые вещества, выделяющиеся после вторичного отстоя, или отстой с биофильтров очистных сооружений; третичный — результат третичного отстоя сточных вод (известь и глина); отстой, перегнивший в анаэробных условиях.
До осушки отстой содержит большое количество влаги (до 95 %). После некоторой стабилизации отстоя, которая достигается путем его сбраживания, содержание твердых веществ составляет 30 %.
Доля содержания органической части в городских сточных водах колеблется от 50 % в перегнившем отстое до 70 % в необработанном отстое. Химический состав типичных отстоев составляет: азот __ до 2 %; фосфор (Р205) — 4%; калий — до 0,5 %. В небольших количествах обнаружены Cd, Си, Ni, Zn, Hg и Pb. Энергосодержание необработанного отстоя составляет около 16 284 кДж/год. Однако практическое использование отстоя в качестве топлива связано с рядом трудностей: высокое содержание влаги не позво- пяет использовать отстой без высушивания, на которое расходуется фактически вся выделяемая в процессе его горения энергия. При очистке сточных вод применяют и метановое брожение, которое осуществляется в реакторах (метантенках) в основном двух типов: в реакторах без фиксации биомассы и в реакторах с прикрепленной (фиксированной) биомассой. В качестве подложки, к которой прикрепляется биомасса, используют мелкий песок, окись алюминия и другие носители. В последнее время анаэробное метановое брожение применяют и для детоксикации стоков. Анаэробные бактерии помимо деградации углеводов, липидов, белков, нуклеиновых кислот способны разрушать и многие отходы нефтехимической промышленности, например бензойную кислоту:
4С6Н5СООН —- 15СН4 + 13С02
Адаптированные ассоциации анаэробов деградируют ацеталь- дегид, ацетон, бутанол, этилацетат, этилакрилат, глицерол, нитробензол, фенол, пропанол, пропиленгликоль, кротоновую, фу- маровую и валериановую кислоты, винилацетат, парафины, синтетические полимеры и многие другие вещества.
Глава 3
БИОТЕХНОЛОГИЯ ПРОИЗВОДСТВА МЕТАБОЛИТОВ
3.1. КЛАССИФИКАЦИЯ ПРОДУКТОВ БИОТЕХНОЛОГИЧЕСКИХ ПРОИЗВОДСТВ
Спектр продуктов, образующихся методами биотехнологии необычайно широк и разнообразен. Целевыми продуктами биотехнологических производств могут быть интактные клетки. Одноклеточные организмы используют для получения биомассы^ являющейся источником кормового белка. Клетки, особенно f иммобилизованном состоянии, выступают в роли биологических катализаторов для процессов биотрансформации.
Процессами биотрансформации называют реакции превращения исходных органических соединений (предшественников) в целевой продукт с помощью клеток живых организмов или ферментов, выделенных из них. В последние годы высокая специфичность процессов биотрансформации и эффективность иммобилизованных ферментов нашли широкое применение для крупномасштабного производства аминокислот, антибиотиков, стероидов и других промышленно важных продуктов.
Продуктами биотехнологических производств являются природные макромолекулы — белки, ферменты, полисахариды, по-

|
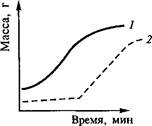
А Б
|
Рис. 3.1. Динамика изменения биомассы и образования первичных (А и вторичных (Б) метаболитов в процессе роста организма: / — биомасса; 2 — продукт
мов — продуцентов и оказались перспективными для оценки влияния на объекты различных факторов среды — ионов тяжелых металлов, кислот, щелочей и др. В 1983 г. С.Браун и С.Оливер использовали методы селекции для отбора мутантных штаммов дрожжей, устойчивых к высоким концентрациям конечного продукта (Ю %-го этанола), при культивировании их в непрерывном режиме (650 ч). Многолетняя селекция штаммов-продуцентов пенициллина позволила увеличить удельную активность антибиотика в культуральной среде в 400 раз, а штаммов бактерий, синтезирующих кобаламин, — в 10 раз. Методами мутагенеза и селекции получены штаммы Eremothecium ashbyii, способные выделять до 1,8 мг рибофлавина в 1 мл среды, и штаммы Brevibacterium ammo- niegenes, продуцирующие до 1 г HSKoA на 1 л среды.
Достижения в области молекулярной биологии и молекулярной генетики позволили биотехнологам начиная с 70-х годов прошедшего столетия перейти от слепого отбора штаммов мутантов к сознательному конструированию геномов, используя для этой цели прогрессивную технологию рекомбинантной ДНК.
Каждое из множества разнообразных веществ создается в клетке в строго необходимых для роста пропорциях в результате ферментативных реакций. Координация химических превращений. обеспечивающая экономность метаболизма, осуществляется у микроорганизмов тремя основными механизмами: регуляцией активности ферментов, в том числе путем ретроингибирования; регуляцией объема синтеза ферментов (индукция и репрессия биосинтеза ферментов); катаболитной репрессией.
| -ЦТ<Г |
В процессе ретроингибирования (ингибирование по принцип1 обратной связи) активность фермента, стоящего в начале многоступенчатого превращения субстрата, тормозится конечным ме таболитом, что детально разработано при изучении регуляции биосинтеза пиримидиновых нуклеотидов и новообразования ряда ами Нокислот:
Аспар-—► Карбамил—Дигидро- —»• Оротовая —»- Оротидин—-УМФ.
тат аспартат оротовая кислота монофосфат
_ кислота
Карбамил-
трансфераза ----------------------------------------------------------------------
| Глутамат - |
| N-ацетил- ■ глутамат... |
Орнитин —- Цитруллин — Орнитин
Ацетил- трансфераза
Хоризмат —»-Антранилат...—»- Индолил- —►Триптофан
глицерофосфат
Антранилат-
синтетаза
Таким способом низкомолекулярные метаболиты передают информацию об уровне своей концентрации и состоянии обмена веществ ключевым ферментам метаболизма. Ключевые ферменты — это регуляторы периодичности в процессе функционирования энзима и соответственно образования продукта. Эта ферменты предсгавле- НЬ1 в клетке аллостерическими белками, а конечные метаболиты — тдлостерическими эффекторами (активаторами и ингибиторами) ключевых энзимов. С помощью описанного механизма конечные продукты саморегулируют свой биосинтез. Ретроингибирование — способ точного и быстрого регулирования образования продукта.
На обмен веществ, аналогичный конечным метаболитам, оказывают эффект их аналоги (табл. 3.1). Указанное обстоятельство используется для селекции организмов с нарушением механизма обратной связи. Обход механизма ретроингибирования делает объект биотехнологического процесса нечувствительным к концентрации конечного продукта.
Таблица 3.1
Аналоги конечных метаболитов
|
Для отбора объектов продуценты выращивают на селективной среде, содержащей подходящий аналог или антиметаболит, которые не включаются в обмен веществ (в частности, аналоги аминокислот не включаются в состав белков), что ведет к подавлению роста организма. Выжившие мутанты обладают дефектами в механизме регуляции активности фермента по принципу обратной связи и поэтому служат важными объектами в обеспечении сверхсинтеза целевого продукта.
Среди тысяч энзимов, присущих микроорганизмам, одни, например ферменты гликолиза, синтезируются постоянно и их образование не зависит от состава питательной среды. Такие ферменты называют конститутивными. Другие энзимы, адаптивные или инду- цибельные, возникают только в ответ на появление в питательной среде индукторов — субстратов или их структурных аналогов. Так, Добавление (3-галактозида — лактозы к питательной среде, на которой культивируются клетки кишечной палочки Е. coli, вызывает мгновенное появление Р-галактозидазы в них, биосинтез которой в последующий период времени возрастает в 10000 раз. Установлено, что регуляция объема биосинтеза ферментов осуществляется на оперонном уровне (Ф.Жакоб и Ж. Моно, 1961) путем изменения количества иРНК, образующихся в процессе транскрипции.
Дата добавления: 2016-02-09; просмотров: 1024;
