Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон был открыт в 1969 г. русским ученым Д.И. Менделеевым.
Современная формулировка периодического закона:
свойства химических элементов, а также формы и свойства их соединения находящиеся в периодической зависимости от величины заряда ядер их атомов.
Заряд ядра (число протонов) равен атомному номеру, определяет число электронов в атоме, и, как следствие этого, строение его электрической оболочки в основном состоянии.
Графическим изображением периодического закона является таблица периодической системы элементов. Формы такого изображения различны. Их известно более 500, но наиболее широко используются три:
1) короткая (8-клетчатая)
2) полудлинная (18- клетчатая )
3) длиннопериодная (32- клетчатая)
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают четыре типа элементов: 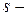 ,
, 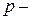 ,
, 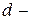 и
и 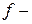 элементы.
элементы.
Периодом в периодической системе называется последовательный ряд элементов, электронная конфигурация внешнего энергетического уровня которых изменяется ns2 до ns2np6.
В вертикальных колонках, называемых группами, объединены элементы, имеющие сходное электронное строение. В короткопериодном варианте таблицы – 8 групп, каждая группа состоит из главной и побочной подгрупп.
Дата добавления: 2016-02-09; просмотров: 726;
