Статья Нитритометрия
Нитритометрия – метод титриметрического анализа, при котором в качестве титрованного раствора используется раствор натрия нитрита.
Применяется для количественного определения соединений, содержащих первичную или вторичную ароматическую аминогруппу, для определения гидразидов, а также ароматических нитросоединений после предварительного восстановления нитрогруппы до аминогруппы.
Методика.Если не указано иначе, точную навеску образца лекарственного средства, указанную в фармакопейной статье, растворяют в смеси 10 мл воды и 10 мл хлористоводородной кислоты разведенной 8,3 %. Прибавляют воду до общего объема 80 мл, 1 г калия бромида и при постоянном перемешивании титруют натрия нитрита раствором 0,1 М. В начале титрования прибавляют раствор натрия нитрита со скоростью 2 мл/мин, а в конце (за 0,5 мл до эквивалентного количества) – 0,05 мл/мин.
Титрование проводят при температуре раствора 15 - 20 ºС, однако в некоторых случаях требуется охлаждение до 0 - 5 ºС.
При потенциометрическом титровании в качестве индикаторного применяют платиновый электрод, в качестве электродов сравнения используют хлорсеребряный или насыщенный каломельный электрод.
При амперометрическом титровании на электроды накладывают разность потенциалов 0,3 - 0,4 В, если не указано иначе в фармакопейной статье.
Точку эквивалентности определяют электрометрическими методами (потенциометрическое титрование, титрование «до полного прекращения тока») или с помощью внутренних индикаторов и внешнего индикатора (йодкрахмальная бумага).
В качестве внутренних индикаторов используют тропеолин ОО (4 капли раствора), тропеолин ОО в смеси с метиленовым синим (4 капли раствора тропеолина ОО и две капли раствора метиленового синего), нейтральный красный (две капли в начале и две капли в конце титрования).
Титрование с тропеолином ОО проводят до перехода окраски от красной к желтой, со смесью тропеолина ОО с метиленовым синим – от красно-фиолетовой к голубой, с нейтральным красным – от красно-фиолетовой к синей. Выдержку в конце титрования с нейтральным красным увеличивают до 2 мин.
Титрование с йодкрахмальной бумагой ведут до тех пор, пока капля титруемого раствора, взятая через 1 мин после прибавления натрия нитрита раствора 0,1 М, не будет немедленно вызывать синее окрашивание на бумаге. В некоторых случаях выдержка может быть увеличена, о чем должно быть указано в фармакопейной статье.
Параллельно проводят контрольный опыт.
Кислотно-основное титрование
В неводных средах
Метод кислотно-основного титрования в неводных растворителях применяется для количественного определения веществ, титрование которых в воде затруднено или невозможно из-за их слабовыраженных в этой среде кислотно-основных свойств, малой растворимости, наличия в объектах анализа компонентов или примесей, полностью блокирующих возможность или нарушающих селективность титрования в водной среде.
В неводных средах кислотно-основные свойства различных веществ в сравнении с наблюдаемыми в воде могут сильно изменяться, причем эти изменения для различных классов веществ индивидуальны, что позволяет путем адекватного выбора среды обеспечивать не только самую возможность титрования, но и контролировать его селективность. Выбор среды позволяет регулировать кислотно-основные свойства веществ в растворах с целью создания оптимальных условий титрования.
Выбор растворителя при наличии необходимых литературных данных может осуществляться на основании величин констант титрования (Кт) илиих показателей (рКт). Эти величиныпозволяют прогнозировать не только возможность, но и точность титрования. Чем меньше величина Кт или больше величина рКт, тем выше вероятность оптимизации условий титрования. Константа титрования определяется как частное от деления ионного произведения растворителя (Кi) на константу диссоциации растворенного вещества (КА – для кислот, КВ – для оснований).
При титровании кислот:
KT = Ki ∙ KA-1, т. е. pKT = pKi − pKA.
При титровании оснований:
KT = KA = Ki ∙ KB-1, т. е. pKT = pKA = pKi − pKB.
При дифференцированном титровании смесей двух кислот или двух оснований: 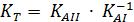 или
или  ,
,
где индексы I и II обозначают последовательность нейтрализации.
Значения величин ионных произведений для ряда растворителей и константы диссоциации некоторых кислот и оснований в воде и в различных растворителях приведены в приложении (табл. 1, 2 и 3).
Для соединений, принадлежащих к одному классу, часто имеет место линейная зависимость между значениями рКА в воде и неводном растворителе. Если эта зависимость изучена, ее можно использовать для предварительной оценки условий титрования в данном растворителе.
Оптимальные условия титрования для слабых кислот достигаются в основных растворителях, таких как пиридин, диметилформамид; а для слабых оснований – в кислых растворителях, таких как уксусная кислота, пропионовая кислота и уксусный ангидрид и, иногда, в нитрометане.
Соли некоторых органических и минеральных кислот могут быть оттитрованы как основания в кислых растворителях и, реже, как кислоты в основных растворителях.
Для раздельного титрования смесей кислот или оснований используют дифференцирующие растворители, т. е. растворители с величиной рKi,обычно превышающей 15, не обладающие выраженными кислотно-основными свойствами, такие как кетоны, нитрилы, нитрометан.
В ряде случаев для титрования применяют смеси неводных растворителей, один из которых является апротонным (бензол, хлороформ и др.). Присутствие апротонного растворителя уменьшает ионное произведение среды (Кi),что иногда способствует улучшению условий титрования.
При предварительном выборе условий кислотно-основного титрования конкретных веществ в неводных средах полезно руководствоваться таблицей.
Таблица – Растворители, индикаторы и титранты, рекомендуемые при кислотно-основном титровании в неводных средах
| Растворители | Индикаторы | Титранты |
| Кислые Уксусная, пропионовая, муравьиная кислоты, уксусный ангидрид и их смеси с другими растворителями | Кристаллический фиолетовый, судан III, тропеолин ОО, метиловый фиолетовый, нейтральный красный, малахитовый зеленый, диметиловый желтый | Раствор хлорной кислоты в уксусной кислоте или нитрометане |
| Основные Диметилформамид, пиридин, этилендиамин | Тимоловый синий, бромтимоловый синий, нафтолбензеин, нитроанилин | Растворы гидроксидов натрия и калия, натрия метилата, лития метилата, гидроксиды тетраэтил- и тетрабутиламмония в спирте метиловом или в его смеси с бензолом или толуолом |
| Дифференцирующие Ацетон, диоксан, нитрометан, метилэтилкетон, метанол, 2-пропанол, 2-метил-2-пропанол, диметилсульфоксид | Метиловый оранжевый, тимоловый синий, нейтральный красный, метиловый красный, бромтимоловый синий | Растворы хлористоводородной кислоты в спирте метиловом или в гликолевых смесях; растворы хлорной кислоты в нитрометане, метаноле или в гликолевых смесях; растворы, применяемые при титровании в основных растворителях |
Как кислоты можно титровать: фенолы, барбитураты, сульфамиды, аминокислоты, соли и другие соединения, способные к количественному депротонированию в основных растворителях.
Как основания можно титровать: амины, азотсодержащие гетероциклические соединения, амиды, соли и другие соединения, способные к протонированию в кислых растворителях.
В ряде случаев титрование возможно только в результате взаимодействия титруемого соединения со вспомогательным реактивом перед титрованием или в процессе титрования. В частности, при титровании как оснований солей галогеноводородных кислот (титрант – 0,1 М раствор хлорной кислоты), в титруемый раствор прибавляют в избытке ртути(II) ацетат, что приводит к образованию недиссоциирующих комплексных галогенидов ртути и эквивалентного количества легко и количественно протонирующихся ацетат-ионов. В среде уксусного ангидрида титруют как основания тем же титрантом соли хлористоводородной кислоты без использования ртути(II) ацетата, поскольку в этой среде в отсутствие воды количественно протонируются непосредственно хлорид-ионы, что в обычных растворителях неосуществимо.
Возможно титрование как оснований соединений, содержащих в молекуле азиридиновые или оксирановые циклы. Для его реализации необходимо присутствие в титруемом растворе избытка нуклеофилов – бромид- или йодид-анионов. Тогда при титровании в среде кислых растворителей или нитрометана (титрант – 0,1 М раствор хлорной кислоты) количественно и быстро происходит раскрытие азиридиновых или оксирановых циклов с присоединением протона и аниона-нуклеофила. Таким образом, соединения, содержащие эти циклы, титруются как основания, но процесс практически необратим, поскольку не приводит к образованию катионов определяемых соединений.
Титрование в неводных средах может быть проведено как с индикаторами, так и потенциометрически с использованием в качестве индикаторного стеклянного или любого другого электрода, обратимого по отношению к протону. В качестве электрода сравнения обычно применяют либо хлорсеребряный, либо каломельный электрод. При проведении потенциометрического титрования целесообразно использовать электролитический мост, заполненный насыщенным раствором калияхлорида или лития перхлората в метаноле. Это предотвращает попадание воды в титруемый раствор и возрастание электрического сопротивления моста в процессе титрования. Использование лития перхлората, как контактного электролита, необходимо, если титрование оснований проводят в протогенной среде в присутствии ртути(II) ацетата или уксусного ангидрида, то есть когда попадание в титруемый раствор даже следов калия хлорида недопустимо.
При титровании в основных растворителях следует принимать меры для защиты титруемого раствора и особенно титранта от углекислого газа, содержащегося в воздухе. Титрование в этилендиамине и пиридине лучше проводить в атмосфере инертного газа (азота или аргона).
Оптимальный объем титруемого раствора составляет от 30 до 50 мл, целесообразная величина расхода титранта в пределах от 5 до 9 мл.
В ряде случаев, особенно при меняющемся в процессе титрования составе среды и при инструментальной индикации точки эквивалентности, проведение контрольного опыта обычным путем неосуществимо. В таком случае проводят титрование двух разных навесок определяемого вещества. Величина разности расходов титранта на эти навески не должна быть меньше 5 мл. Расчет результата определения ведется по величине этой разности, отнесенной к разности навесок, что исключает ошибку, связанную с нецелевым расходом титранта, практически одинаковую при титровании каждой из навесок.
Приложение
Табл. 1 – Величины pKi различных растворителей (pKi = −lg Ki) при температуре от 20 до 25 °С
| № п/п | Растворитель | pKi |
| Серная кислота | 3,62 | |
| Муравьиная кислота | 6,1 | |
| Уксусная кислота | 14,4 | |
| Уксусный ангидрид | 14,5 | |
| Этилендиамин | 15,3 | |
| Этиленгликоль | 15,6 | |
| Формамид | 16,7 | |
| Метанол | 16,7 | |
| Пропиленгликоль | 16,8 | |
| Диэтиленгликоль | 17,5 | |
| Этанол | 19,1 | |
| н-Бутанол | 20,1 | |
| Метилцеллозольв | 20,7 | |
| Изопропанол | 22,0 | |
| Диметилацетамид | 23,9 | |
| Нитрометан | 24,0 | |
| N-Метилпирролидон | 24,2 | |
| Пиридин | 24,2 | |
| Диметилформамид | 25,3 | |
| Метилбутилкетон | 25,3 | |
| Метилэтилкетон | 25,7 | |
| Ацетон | 25,9 | |
| Ацетонитрил | 32,2 | |
| Диметилсульфоксид | 33,3 |
Табл. 2 – Величины рКА кислот в различных растворителях (pКА = − lg КА)
| Кислота | Растворитель | ||||||||||||||||||||
| Вода | Метанол | Спирт 95 % | Бутанол | Изопропанол | Этиленгликоль | Пропиленгликоль | Метилцеллозольв | Ацетон | Метилизобутилкетон | Метилэтилкетон | Формамид | Диметилформамид | Диметилсульфоксид | Ацетонитрил | Нитрометан | N-метилпирролидон | Пиридин | Уксусная кислота | Муравьиная кислота | Уксусный ангидрид | |
| Азотная | 0,2 | 3,17 | 3,75 | 4,66 | 8,80 | 4,30 | 5,10 | 8,20 | |||||||||||||
| Ацетилсалициловая | 3,50 | 16,30 | 11,30 | ||||||||||||||||||
| Барбитуровая | 4,01 | 6,67 | |||||||||||||||||||
| Бензойная | 4,20 | 9,52 | 10,13 | 10,24 | 8,16 | 8,83 | 10,70 | 11,95 | 16,6 | 6,36 | 12,20 | 11,10 | 20,70 | 19,60 | 12,30 | 9,80 | |||||
| Винная | 3,03 | 7,40 | 8,90 | ||||||||||||||||||
| Дихлоруксусная | 1,31 | 6,30 | 7,14 | 7,30 | 7,80 | 4,50 | 10,20 | 10,26 | 15,80 | 14,10 | 8,30 | ||||||||||
| Лимонная | 3,10 | 10,1 | 10,60 | ||||||||||||||||||
| Монохлоруксусная | 2,86 | 7,80 | 8,51 | 8,50 | 9,23 | 6,05 | 9,10 | 11,20 | 15,4 | 4,50 | 10,10 | 8,90 | 18,80 | 17,0 | 10,90 | ||||||
| Муравьиная | 3,75 | 9,15 | 9,70 | 16,70 | 5,74 | 11,55 | 12,0 | 8,84 |
| Никотиновая | 4,73 | 16,60 | 15,0 | 10,80 | 9,60 | ||||||||||||||||
| п-Аминобензойная | 4,92 | ||||||||||||||||||||
| Пикриновая | 0,80 | 4,80 | 3,93 | 4,50 | 3,70 | 3,17 | 11,0 | 3,70 | 1,33 | 3,65 | 1,0 | 11,0 | 10,50 | 3,65 | |||||||
| п-Нитробензойная | 3,40 | 8,40 | 8,87 | 9,10 | 9,60 | 10,59 | 5,88 | 10,60 | 9,0 | 18,70 | 17,60 | 10,50 | 7,94 | ||||||||
| п-Толуолсульфоновая | 1,55 | 5,30 | 2,68 | 0,34 | |||||||||||||||||
| Салициловая | 2,89 | 7,90 | 8,60 | 7,73 | 8,90 | 9,53 | 13,0 | 4,73 | 8,30 | 6,80 | 16,70 | ||||||||||
| Серная | 1,44 | 3,42 | 5,48 | 3,10 | 4,60 | 5,10 | 4,25 | 0,58 | 4,90 | ||||||||||||
| Сульфадимезин | 7,51 | 19,60 | 18,70 | 13,0 | |||||||||||||||||
| Сульфадиметоксин | 5,90 | ||||||||||||||||||||
| Трихлоруксусная | 0,70 | 4,90 | 5,70 | 6,30 | 5,90 | 8,20 | 8,86 | 1,46 | 10,60 | ||||||||||||
| Уксусная | 4,75 | 9,70 | 10,41 | 10,35 | 11,35 | 8,32 | 9,10 | 11,10 | 12,55 | 16,6 | 6,91 | 13,50 | 12,60 | 22,30 | 20,50 | 13,30 | 11,44 | ||||
| Фенилуксусная | 4,31 | 8,06 | 8,78 | 6,57 | 12,90 | 11,60 | 20,10 | ||||||||||||||
| Фенобарбитал | 7,21 | 19,20 | 13,30 | 13,40 | 10,98 | ||||||||||||||||
| Хлористоводородная | 0,8 | 1,05 | 1,95 | 3,10 | 8,90 | 8,30 | 6,20 | 8,10 | 4,08 | 5,40 | 5,30 | 0,89 | 8,30 | ||||||||
| Хлорная | 2,90 | 2,20 | 1,90 | 2,23 | 3,23 | 2,70 | 0,28 | 0,90 |
Продолжение табл. 2
Табл. 3 – Величины рКА оснований в различных растворителях (pКА = pКi − pКВ = pКТ)
| Основание | Растворитель | |||||||||||||||||
| Вода | Метанол | Спирт 95% | Этиленгликоль | Пропиленгликоль | Метилцеллозольв | N-метилпирролидон | Муравьиная кислота | Уксусная кислота | Уксусный ангидрид | Ацетон | Метилэтилкетон | Метилизобутилкетон | Формамид | Диметилформамид | Диметилсульфоксид | Нитрометан | Ацетонитрил | |
| Аденин | 9,90 | 13,70 | ||||||||||||||||
| Аммиак | 9,30 | 11,70 | 10,10 | 9,45 | 10,50 | 15,70 | 16,46 | |||||||||||
| Анилин | 4,58 | 6,10 | 5,70 | 6,12 | 6,12 | 5,49 | 8,60 | 5,92 | 9,63 | 4,10 | 4,36 | 3,60 | 9,07 | 10,56 | ||||
| Ацетамид | 0,48 | 6,75 | 8,60 | 9,50 | ||||||||||||||
| Ацетанилид | 0,40 | 6,80 | 7,30 | |||||||||||||||
| Бензиламин | 9,62 | 11,30 | ||||||||||||||||
| Гидразин | 8,11 | 11,10 | ||||||||||||||||
| Гуанозин | 12,40 | 15,0 |
Продолжение табл. 3
| Дибазол | 4,20 | 9,00 | 6,40 | |||||||||||||||
| Димедрол | 8,20 | 7,70 | ||||||||||||||||
| Диметиламин | 10,60 | 10,0 | 10,40 | 17,96 | 18,73 | |||||||||||||
| Диметиланилин | 5,10 | 4,50 | 4,40 | 9,93 | 4,91 | 6,20 | 2,51 | 11,04 | ||||||||||
| Дифениламин | 0,90 | 3,18 | 7,45 | 3,87 | 5,24 | |||||||||||||
| Диэтиламин | 10,90 | 12,20 | 9,20 | 5,19 | 10,10 | 13,44 | 10,10 | 10,50 | 17,95 | 18,70 | ||||||||
| Диэтиланилин | 6,52 | 10,20 | 10,60 | 6,26 | 7,20 | |||||||||||||
| Кодеин | 8,00 | 8,60 | 11,40 | 9,38 | 5,11 | 10,80 | 9,62 | 11,18 | 8,30 | |||||||||
| Кофеин | 0,60 | 5,17 | 6,30 | |||||||||||||||
| Мочевина | 0,20 | 4,67 | 7,65 | 9,36 | ||||||||||||||
| α-Нафтиламин | 3,92 | 5,66 | 5,10 | 5,05 | 9,60 | 5,42 | 6,38 | |||||||||||
| Новокаин | 8,80 | 11,30 | 8,60 | |||||||||||||||
| Папаверин | 5,90 | 6,92 | 7,25 | 10,80 | 8,03 | 6,60 | ||||||||||||
| Пилокарпин | 6,80 | 10,90 | ||||||||||||||||
| Пиперидин | 11,20 | 11,0 | 12,51 | 12,52 | 11.71 | 10,40 | 10,1 | 12,24 | 13,48 | 11,08 | 10,40 | 18,22 | 18,92 | |||||
| Пиридин | 5,15 | 5,54 | 4,30 | 5,92 | 5.69 | 5,50 | 10,0 | 9,90 | 5,77 | 6,94 | 4,43 | 3,30 | 3,40 | 12,16 | 19,33 | |||
| Промедол | 8,40 | 11,30 | 14,40 | 8,20 |
Продолжение табл. 3
| Теобромин | 0,10 | 5,26 | 6,10 | |||||||||||||||
| Теофиллин | 2,60 | 6,60 | ||||||||||||||||
| Трибутиламин | 9,85 | 10,10 | 17,77 | 18,10 | ||||||||||||||
| Триэтиламин | 10,70 | 11,15 | 10,87 | 8,70 | 10,20 | 11,50 | 11,62 | 12,40 | 9,99 | 9,25 | 9,0 | 18,35 | 18,46 | |||||
| Цитидин | 9,80 | 13,20 | ||||||||||||||||
| Эфедрин | 9,70 | 11,29 | 8,90 |
Дата добавления: 2016-01-30; просмотров: 2248;
