Кристаллизация изоморфных смесей.
Изоморфизм - способность атомов, ионов или молекул замещать друг друга в кристаллических структурах. В результате изоморфизма образуются твёрдые растворы замещения. Вещества, которым присущ изоморфизм, называют изоморфными.
При изоморфизме в минералах химические элементы (атомы или ионы) замещают друг друга в кристаллической решетке минерала не меняя при этом его структуру (Собственно изоморфизм). Изоморфные вещества могут кристаллизоваться совместно, давая смешанные кристаллы - изоморфные смеси. Эти смеси образуются лишь тогда, когда замещающие друг друга частицы (атомы, ионы, молекулы) близки по своим эффективным размерам. Согласно правилу Гольдшмидта, образование изоморфных смесей с широким диапазоном концентраций возможно при тождестве знака заряда и близкой поляризуемости замещающих друг друга атомов или ионов, если их ионные радиусы различаются не более чем на 15%. Если два вещества дают изоморфные смеси любых концентраций (непрерывный ряд твердых растворов), то изоморфизм называют совершенным. В противном случае говорят о несовершенном (или ограниченном) изоморфизме. Совершенный изоморфизм характерен только для изоструктурных веществ, имеющих сходное пространственное расположение атомов или ионов и поэтому сходные по внешней форме кристаллы. Для ограниченного изоморфизма условие изоструктурности необязательно
Углеродный цикл.
Вся земная жизнь основана на углероде. Каждая молекула живого организма построена на основе углеродного скелета. Атомы углерода постоянно мигрируют из одной части биосферы в другую. На примере круговорота углерода в природе можно проследить в динамике картину жизни на нашей планете.
Основные запасы углерода на Земле находятся в виде содержащегося в атмосфере и растворенного в Мировом океане диоксида углерода, то есть углекислого газа (CO2).
17-1. Распределение вещества в Солнечной системе. Закон Тициуса – Бодэ
В спектре солнечной атмосферы открыто более 70 элементов с преобладанием Н (70 % по массе), Не (28%), на долю остальных приходится 2 %. Очень мало тяжелых элементов по-
сле железа. В порядке уменьшения обнаружены следующие 13 элементов: H, He ,O,C, N, Si, Mg, Ne, Fe, S, Ca, Ni, Ar. Ядерные реакции зависят от температуры звезд. Энергетически более выгодно образование устойчивых ядер с небольшим числом четного количества протонов и нейтронов, поэтому в космосе и на
Земле преобладают элементы с небольшими атомными массами. Солнце представляет собой водородно-гелиевый раскаленный шар. Газовые туманности состоят из сильно разреженных газов, (Н,О).В космических лучах космические нейтроны образуют вторичные радиоактивные изотопы(12C.10Be, 22Na,26Al, 32Si, 36Cl, 39Ar.) в верхней части атмосферы, преобразуя атомные ядра азота.Космические частицы богаче тяж.ме. метеориты по составу бывают металлические (Fe, Ni), силикатные (Si, Al), сульфидные (FeS и др.).
Правило Тициуса — Боде (известно также как закон Боде) представляет собой эмпирическую формулу, приблизительно описывающую расстояния между планетами Солнечной системы и Солнцем (средние радиусы орбит)
. 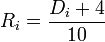 Полученное число считается радиусом орбиты i-й планеты в астрономических единицах.
Полученное число считается радиусом орбиты i-й планеты в астрономических единицах.
Планета-i
Меркурий −1
Венера 0
Земля 1
Марс 2 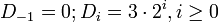
Т.о.
Di=0,3,6,12..
И например для венеры теор.раст=(3*2^0+4)/10=0.7(на самом деле=0.72)
Дата добавления: 2016-01-26; просмотров: 1498;
