Метод избыточных концентраций
Наиболее просто и точно задача определения порядка реакции решается в том случае, если скорость реакции может быть получена как функция концентрации только одного из реагентов. Для того, чтобы скорость реакции зависела только от концентрации одного из исходных веществ, обычно используют способ избыточных концентраций, называемый также методом понижения порядка реакций.. По этому методу, предложенному Оствальдом, проводят серию опытов, в каждом из которых изучается влияние концентрации только одного из исходных веществ на скорость реакции. Для этого все остальные исходные вещества берут в таком избытке по сравнению с исследуемым, чтобы их концентрации можно было считать практически постоянными. Определяют порядок реакции по каждому из исследуемых исходных веществ одним из перечисленных ниже способов. Затем определяют общий порядок реакции.
Рассмотрим формально простую реакцию n1-го порядка по веществу 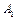 и n2 — по
и n2 — по 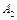
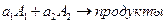 .
.
Зависимость этой реакции от концентрации исходных веществ описывается выражением
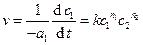 . (4.47)
. (4.47)
Общий суммарный порядок реакции равен сумме порядков реакции по отдельным исходным веществам: 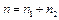 . Если реакция является элементарной или формально простой, но подчиняется кинетическому уравнению для элементарной реакции, то порядок по веществам
. Если реакция является элементарной или формально простой, но подчиняется кинетическому уравнению для элементарной реакции, то порядок по веществам 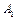 и
и 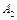 равен стехиометрическим коэффициентам в уравнении, а общий порядок равен их сумме
равен стехиометрическим коэффициентам в уравнении, а общий порядок равен их сумме 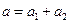 .
.
Проведем реакцию сначала в условиях, когда концентрация исходного вещества 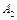 по сравнению с концентрацией
по сравнению с концентрацией 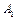 избыточна. Т. е. считаем, что при протекании реакции меняется только концентрация вещества
избыточна. Т. е. считаем, что при протекании реакции меняется только концентрация вещества 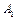 , а концентрация вещества
, а концентрация вещества 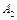 остается практически постоянной и ее можно ввести в постоянный коэффициент. При этом уравнение (4.47) примет вид
остается практически постоянной и ее можно ввести в постоянный коэффициент. При этом уравнение (4.47) примет вид
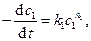 (4.48)
(4.48)
где 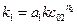 частный порядок реакции по первому компоненту.
частный порядок реакции по первому компоненту.
Затем проводим реакцию при избытке вещества 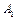 . Тогда получаем уравнение
. Тогда получаем уравнение
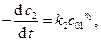 (4.49)
(4.49)
где 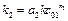 частный порядок реакции по второму компоненту.
частный порядок реакции по второму компоненту.
Если определить порядок реакции по данному исходному веществу, то можно определить общий порядок реакции, а затем и константу скорости реакции
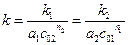 . (4.50)
. (4.50)
Методы определения порядка реакции по данному веществу подразделяются надифференциальные и интегральные в зависимости от того, используют они интегральные или дифференциальные кинетические уравнения для обработки экспериментальных данных зависимости концентрации реагирующих веществ от времени.
Дата добавления: 2016-01-09; просмотров: 993;
