Упражнения для самостоятельного решения
1. Определите степень окисления хрома в следующих соединениях:
Сг2О3 ,К2Сг2О7 ,Сг2(SO4)3,Fe(CrO2)2 .
2. Укажите, какие из приведенных процессов представляют собой окисление и какие — восстановление:
а)S→ SO42- ; б)Br2 → 2Br -; в)V2+→ V03– ; г)Cl–→ ClO3– .
3. Укажите, какиеиз следующих реакций относятся к окислительно-восстановительным:
а) NH4Cl= NH3 + HCl; б) 2K2CrO4+ H2SO4 = К2Сг2O7+ К2S04+ Н2О;
в) Fe + S = FeS ; г) H2 + Cl2 = 2 HCl.
4. Укажите, в каких из следующих реакций азот является окислителем, в каких— восстановителем:
а) N2+O2= …; б) N2 + Li =… ; в) N2+Mg = … г) N2 + H2= …
5. Составьте уравнения полуреакций:
а) MпО4–→ Mnz+ (рН<7); б)Cr02– → СгО42– (рН>7); в)SO32–→ SO42– (рН=7).
6. Закончите уравнения .реакций:
а) HClO3 →ClO2 + HClO4 + Н20 ; б) NH4NO3 →N2О + H20;
в) KI+ K2Cr207+ H2.SO4 →.I2 + . . .; г) Al + HNO3 →NH4NO3 + ...
7. По приведенным ниже полуреакциям составьте уравнения окислительно-восстановительных реакций в молекулярном виде:
a) 10 Fe2+ → 10Fe3+ + 10e
2МпО4– + 16Н+ + 10е →2Mn2+ + 8Н2О
б) 3Mg° → ЗMg2+ +6e
SO4 2– + 8Н+ + 6е → S0 + 4Н2О
8. Напишите следующие окислительно-восстановительные реакции:
а) Na2S + К2 Сг2 О7 + Н2S04 →…; б) Н202 + KI →…;
в) РН3.+ KMnO4 + HCl → …. ; г) NaClO + CrCL3 + NaOH →. . .
9. В 1 л раствора содержится 10г HCl04 .Вычислите нормальность HClO4 , исходя из реакции: SO2 + HClO4 + Н20 → HCl + Н2SO4
Ответ: c(1/8HClO4) = 0,8 моль/л.
10. Какой обьём 0,1Н К2Сг207 потребуется для окисления 20мл 0,02М Na2SО3 в кислой среде?
Ответ: 8мл.
ХИМИЧЕСКАЯ СВЯЗЬ
Химическая связь – это совокупность сил между атомами, образующая устойчивые системы: молекулы, ионы, радикалы.
Основные типы химической связи: ковалентная, ионная, водородная и металлическая.
Нет единой теории описывающей все молекулы. Отнесение химической связи к одному из этих типов – не является простой задачей. В большинстве соединений имеет место наложение разных типов связи.
Учение о химической связи составляет основу теоретической химии.
Квантовая механика дала решение вопроса о природе химической связи.
Гейтлер и Лондон нашли приближённое решение уравнения Шредингера для молекулы Н2, подойдя к ней как к системе, состoящей из двух атомов водорода. Они исходили из предположения, что при образовании молекулы из атомов атомы сохраняют свою электронную конфигурацию, а силы связывания между атомами обусловлены обменом электронов между ними в результате спаривания спинов двух электронов, находящихся на атомных орбиталях.
Гейтлер и Лондон показали:
а) уравнение Шредингера справедливо не только для атома, но и для молекулы;
б) химическая связь имеет электрическую природу, так как в уравнении Шредингера в качестве потенциальной энергии рассматривалась только энергия электростатического взаимодействия ядер и электронов, а результаты опытов удовлетворительно согласуются с расчётом;
Результаты расчёта энергии электронов в молекуле Н2 представлены на рис.2.
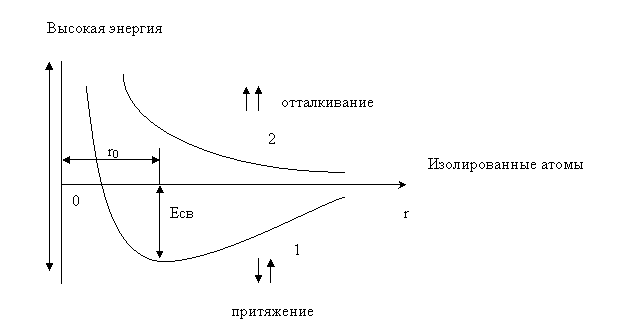
Рис.2 Зависимость потенциальной энергии Е системы из двух атомов водорода от межъядерного расстояния r :
1– при образовании химической связи; 2 – без её образования.
Расчёт Гейтлера и Лондона показал, что если электроны атомов водорода обладают противоположно направленными спинами, то при сближении атомов происходит значительное уменьшение энергии (кривая1) —возникает химическая связь. Образование химической связи обусловлено тем, что при наличии у электронов антипараллельных спинов становится возможным передвижение электронов около обоих ядер, что приводит к значительному увеличению плотности электронного облака в пространстве между ядрами, которое удерживает вместе положительно заряженные ядра, поскольку пребывание двух электронов в поле двух ядер энергетически выгоднее нахождения каждого из них в поле одного ядра. Притяжение уменьшает потенциальную энергию системы — возникает химическая связь.
На рис.2 показана энергетическая кривая, характерная для взаимодействующих атомов водорода. Сближение атомов сопровождается выделением энергии, которое будет тем больше, чем больше перекроются электронные облака. Однако в обычных условиях, вследствие кулоновского отталкивания, невозможно достичь слияния ядер двух атомов. Значит, на каком-то расстоянии вместо притяжения атомов, будет происходить их отталкивание. Таким образом, расстояние между атомами r0, которому отвечает минимум на энергетической кривой, будет соответствовать длине химической связи (кривая 1). Если же спины электронов у взаимодействующих атомов водорода одинаковы, то будет происходить их отталкивание (кривая 2). Энергия связи для различных атомов изменяется в пределах 170–420 кДж/моль.
Причина образования химической связи – понижение полной энергии системы.
При разработке теории строения молекул в начале 30-х годов возникли и развивались два метода — метод валентных связей МВС (Гейтлер и Лондон, Полинг, Слейтер и др.) и метод молекулярных орбиталей ММО(Малликен, Гунд,Хюккель и др).
При расчётах с большой точностью оба метода дают практически одинаковые результаты, но в более простом приближении каждый из них имеет какие то преимущества в описании одних явлений и недостатками при описании других. В методе валентных связей МВС каждую молекулу рассматривают составленной из атомов, а для объяснения электронного строения молекулы применяются атомные орбитали составляющих её атомов. В методе молекулярных орбиталей ММО молекулу рассматривают как самостоятельное целое, а не простую совокупность атомов.
Метод валентных связей МВС можно использовать и для расчёта многоатомных молекул, но такие расчёты не получили широкого распространения. В последнее время развивается новый подход, который синтезирует идеи двух методов (МВС и ММО)— обобщённый метод валентных связей.
Ковалентная связь
Дата добавления: 2016-01-07; просмотров: 971;
