Упражнения и задачи для самостоятельного решения. 1. Напишите выражения констант химического равновесия Кс следующих обратимых реакций (V = const
1. Напишите выражения констант химического равновесия Кс следующих обратимых реакций (V = const. Т = const)
а)N2(г) + 3H2(г) = 2NH3(г)
б)C(тв)+ CO2(г) =2CO(г)
в)4HCl(г) +O2(г) = 2H2O(г) + 2Cl2(г)
г)2NO2(г) =2NO(г) +O2(г)
2. В каком направлении смещено равновесие в реакции Н2(г)+ J2(г)= 2HJ(г), если при некоторой температуре константа равновесия Кс>1?
Ответ: вправо; в сторону увеличения равновесной концентрации HI.
3. С ростом температуры равновесие в реакции
N2(г) + O2(г)= 2NO(г) сдвигаетсяв сторону прямой реакции.
Сделайте вывод о знаке энтальпии реакции.
Ответ: ∆Нр-ции >0
4. При некоторой температуре константа равновесия реакции А=В равна 4.
Как изменится константа равновесия реакции, если концентрацию вещества А увеличить в 10 раз?
Ответ: не изменится
5. При температуре 298К константа равновесия реакции А=В равна 4×10-4, а при температуре 1000К равна 5×10-6. Экзотермическая или эндотермическая эта реакция?
Ответ: экзотермическая
6. Как повлияет повышение давления на состояние равновесия системы: СН4(г) = С(тв) + 2Н2(г) ?
Ответ: равновесие сместится влево.
7. Как повлияет понижение температуры на величину константы равновесия реакции N2(г)+ ЗН2(г)=2 NH3(г), если стандартная энтальпия реакции –92,4кДж.
Ответ: Величина константы равновесия увеличится.
8. Исходные концентрации СО и Н2О соответственно равны
0,08 моль/л, а СО2 и Н2 — 0 моль/л. Вычислите равновесные концентрации СО, Н2О и Н2 в системе
СО(г)+ Н20(г)= СО2(г)+ Н2(г), если равновесная концентрация СО2 оказалась равной 0,05моль/л.
Ответ: [CO] = 0,03 моль/л; [H2O] = 0,03 моль/л; [H2] = 0,05 моль/л.
9. Равновесие реакции 4HCl(г) + 02(г)= 2H2O(г)+ 2Cl2(г) установилось
при следующих концентрациях реагирующих веществ (в моль/л):
[Н2О] = [Cl2 ] = 0.4; [HCl] = [О2] = 0.2. Вычислите константу равновесия Кс и исходную концентрацию кислорода в реакционной смеси.
Ответ: Кс = 200; [O2]исх = 0,6 моль/л.
РАСТВОРЫ
Основные понятия. Образование растворов
Растворами называются однородные системы, состоящие из двух и более компонентов, состав которых можно изменять в определённых пределах без нарушения однородности. Растворы бывают газовые, жидкие и твёрдые. В химии, биологии и медицине чаще всего приходится иметь дело с жидкими растворами. В жидких растворах принято различать растворитель и растворённое вещество. Растворителем называют (чаще всего) тот компонент раствора, которого больше, либо тот компонент, который не меняет своего агрегатного состояния при растворении.
Причина образования истинного раствора ― уменьшение энергии Гиббса в результате взаимодействия компонентов раствора ΔGрастворения < 0.
При внесении растворяемого вещества в растворитель процесс растворения идёт самопроизвольно (ΔGрастворения < 0) и раствор остаётся ненасыщенным. Когда энтальпийный и энтропийный факторы процесса станут одинаковыми, т.е. ΔGрастворения = 0, система окажется в состоянии истинного равновесия. Раствор становится насыщенным.
Таким образом, раствор — это равновесная однородная система,которая достигла минимума энергии Гиббса в результате взаимодействия всех её частиц за счёт всех возможных типов взаимодействия между ними.
Можно получить и пересыщенный раствор, т.е. такой, концентрация которого выше концентрации насыщенного раствора (при данной температуре и давлении). Такой раствор получается при осторожном и медленном охлаждении насыщенных при высокой температуре растворов. Пересыщенный раствор представляет собой систему, находящуюся в кажущемся равновесии (∆G>0). Встряхивание или внесение в раствор кристаллов того же вещества вызывает кристаллизацию и раствор становится насыщенным.
Растворимость данного вещества определяется концентрацией его в насыщенном растворе.
Эффекты, возникающие в результате взаимодействия молекул растворителя с частицами растворённого вещества, называются сольватационными. По своей природе они являются частично электростатическими (физическая сольватация), частично химическими (химическая сольватация). В растворителях неполярных и малополярных, не содержащих ни подвижных протонов, ни донорных атомов, способных к образованию координационных связей, возможна только физическая сольватация, обусловленная ван-дер-ваальсовыми силами (углеводороды и их галогенопроизводные).В полярных растворителях, имеющих донорные атомы, содержащих или не содержащих подвижных протонов (кетоны, простые эфиры, вода спирты, карбоновые кислоты, амины) возможна как физическая, так и химическая сольватация. Для недиссоциированных молекул и ионов, недостаточно склонных к образованию координационных связей (катионы большинства щелочных и щелочно-земельных металлов, органические ионы, многие анионы) характерна физическая сольватация.
Химическая сольватация обусловлена образованием координационных связей между молекулами растворителя и частицами растворённого вещества. Она характерна для катионов d- и p- элементов. Такие катионы, например, образуют в воде аквакомплексы: [Cr(H2O)6]3+ , [Zn(H2O)4]2+, [Al(H2O)6]3+ и т.д.
Термодинамика процесса растворения
ΔGрастворения =ΔHрастворения – TΔSрастворения
Если имеет место сильное взаимодействие частиц растворяемого вещества и растворителя, то процесс растворения — экзотермический: ΔHрастворения < 0.
В этом случае изменение энтропии может быть как положительной (ΔSрастворения >0), так и отрицательной величиной (ΔSрастворения<0).
Часто процесс растворения сопровождается изменением агрегатного состояния. Тогда:
ΔHрастворения =ΔНфазового перехода + ΔHсольватации
ΔSрастворения =ΔSфазового перехода + ΔS сольватации
Для кристаллов энтальпия фазового перехода ΔНф.п. равна энергии разрушения кристаллической решётки и, следовательно, ΔНф.п. > 0 и ΔSф.п.> 0.
Сольватация — процесс экзотермический ΔНсольв.<0. Поэтому энтальпия процесса растворения может быть ΔНраств > 0 и < 0.Поскольку процесс растворения связан с взаимодействием растворяемого вещества и растворителя, растворение сопровождается изменением структуры и растворяемого вещества и растворителя.
Сольватация означает упорядочение системы (происходит уменьшение числа частиц, образование новых структур). Следовательно: ΔSсольв.<0. Однако по абсолютной величине изменение энтропии мало и поэтому при растворении ΔS.> 0.
По мере увеличения концентрации раствора усиливается интенсивность
взаимодействия между содержащими его частицами и усложняется его структура. При разбавлении, наоборот, строение раствора упрощается, и взаимодействие между частицами ослабевает. Введение растворённого вещества может привести как к уменьшению энтропии растворителя, так и к её увеличению. Структурирующие ионы для воды (уменьшающими её энтропию) — это малые по размеру и многозарядные ионы: Li+, Na+, Mg2+, Al3+,Fe3+,OH и др. Деструктурирующие ионы (увеличивающие её энтропию) — это большие однозарядные ионы: K+, Rb+, Cs+, Cl-, NO3-, ClO4- и др.. Структурирующие ионы — ионы с высокой напряжённостью электрического поля, которые могут поляризовать молекулы воды за пределами первой гидратной оболочки. Это приводит к повышению вязкости растворов. Деструктурирующие ионы не могут поляризовать воду за пределами первой гидратной оболочки, в результате вязкость этих растворов меньше, чем у чистой воды.
4.2. Способы выражения состава растворов
Массовая доля ω(в) растворённого вещества «В» — отношение массы растворённого вещества m(в) к сумме масс растворённого вещества и растворителя, чаще всего, воды (т.е. к массе раствора):
w(в) = 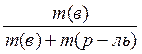
Массовая доля растворённого вещества выражается в долях или в %%( процентное содержание). Например, раствор с массовой долей серной кислоты ω(H2SO4)=0,2(т.е.20%) может быть обозначен как 20% - раствор серной кислоты.
В биологии и медицине также часто используют мг% и мкг%. Число мг% показывает, сколько мг растворённого вещества содержится в 100 г раствора. Число мкг% показывает, сколько мкг растворённого вещества содержится в 100 г раствора. Содержание растворённого вещества в мг% и мкг% применяют для характеристики очень разбавленных растворов. Например, массовая доля раствора глюкозы равна 0,001% или 1мг% или 1000мкг%.
Молярная концентрация с(в) растворённого вещества «В» — отношение количества вещества n(в) к объёму раствора:
c(в)= 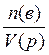 (моль/л).
(моль/л).
Раствор, в котором молярная концентрация растворённого вещества равна с(в) моль/л, характеризуется молярностью, численно равной значению с(в). Например, раствор с молярной концентрацией серной кислоты с(H2SO4)= 0,1моль/л может быть обозначен как 0,1М H2SO4 (децимолярный раствор серной кислоты в воде).
Нормальность (молярная концентрация химического эквивалента сeq (в) растворённого вещества «В» —это отношение эквивалентного количества вещества neq(в) к объёму раствора:
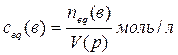
Раствор, в котором молярная концентрация эквивалента равна ceq(в) моль/л, характеризуется нормальностью, численно равной значению ceq(в).
Например, раствор с молярной концентрацией эквивалента серной кислоты ceq(H2SO4)= 1моль/л может быть обозначен как 1н H2SO4 (однонормальный раствор серной кислоты в воде). Нормальность раствора определяется эквивалентным количеством растворённого вещества и, следовательно, как и последнее, зависят от эквивалентного числа z(в), постоянного только для конкретной реакции, причём величина ceq(в) всегда в z(в) раз больше его молярной концентрации c(в):
сeq(в)=z(в)∙ с(в).
Молярная доля χрастворённого вещества ― отношение количества данного компонента «В» в молях, содержащегося в растворе, к общему количеству всех веществ, включая растворитель: χ = n(в) / [n(в) + n(р-ль)]
Молярная доля χ , как и массовая выражается в долях единицы, в процентах.
Например, χ(H2SO4) = 0,01 = 1%.
Моляльность раствора b –отношение количества данного растворённого вещества n(в) моль к массе растворителя (в кг):
b = n(в) / m(р-ль).
Например, b(H2SO4) = 0.1моль/кг.
Пример 1. В 450 г воды растворили 50 г CuSO4·5H2O. Вычислите массовую долю кристаллогидрата, безводной соли и ионов меди в растворе.
Решение: ω (CuSO4·5H2O) = 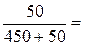 0,1 = 10%
0,1 = 10% 
ω (CuSO4) = 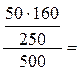 6,4% ω (Cu2+) =
6,4% ω (Cu2+) = 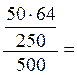 2,56%
2,56% 
Пример 2. Какую массу 5%-ного раствора MgSO4 можно приготовить из 300 г
MgSO4 ·7H2O?
Решение: ω(MgSO4) = m(MgSO4) / m (р-р) . m(р-р) = m(MgSO4) / 0,05.
m(MgSO4) = m( MgSO4 ·7H2O) /M (MgSO4 ·7H2O) ·M(MgSO4) =
=300 / 246 · 120 = 146,3(г)
m(р-р) = 146,3 / 0,05 = 2926,8(г)
Пример3. Сколько воды следует прибавить к 200мл 20% -ного раствора серной кислоты с плотностью 1,14г/мл, чтобы получить 5% -ный раствор?
Решение: m(р-ра H2SO4) = 200·1,14 = 228(г). m(H2SO4) = 228 · 0.2 = 45.6(г)
Массовая доля серной кислоты в конечном растворе:
0,05 =45,6 / [228 + m(H2O)].
Отсюда: [228 + m(H2O)] = 45,6/0,05 = 912(г)
m(H2O) = 912 – 228 = 684(г).
Пример 4. Смешали 300г 40% раствора азотной кислоты и 700г 10% раствора той же кислоты. Определите массовую долю полученного раствора.
Решение: m(р-ра HNO3) = 300 + 700 = 1000(г).
m(HNO3) = 300 · 0,4 + 700 · 0,1 = 190(г).
ω(нового раствора) = 190/1000 = 0,19=19%
Пример 5. Определите массу 30% раствора серной кислоты, которую следует добавить к 600 г 80% раствора той же кислоты для получения 60% раствора.
Решение: Пусть масса 30% раствора x. Тогда масса раствора после смешения:
m(р-р) = 600 + x
m(H2SO4) = 600 · 0,8 + x · 0,3. 0,6 = [600 · 0,8 + x · 0,3. 0,6] / (600 + x).
x = 400(г).
Пример 6. Как приготовить 500мл 1,5 М раствора серной кислоты из
96%-ного раствора с плотностью 1,84г/мл?
Решение: n(H2SO4) = 1,5 · 0,5 = 0,75(моль). m(H2SO4) = 98 0,75 = 73,5(г).
V(96% р-ра H2SO4) = 73,5/ 1,84 · 0,96 = 42(мл). Далее: необходимо долить воды, чтобы довести объём раствора до 500мл.
Пример 7. Вычислите нормальность и молярную концентрацию раствора H3PO4 с массовой долей кислоты 49% и плотностью 1,33г/мл. Фактор эквивалентности кислоты равен 1/3.
Решение: Масса 1л раствора: 1000 ·1,33 = 1330(г). m(H3PO4) =
= 1330 · 0,49 = 650(г). n(H3PO4) = 650 / 98 = 6,6(моль).
c(H3PO4) = 6,6 моль/л; c(1/3 H3PO4) = 6,6 / (1/3) = 19,8(моль экв),
т.е.19,8н H3PO4.
Пример 8. Рассчитайте нормальность и молярную концентрацию раствора гидроксида натрия, если 20мл этого раствора было нейтрализовано 10мл 0,1н H2SO4.
Решение: В соответствии с законом эквивалентов:
c(NaOH) ∙V(NaOH) = c(1/2H2SO4) ∙ V(H2SO4).
Отсюда c(NaOH) = c(1/2H2SO4) ∙ V(H2SO4) / V(NaOH) = 0,1 ∙10 / 20 =
= 0,05(моль/л).
Дата добавления: 2016-01-07; просмотров: 1083;
