Кислотно-основное равновесие. Современные представления о кислотно-основных равновесиях.
Кислотно-основное равновесие – относительное постоянство реакции внутренней среды организма, количественно характеризующееся или концентрацией водородных ионов (протонов), выраженной в молях на 1 л, или водородным показателем – отрицательным десятичным логарифмом этой концентрации – рН (powerhydrogen – сила водорода).
БИОХИМИЯ
1.Основные положения теории строения органических соединений А.М.Бутлерова. Изомерия как специфическое явление органической химии. атомы в молекулах соединены друг с другом согласно их валентности, порядок распределения связей в молекуле называется химическим строением;
изменение этой последовательности приводит к образованию нового вещества с новыми свойствами;
свойства веществ зависят не только от их состава, но и от «химического строения», то есть от порядка соединения атомов в молекулах и характера их взаимного влияния. Наиболее сильно влияют друг на друга атомы, непосредственно связанные между собой;
атомы в молекулах оказывают влияние друг на друга, и это влияние приводит к химическим изменениям поведения атома;
определить состав и строение химического вещества можно по продуктам химических превращений.
2. Классификационные признаки органических соединений6строение углеродного скелета и природа функциональной группы. Функциональная группа. Структурная формула. Структурные изомеры.
Органические соединения отличаются своей многочисленностью и разнообразием. Органические соединения классифицируют , учитывая два основных признака:
-строение углеродного скелета
-наличие и строение функцианальных групп.
Углеродные скелеты разделяют на ациклические(не содержащие циклов), циклическиеи гетероциклические.
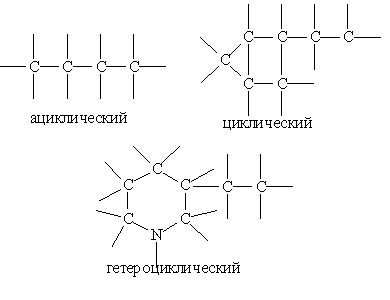
В гетероциклическом скелете в углеродный цикл включается одни или несколько атомов, отличных от углерода. Исторически сложилась традиция не рассматривать такие гетероатомы как функциональные группы, а считатьих частью углеродного скелета.
В самих углеродных скелетах нужно классифицировать отдельные атомы углерода по числу химически связанных с ними атомов углерода. Если данный атом углерода связан с одниматомом углерода, то его называют первичным, с двумя — вторичным, тремя — третичным и четырьмя — четвертичным.
Поскольку атомы углерода могут образовывать между собой не только одинарные, но и кратные (двойные и тройные) связи, то соединения, содержащие только одинарные связи углерод—углерод, называют насыщенными, соединения с кратными углерод¾ углеродными связями называют ненасыщенными.Соединения, в которых атомы углерода связаны только с атомами водорода, называют углеводородами.
1. Природа функциональной группыФункциональные группы, содержащие атом кислорода:
· гидроксильная –ОН,
· карбонильная >С=O
· карбоксильная –COOH
· алкоксильная –OR (типа –ОСН3) и др.
2Функциональные группы, содержащие атом азота:
· аминогруппа –NH2
· нитрогруппа –NO2
· нитрозогруппа –NO
· нитрильная группа или цианогруппа –CN
· гидразинная –NHNH2
· амидная –CONH2 и др.
3Функциональные группы, содержащие атом серы
· тиольная (сульфгидрильная, меркапто-) –SH
· сульфидная >S
· дисульфидная –S–S–
· сульфоксидная >S=O,
· сульфонная >SO2 и др.
4Функциональные группы, содержащие ненасыщенные углерод-углеродные связи:
· двойные и тройные связи (в том числе сопряжённые диеновые системы) –С=С–, –С≡С–
· ароматические фрагменты –С6H5 и др.
5Функциональные группы, содержащие прочие атомы:
· атомы металлов –Li
· атомы галогенов –Cl, и др.
Функциональная группа- атом или группа атомов, определяющие принадлежность соединения к определенному классу и ответственные за его химические свойства.
Дата добавления: 2015-12-26; просмотров: 1375;
