Образование 80S-комплекса инициации
II стадия ЭЛОНГАЦИИ ( включает 3 этапа)
1. связывание аминоацил-т-РНК (узнавание кодона)
2. образование пептидной связи
3. транслокация (перемещение рибосомы относительно м-РНК)
 мет мет арг
мет мет арг







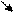 Р-уч. А-уч фактор элонгации ЕF1, доставляет аминоацил-т-РНК
Р-уч. А-уч фактор элонгации ЕF1, доставляет аминоацил-т-РНК 




АУГ-ЦГА-ГЦУ-м- РНК АУГ-ЦГА-ГЦУ
ГТФ ГДФ+Ф

Пептидилтрансфераза
катализирует образование пептидной связи арг-мет
 мет свободный мет арг
мет свободный мет арг







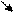 Р-уч. А-уч фактор транслокации
Р-уч. А-уч фактор транслокации 




АУГ-ЦГА-ГЦУ АУГ-ЦГА-ГЦУ
ГДФ+Ф ГТФ
1. Цикл начинается с введения аминоацил–т-РНК в пустой А-участок рибосомы. В зависимости от того, какой кодон м-РНК находится в А-участке выбирается определенная разновидность т-РНК. Комплиментарная аминоацил-т-РНК оставляется в А-участок фактором элонгации ЕF1. Когда аминоацил-т-РНК занимает правильное положение на рибосоме происходит гидролиз 1 молекулы ГТФ.
2. Т.о. имеется комплекс, в котором аминоацил-т-РНК занимает А-участок, а мет-т-РНК занимает Р-участок. Все готово к образованию пептидной связи. Эту реакцию катализирует пептидилтрансфераза, входящая в состав 60S-субъединицы.
Активированная мет-т-РНК с Р-участка переносится на амино-группу аминоацил-т-РНК в А-участок, образуя дипептид т-РНК.
После этого под действием фактора элонгации – транслоказы происходит сдвиг рибососмы по м-РНК на 3 нуклеотида, используя энергию ГТФ. В А-участке оказывается следующий кодон или триплет нуклеотидов, характерный для определенной АК. Дальнейшее удлинение цепи происходит путем многократного повторения этих процессов. Скорость элонгации довольно велика: пептид из 100 АК образуется ≈ за 2 мин. Остаток мет может отщепляться в ходе элонгации от цепи под действием специфической пептидгидролазы, а может и сохраниться в некоторых белках.
III стадия ТЕРМИНАЦИЯ. Удлинение пептидной цепи продолжается до тех пор пока А-участок не окажется занятым одним из стоп-кодонов УАА, УАГ, УГА. В этом случае при участии факторов терминации происходит гидролитическое взаимодействие между пептидом и последней т-РНК, а в цитоплазму высвобождается готовый белок.
В результате трансляции не всегда образуется функционально активный белок. Во многих случаях необходимы дополнительные пострансляционные изменения.
Принципиальная схема биосинтеза белка (по А.С. Спирину).
ЛЕКЦИЯ 6
ФЕРМЕНТЫ
Ферменты, или энзимы – это белковой природы, образующиеся и функционирующие во всех живых организмах. Слово фермент происходит от лат. fermentum – закваска, другое название ферментов – энзимы от греч. en zyme – в дрожжах.
Впервые ферментативные процессы были открыты в бродильном производстве. Современная ферментология или энзимология– это наука о ферментах, их структурной организации. Она решает задачи изучения механизмов действия ферментов, путей регуляции ферментной активности. Такой интерес к биокатализаторам не случаен. Ферменты – это важнейшие компоненты клетки, без них невозможны синтез, распад и взаимопревращения в живых организмах. Через ферментный аппарат и регуляцию его активности происходит и регуляция скорости метаболических реакций. Изучение важно для биологии, медицины, фармации, многих областей народного хозяйства. Установлено, что многие заболевания человека связаны с нарушением деятельности ферментов, целый ряд ферментов является лекарственными препаратами.
Общие и специфические свойства ферментов.
Являясь катализаторами, то есть веществами, ускоряющими реакции, ферменты имеют ряд общих свойств с химическими небиологическими катализаторами.
1. Ферменты и входят в состав конечных Р и выходят из реакции в неизменном виде, они не расходуются в процессе катализа.
2. Ферменты не могут возбудить реакций, противоречащим законам термодинамики, они ускоряют только те реакции, которые могут протекать и без них.
3. Ферменты, как правило, не смещают положения равновесия реакции, а лишь ускоряют его достижение.
Вместе с тем ферменты обладают и специфическими свойствами:
1. По химическому строению ферменты являются белками (>99,9).
2. Эффективность ферментов на несколько порядков выше, чем небиологических катализаторов.
Например: H2O2 ® H2O + ½ O2
а) если реакция протекает без катализатора, то Еа = 75,7 кдж/моль, пузырьки О2 почти не видны;
б) если прибавить катализатор небиологический то Еа = 54,1 кдж/моль, пузырьки отчетливо видны;
в) если прибавить биологический катализатор каталазу, то Еа = 18 кдж/моль, раствор просто «кипит».
3. Высокая специфичность – каждый фермент катализирует одну единственную реакцию или одну группу реакций, тогда как неорганические катализаторы действуют при различных типах реакций.
4. Ферменты катализируют реакции в «мягких» условиях: при нормальном Р, рН = 7,0. Для неорганических катализаторов присуща необходимость экстремальных значений рН, нагревание до очень высоких температур.
Химическая природа и строение ферментов.
Важным доказательством белковой природы ферментов явились работы Пастера (инактивация ферментов брожения при кипячении), Павлова (доказал белковую природу пепсина – фермента желудочного сока) и т.д.
1) важный признак белковой природы ферментов – их большая Mr. Например, у ДГ Mr = 4 ´106; 4,8 ´105 и т.д.
2) растворы ферментов имеют коллоидный характер – они не проходят через полунепроницаемую мембрану, осаждаются из растворов теми же реактивами, что и белки;
3) ферменты денатурируют и теряют свою активность под влиянием высокой температуры, УЗ, сильных щелочей и других факторов;
4) ферменты, как и белки, обладают амфотерными свойствами, электрофоретической подвижностью и рI.
5) как и белки, ферменты обладают высокой специфичностью;
6) наконец, прямым доказательством белковой природы ферментов явился искусственный синтез ферментов (рибонуклеаза, лизоцим), которые не отличаются по свойствам и биологической активности от природных аналогов.
| Ферменты | |

| |
| простые белки | сложные белки |
| состоят только из ППЦ | состоят из ППЦ + небелковый компонент |
| (гидролитические ферменты – пепсин, трипсин, уреаза и др.) или ферменты–протеины | (ацетил КоА, лактат ДГ и т.д.) или ферменты–протеиды |
В ферментах-протеидах белковая часть называется апоферментом, а небелковая – простетической группой. Общее название сложных ферментов – холофермент.
Если простетическая группа слабо связана с белковой частью и легко диссоциирует, она называется коферментом. Кофермент может соединяться с разными белками, и именно белковая часть определяет специфичность действия сложных ферментов. Вместе с тем, без кофермента сложный фермент не может функционировать, так как кофермент, как правило, непосредственно контактирует с субстратом (S) и служит в качестве переносчика ē, атомов или группы атомов.
Кофакторы, или коферменты это:
1) ионы Me – Mg2+, Ca2+, Cu2+, Mn2+ b lh/$
2) витамины и их фосфорные эфиры – витамин Н (биотин)(в составе коферментов карбоксилирования), липоевая, фолиевая кислоты, В1 и др.;
3) мононуклеотиды ФМН, АТФ, ГТФ и т.д.;
4) большая часть коферментов – это динуклеотиды НАД, НАДФ, HS-KoA и др.
При гиповитаминозах и авитаминозах недостаток витаминов ослабляет биосинтез многих ферментов и вызывает гипокоферментоз. Коферменты выполняют также важную роль в стабилизации и охране апоферментов. Последние без коферментов скорее разрушаются протеолитическими ферментами.
Таким образом, сами по себе ни коферменты, ни апоферменты каталитической активностью не обладают, а только в комплексе друг с другом.
Молекулы S-в чаще всего имеют небольшие размеры по сравнению с молекулами ферментов, поэтому при образовании Е-S-го комплекса в контакт с S вступает ограниченная часть аминокислот ППЦ, которая называется активным центром (АЦФ). У Е-протеидов в состав АЦФ входят также и простетические группы.
Таким образом, активный центр фермента – это уникальная комбинация аминокислотных остатков, обеспечивающих непосредственное взаимодействие Е и S и прямое участие в акте катализа.
| АЦФ | |

| |
| связывающий центр | каталитический центр |
| участок, где происходит связывание S и Е – это контактная или «якорная» площадка | участок, где происходит превращение S после его связывания |
При сближении Е и S и образовании ЕS-комплекса нуклеофильные и электрофильные группы АЦФ, отдавая или принимая ē-ны, тем самым как бы «расшатывают» электронную структуру S, активируя его и ускоряя химическую реакцию. Есть ферменты, имеющие несколько АЦФ – уреаза–3; алкоголь ДГ–4; ацетилхолингетераза – 25-30 АЦФ у разных животных.
Аллостерические центры ферментов.
Кроме АЦФ, у ферментов имеются и аллостерические ( греч. allos – другой) или инопространственные центры. Это место воздействия на ферменты разных регуляторных факторов. Взаимосвязь между АЦФ и АЛЦФ называется аллостерическими взаимодействиями. Важная особенность АЛЦФ – их более высокая по сравнению с АЦФ чувствительность к различным воздействиям.
Например, при повышении температуры и применении рН раньше затормаживается функция АЛЦФ. В частности, при повышении температуры аллостерический центр гексокиназы теряет чувствительность к регуляторному воздействию инсулина и глюкокортикоидов, а функциональная активность ферментов сохраняется и продолжает фосфорилировать глюкозу за счет АТФ.
Регуляторное воздействие на аллостерический центр оказывают: различные метаболиты ферментативных реакций, гормоны и продукты их обмена, медиаторы НС и т.д. Они называются эффекторами или модификаторами. Их молекулы не сходны с молекулами S-в.
Связываясь с аллостерическим центром, эффекторы изменяют ТС и ЧС ферментов, тем самым изменяют конфигурацию АЦФ, что приводит к повышению (активированию) или понижению (ингибированию) ферментативной активности.
Изоферменты – это молекулярные формы ферментов, возникающие вследствие генетических различий в ПС ферментного белка. Это группа ферментов, которые присутствуют внутри одного вида (ЛДГ) или внутри одной клетки (аминотрансферазы), имеют одинаковый механизм действия, но отличаются по некоторым физико-химическим свойствам: электрофоретической подвижности, иммунобиологическим реакциям. Например, 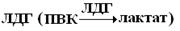 существует в виде пяти изоферментов. Хотя они катализируют одну и ту же реакцию, отличаются по своей Кт. У них одинаковая Mr (134.000) и по 4 ППЦ с Mr 33.500. Пять изоферментов соответствую пяти различным комбинациям двух разных типов ППЦ, названных M – (muscle) и H– (heart) цепями. Изофермент М4 – находится в мышечной ткани, содержит идентичные 4М-цепи; Н4 – находится в сердце, содержит идентичные 4Н-цепи. Остальные три изофермента – это различные сочетания М3Н; М2Н2; МН3. Два типа цепей – М и Н, кодируются двумя различными генами, сочетание ППЦ находится под генетическим контролем. Наличие изоферментов и изменение их соотношения в организме – один из способов регуляции ферментов.
существует в виде пяти изоферментов. Хотя они катализируют одну и ту же реакцию, отличаются по своей Кт. У них одинаковая Mr (134.000) и по 4 ППЦ с Mr 33.500. Пять изоферментов соответствую пяти различным комбинациям двух разных типов ППЦ, названных M – (muscle) и H– (heart) цепями. Изофермент М4 – находится в мышечной ткани, содержит идентичные 4М-цепи; Н4 – находится в сердце, содержит идентичные 4Н-цепи. Остальные три изофермента – это различные сочетания М3Н; М2Н2; МН3. Два типа цепей – М и Н, кодируются двумя различными генами, сочетание ППЦ находится под генетическим контролем. Наличие изоферментов и изменение их соотношения в организме – один из способов регуляции ферментов.
Дата добавления: 2015-12-22; просмотров: 806;
