Методи формування наноелектронних структур. 2 страница
Технология формирования пленок полупроводников электрохимическим осаждением зародилась более чем через столетие после установления основных закономерностей электрохимического осаждения металлов М. Фарадеем. Сегодня полупроводниковые соединения (CdS, CdSe, CdTe, ZnSe) осаждают по трехступенчатой схеме включающей: 1) осаждение металла из водного раствора; 2) химическое или электрохимическое окисление осажденного металла до образования оксида (или гидроксида) этого металла; 3) замещение кислорода (гидроксильной группы) анионом металлоида (S, Se, Те). Электрохимическое осаждение кремния и германия осуществляют главным образом из неводных растворов или расплавов (для кремния при температуре выше 800 °С) из-за высокого отрицательного потенциала осаждения Si и чрезвычайно высокой скорости высвобождения водорода на поверхности Ge. Широкого практического распространения эти методы не получили. Формирование периодически расположенных наноструктур - наноточек, наношнуров и нанотрубок, осуществляют селективным электрохимическим осаждением материала либо с использованием анизотропии свойств и существенной неоднородности напряженности электрического поля у ступенек на поверхности проводящих подложек, либо через сформированный на поверхности проводящей подложки трафарет (template)из материала, не проводящего электрический ток. При использовании подложек со ступенчатым рельефом поверхности (рис. 2.7) внутренние уголки ступенек действуют как концентраторы силовых линий электрического поля. За счет этого обеспечивается максимальный приток ионов к ним из электролита. С другой стороны, конденсация и нейтрализация ионов в этих уголках энергетически более выгодна, чем на плоской поверхности. Таким способом создают наношнуры, лежащие на поверхности подложки и повторяющие геометрию ступенек на ней.
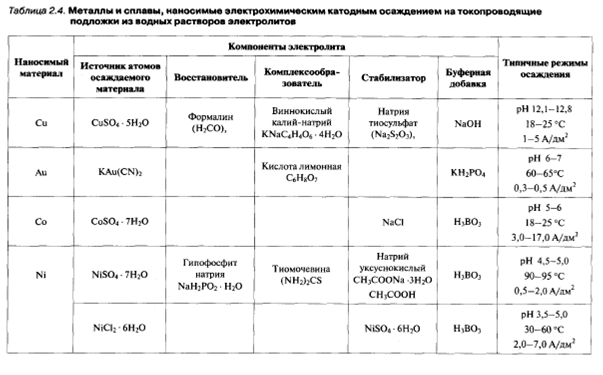
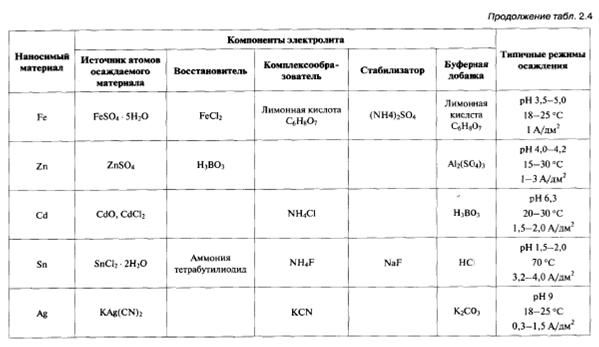
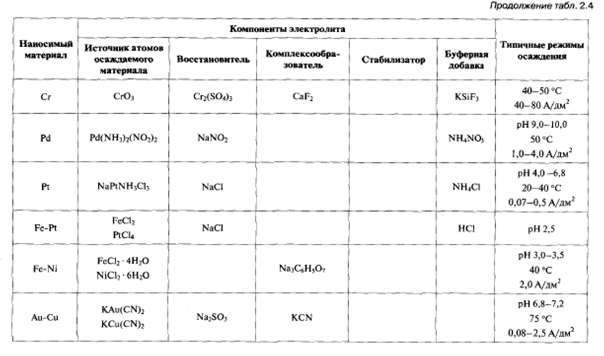
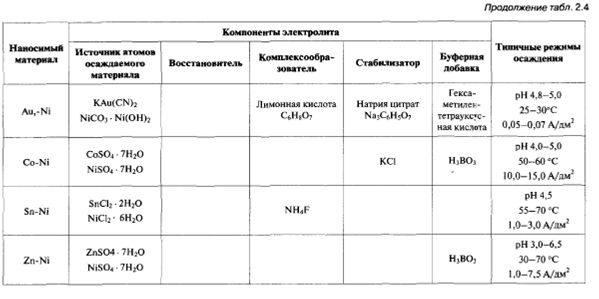
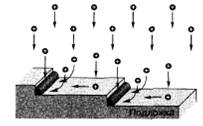
Рис. 2. 7. Формирование наноструктур селективным электрохимическим осаждением материалов с использованием ступенчатой поверхности подложки
При трафаретном формировании наноструктур электрохимическое осаждение материала осуществляют на проводящий затравочный слой, находящийся на дне отверстий в изолирующей маске (рис. 2.8). В качестве маски используют пористый анодный оксид алюминия, пористый кремний, а также поликарбонатные мембраны. Осаждение материала в глубокие наноразмерные поры таких масок характеризуется очень высокой точностью воспроизведения геометрии отверстий в маске и позволяет формировать упорядоченные массивы наноточек, наношнуров и нанотрубок, расположенных перпендикулярно плоскости подложки.
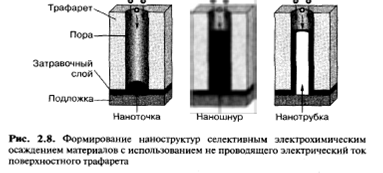

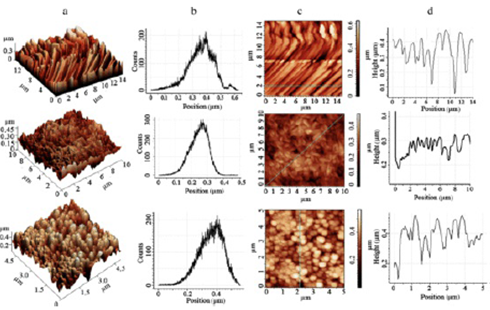
Fig. 7AFM images of ZnO arrays from Table 1 deposited at f = 2 Hz and: (a), (b): at t = 70 °C, Dc = 0.4; (c) at t = 85 °C, Dc = 0,4; (d) at t = 70 °C, Dc = 0.8; (e) at t = 77 → 70 °C, Dc = 0.4. 
Главными достоинствами метода электрохимического осаждения материалов являются простота его реализации, возможность осаждения толстых (более 1 мкм) покрытий на поверхности различной формы, контроль и изменение свойств формируемых покрытий, высокая производительность и низкая стоимость используемого оборудования. К недостаткам следует отнести высокую степень зависимости свойств осаждаемых материалов от режимов осаждения и состава электролита, а также ограниченный набор осаждаемых этим методом материалов.
Электрохимическое оксидирование металлов и полупроводников (анодирование) (oxidation, anodization) - в технологическом аспекте это процесс создания оксидной пленки на поверхности материала в результате окислительно-восстановительных реакций. По условиям проведения этого процесса различают термическое, химическое, электрохимическое и плазменное оксидирование. Все они широко используются в технологии изготовления полупроводниковых приборов и интегральных микросхем. Электрохимическое оксидирование (electrochemical oxidation)или, как его еще называют, электрохимическое анодирование ( electrochemical anodization)- это процесс получения оксидных пленок на поверхности металлов и полупроводников при их анодной поляризации (размещении на аноде) в кислородсодержащей жидкой среде с ионной проводимостью (электролите). Особый интерес именно к этому технологическому методу связан с предоставляемой им возможностью формировать структуры с естественным наноструктурированием, что неосуществимо при использовании других методов оксидирования. Технологическая установка для анодирования имеет те же основные элементы, что и рассмотренная в предыдущем разделе электролитическая ячейка для электрохимического осаждения материалов (см. рис. 2.6) - анод, катод и электрод сравнения, помещенные в жидкий электролит. Принципиальное отличие состоит лишь в том, что технологически полезные процессы в данном случае происходят на аноде. При поrружении рабочих электродов - анода и катода, в электролит у их поверхности устанавливается динамическое равновесие, при котором состав фаз, образующихся на электродах, остается неизменным. В этих условиях на каждом из них устанавливается определенный равновесный электрический потенциал, величина которого зависит от свойств материала электрода и состава электролита. При приложении к рабочим электродам напряжения в цепи анод-электролит-катод начинает протекать ток, который изменяет потенциалы этих электродов. (Равновесный потенциал - это потенциал, возникающий на электроде, погруженном в раствор электролита, вследствие установления динамического фазового равновесия на границе электрод/электролит). Данное явление называется поляризацией электродов и характеризуется потенциалом поляризованного электрода. Разность между потенциалом поляризованного электрода и его равновесным потенциалом называется перенапряжением. Для описания процесса анодирования обычно используют метод потенциодинамической поляризации анода (potential dynamics anode polarization), при котором регистрируется зависимость анодного тока Ia от потенциала поляризованного анода Va. Ее записывают с учетом электрода сравнения при скорости увеличения напряжения на аноде, достаточно малой в сравнении со скоростью установления равновесия в протекающих на нем процессах. Участок 1 поляризационной кривой отражает активное состояние анода. С ростом перенапряжения на аноде ток экспоненциально возрастает, при этом происходит растворение материала анода, которое поддерживается ионизацией атомов анода. Далее, по мере увеличения перенапряжения на поверхности анода, формируется и утолщается пленка из продуктов реакций, которые не успевают растворяться и переходить в объем электролита. Пик поляризационной кривой соответствует максимальной скорости окисления анода, сбалансированной скоростью растворения продуктов окисления. Максимальному току соответствует так называемый Фладе- потенциал (VF), по превышении которого скорость анодного окисления становится больше скорости растворения продуктов реакции. Участок 2 соответствует переходу анода из активного состояния в пассивное. Растущая на нем оксидная пленка все больше препятствует проникновению ионов электролита в анод, что приводит к уменьшению анодного тока, несмотря на возрастание прилагаемого напряжения. Участок 3 характеризует пассивное состояние анода, при котором скорость окисления анода, значительно упавшая из-за образования на аноде слабопроводящей электрический ток оксидной пленки, снова становится равной скорости ее растворения. Последняя не зависит от падения потенциала на границе анод/электролит, а является функцией концентрации в электролите частиц, способствующих растворению продуктов окисления анода, скорости их подвода к поверхности анода и скорости отвода от нее продуктов растворения. Она определяет остаточный ток Ir, называемый также коррозионным током.
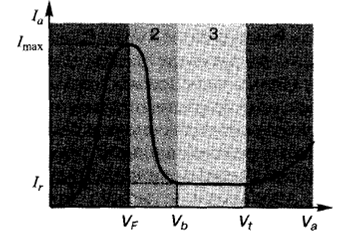
Рис. 2.9. Типичная анодная поляризационная кривая
Пассивное состояние анода сохраняется в диапазоне перенапряжений от Vb до Vt,. Участок 4 демонстрирует возрастание анодного тока, связанное с так называемой транспассивацией анода. Рост тока на этом участке связан со следующими возможными процессами: - увеличение степени ионизации атомов анода и образование ими легко растворимых соединений; - электрический пробой образовавшейся оксидной пленки и ускоренное анодное окисление в местах пробоя; - возрастание электронной проводимости пленки.
Одним из основных параметров процесса анодирования является скорость роста анодной оксидной пленки. Она зависит как от свойств материала анода и состава электролита, так и от электрического режима анодной обработки, характеризуемого анодным током и анодным напряжением. Анодирование можно проводить, поддерживая постоянным анодный ток - это гальваностатический режим (galvanostatic mode), или напряжение на аноде - потенциостатический режим (controlled potential mode), а также комбинируя эти два режима. В любом случае, если скорость растворения образующейся оксидной пленки мала, то ее толщина согласно закону Фарадея пропорциональна количеству прошедшего через анод электричества. Для гальваностатического анодирования плотность тока обычно задают по значению в середине второго участка анодной поляризационной кривой (см. рис. 2.9), экспериментально полученной для данной системы электрод-электролит. Обычно она составляет 0,3-3 мА/см2 и поддерживается постоянной с помощью внешних элементов питающей анод электрической цепи. Скорость роста анодной пленки линейно зависит от плотности анодного тока. Толщина же пленки пропорциональна продолжительности анодирования. С ростом толщины пленки поддержание постоянным анодного тока требует соответствующего повышения питающего напряжения. На постоянном токе эта возможность ограничивается потенциалом начала транспассивации (Vt на рис. 2.9), при превышении которого происходит электрический пробой растущей оксидной пленки и другие необратимые изменения ее свойств, вследствие воздействия на нее сильного электрического поля. Напряжение для потенциостатического анодирования - напряжение формовки- выбирают на 15-30% меньше напряжения начала транспассивации Vi (см. рис. 2.9). В начальный момент подачи на анод напряжения анодный ток максимален и ограничивается лишь сопротивлением внешних элементов питающей цепи. Он экспоненциально уменьшается по мере увеличения времени анодирования и стабилизируется на уровне остаточного тока (Ir на рис. 2.9). Аналогично, изменяется и скорость роста оксидной анодной пленки. Анодирование в комбинированном режиме обычно начинают с гальваностатических условий, повышая анодное напряжение до величины на 15-30% меньше напряжения пробоя пленки. Затем это напряжение поддерживают постоянным, переходя, таким образом, к потенциостатическому анодированию - до тех пор, пока анодный ток не уменьшится до остаточного тока. Такой режим позволяет получать пленки более совершенной структуры и с улучшенными диэлектрическими свойствами. Наряду с электрическим режимом анодирования, важным фактором, определяющим и кинетику роста анодной оксидной пленки, и ее свойства, является состав электролита. Выделяют две основные группы электролитов оксидирования. В первую группу входят слабые электролиты, такие как растворы борной и разбавленной лимонной кислот, бикарбонатов, нитратов и фосфатов. В них образуются плотные оксидные пленки так называемого барьерного типа. Толщина этих пленок, как правило, не превышает 500 нм. Ко второй группе относят электролиты, слабо растворяющие оксид. Их готовят на основе серной, фосфорной, хромовой, щавелевой, сульфосалициловой и других сильных кислот, а также из сульфатов и концентрированных растворов лимонной и винной кислот. Формируемые в этих электролитах оксидные пленки имеют двухслойную структуру. Тонкий, прилегающий к материалу анода слой образован плотным оксидом барьерного типа, а наружный более толстый слой имеет пористую или трубчатую структуру. Его толщина может достигать сотен микрометров. Формирование анодных оксидных пленок имеет свои специфические особенности для металлов и для полупроводников. Электрохимическое окисление металлов происходит за счет дрейфа ионов металла и кислорода через растущий оксидный слой к внутренней и внешней границам оксида и образования оксидов на этих границах. Детальное количественное описание этих процессов осложняется наличием границ металл/оксид и оксид/электролит, гетерогенным строением оксидной пленки, а также возможностью протекания побочных реакций, связанных с разрядом иона кислорода и растворением образовавшейся оксидной пленки. Тем не менее, кинетические закономерности образования анодных оксидных пленок и их свойства для многих металлов достаточно хорошо изучены экспериментально и рассмотрены в ряде обзорных работ. Методика и теория процесса электрохимического окисления наиболее детально разработаны для А1 и тугоплавких металлов (в первую очередь Ti, Та, NЬ, а также Zr, Hf, W). На этих металлах можно получить достаточно толстые (от 300 нм до 500 нм) плотные оксидные пленки барьерного типа, обладающие хорошими антикоррозионными свойствами и высокими электрическими характеристиками. Близкие по свойствам формируемых оксидов дает анодирование Ве, Mg, Sn, U. С практической точки зрения одной из основных целей электрохимического оксидирования является получение анодных оксидных пленок, обладающих высокими диэлектрическими свойствами, так как в основном они используются в качестве разделительных изолирующих элементов, элементов конденсаторных и туннельных структур в интегральных микросхемах и дискретных электронных приборах. Для оксидов, являющихся хорошими электронными проводниками (оксиды V, Cr, Mn), задача получения их методом анодного окисления осложняется тем, что достаточная напряженность поля достигается только в слоях толщиной в несколько нанометров. Дальнейший рост оксидной пленки прекращается, на аноде начинается выделение кислорода или растворение металла. При анодировании металлов переходных групп следует иметь в виду, что важнейшей особенностью их взаимодействия с кислородом является переменная валентность, связанная с существованием у них незаполненной d-оболочки. Вследствие этого при анодном окислении этих металлов возможно образование слоев оксидов различного состава. Как правило, они в основном состоят из оксида высшей валентности (например Та2О5 , Nb2О5 , ТiО2), но на границе с металлом существуют оксиды и низшей валентности (для Та и NЬ степень окисления может быть равна 3, 4 и 5, а для Ti - 2, 3 и 4). Состав и толщина таких слоев определяются условиями оксидирования, что позволяет в некоторых случаях формировать слои низших оксидов переходных металлов толщиной до нескольких десятков нм.
Процессы, протекающие при оксидировании полупроводников, во многом схожи с теми, что имеют место для металлов. Основное отличие ‒ атомы полупроводника слабее ионизируются и менее подвижны в растущем слое оксида, чем атомы металлов. Вследствие этого образование новых порций оксидов происходит преимущественно на границе полупроводник/оксид, за счет дрейфа к ней ионов кислорода. Основной целью оксидирования полупроводников является получение тонких (не более 0,5 мкм) диэлектрических слоев с удельным сопротивлением 1012-1016 Ом·см и малым встроенным зарядом. При выборе условий анодирования полупроводников особенно важен тип электролита, который должен удовлетворять следующим требованиям: содержать малые количества воды (полностью ее исключать не нужно, так как она является источником кислорода для образования оксидов); иметь достаточно высокую электропроводность и диэлектрическую проницаемость; плохо растворять продукты окисления анода; оставаться стабильным при прохождении электрического тока. Этим требованиям в определенной степени удовлетворяют электролиты, приготовленные на основе органических растворителей, таких как этиленгликоль, изопропиловый спирт, диметилформамид, диметилсульфоксид, тетрагидрофурфуриловый спирт и другие. Они содержат электропроводящие добавки слабых кислот (борная, пирофосфорная, уксусная, винная, сульфосалициловая и др.) или оснований (гидроксид аммония, гуанидин), их солей, окислителей (нитраты, феррицианид). Нежелательно присутствие в электролите ионов металлов, особенно щелочных, которые способны внедряться в оксид и ухудшать его электрофизические свойства. Анодное окисление кремния обычно осуществляют в электролитах на основе этиленгликоля и N-метилацетамида при плотностях тока 3-15 мА/см2. Анодное окисление германия обычно сопровождается образованием нескольких оксидов - GeO и GeO2, толщиной до десятков нм. Аналогичные ограничения, а именно композиционный состав и малые толщины, присущи анодным оксидным пленкам и на полупроводниковых соединениях, вследствие чего такие пленки не находят практического применения. Анодные же оксидные пленки металлов, наряду с традиционными приложениями в микроэлектронике для тонкопленочных конденсаторов, межуровневой и межкомпонентной изоляции, защиты и пассивации поверхности элементов интегральных микросхем, получают все больнее распространение в технологии изготовления наноэлектронных приборов и схем. Так, матрицы из пористого анодного оксида алюминия А12О3 используются в качестве трафарета при изготовлении эмиссионных нанокатодов, массивов наноточек из золота и других металлов. Нанопористые и нанотрубчатые структуры из TiО2, WOx, являющихся щирокозонными полупроводниками, активно осваиваются для фотоэлектрических и фотокаталитических применений. Главными достоинствами метода электрохимического оксидирования являются: простота, экономичность, низкая температура (чаще всего комнатная), пригодность для обработки изделий любой сложности (формы), равномерность формируемых оксидных пленок по толщине на изделиях большой площади. К недостаткам следует отнести необходимость применения токсичных, экологически небезопасных электролитов, сопутствующую им коррозию технологического оборудования, что зачастую требует существенных затрат на противокоррозионную защиту и на утилизацию использованных химических реагентов.
МЕТОДЫ, ОСНОВАННЫЕ НА ИСПОЛЬЗОВАНИИ СКАНИРУЮЩИХ ЗОНДОВ Методы создания наноразмерных структур с применением сканирующих точечных зондов берут свое начало от сканирующей туннельной микроскопии (scanning tunneling microscopy, SТМ) и атомной силовой микроскопии (atomicforce microscopy, АFМ). Они сочетают возможности получения наноструктур с проведением их исследования с атомным разрешением. Физическую основу сканирующей туннельной микроскопии составляют явления, определяемые туннелированием электронов в зазоре между атомарно острым зондом и поверхностью анализируемого образца. Рассмотрим ситуацию, когда к поверхности проводящего электричество образца подведен металлический зонд, на острие которого находится один атом. При расстоянии между ними, сравнимом с межатомным (0,1-0,3 нм), волновые функции электронов, принадлежащих атому зонда и ближайших к нему атомов на поверхности образца, будут перекрываться, обеспечивая таким образом благоприятные условия для туннелирования электронов через этот зазор. Туннельный ток через зазор пропорционален вероятности туннелирования. Он экспоненциально зависит от ширины зазора, а следовательно, очень чувствителен к структурным неоднородностям поверхности образца. Поэтому, перемещая зонд вдоль поверхности и контролируя протекающий по нему туннельный ток, можно анализировать топологию поверхности с атомным разрешением.
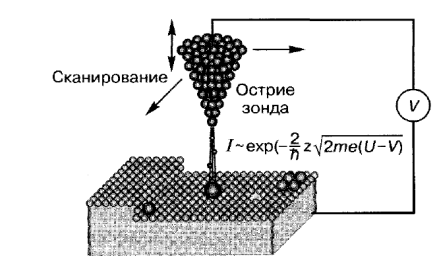
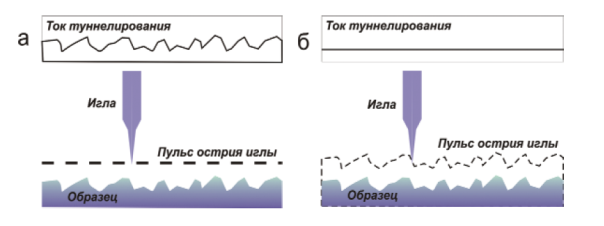
Рис. 2.11.Принцип работы сканирующего туннельного микроскопа
В сканирующем туннельном микроскопе эта идея реализуется следующим образом (рис. 2.11). Металлический зонд, обычно изготавливаемый из вольфрама, закрепляют в держателе, пространственное положение которого регулируется тремя пьезоэлементами с помощью подаваемого на них управляющего напряжения. Зонд подводят к образцу на расстояние, обеспечивающее протекание туннельного тока, и сканируют вдоль поверхности пьезоэлементами, задающими положение зонда в плоскости образца ху. Изменение туннельного тока при неизменной высоте расположения зонда и постоянном приложенном напряжении отражает изменение топологии поверхности. Этот режим называют режимом с постоянной высотой зонда (constant height mode). Возможно также поддерживать постоянным туннельный ток, меняя с помощью системы обратной связи приложенное напряжение V. Этот режим называют режимом с постоянным током (constant current mode). Зависимость V(x, у) отражает атомный рельеф поверхности. Локальное изменение работы выхода, характерное для образцов, состоящих из различных по своим свойствам атомов, учитывается с помощью дополнительной небольшой модуляции ширины зазора между зондом и анализируемой поверхностью. Таким образом удается не только «увидеть» расположение атомов на поверхности, но и различить области с разным химическим составом. Вертикальное разрешение достигает 0,01-0,05 нм, а горизонтальное - 0,3 нм. Размер анализируемой поверхности обычно составляет сотни микрометров. Ограничением метода является требование высокой электропроводности исследуемого материала, что необходимо для протекания достаточного для регистрации туннельного тока.
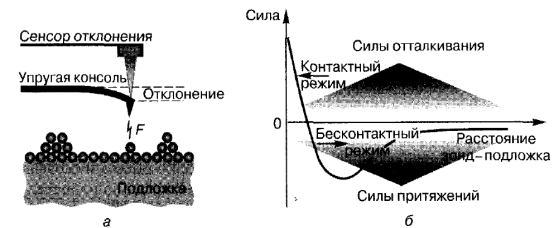
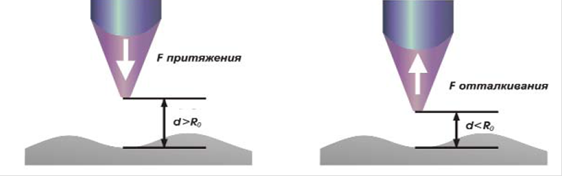 Рис. 2.12.Относительное расположение зонда и подложки (а) и соотношение сил, действующих между зондом и подложкой в атомном силовом микроскопе (б)
Рис. 2.12.Относительное расположение зонда и подложки (а) и соотношение сил, действующих между зондом и подложкой в атомном силовом микроскопе (б)
В атомной силовой микроскопии для анализа поверхности вместо туннельного тока регистрируется сила взаимодействия между зондом и подложкой (рис. 2.12). Для определения этой силы острый зонд закрепляют на упругой консоли. Отклонение консоли пропорционально действующей на нее силе. Это отклонение регистрируется с высокой точностью оптическими (например, посредством лазерной интерференции) или электронными (например, зондом сканирующего туннельного микроскопа) методами. При сканировании зонда вдоль анализируемой поверхности сигнал об отклонении консоли дает информацию о распределении атомных и молекулярных сил по поверхности образца, а следовательно, и о расположении и природе поверхностных атомов. Атомная силовая микроскопия, в отличие от сканирующей туннельной микроскопии, может быть использована для анализа поверхности как проводящих, так и диэлектрических материалов. Обычно атомную силовую микроскопию проводят в контактном (зонд контактирует с анализируемой поверхностью) или бесконтактном режиме. В контактном режиме на зонд действует сила отталкивания. Эта сила уравновешивается пьезоэлектрическим элементом позиционирования, толкающим зонд к поверхности. Бесконтактный режим с зазором 5-15 нм используется, когда имеется опасность того, что зонд может изменить (повредить) поверхность. В контактном режиме сканирование выполняется непрерывно или же путем «обстукивания» образца. Контролируя возмущение у поверхности образца, можно осуществлять управляемую локальную модификацию поверхности с атомным разрешением. Этому способствуют экстремальные условия, которые можно создать вблизи острия зонда, а именно - электрические поля и токи. Таким образом, использование сканирующих зондов позволяет реализовать локальное окисление поверхности, осаждение на нее различных материалов, манипулирование отдельными атомами (атомная инженерия), низкоэнергетическую электронно-лучевую литографию. Преимущества зондовых методов модификации материалов обусловлены не только высокой локальностью воздействия на поверхность, но и возможностью непосредственной визуализации результата этого воздействия и даже проведения локальных электрических измерений с использованием того же самого зонда.
Атомная инженерия При параллельных процессах переноса атомов атомы или молекулы перемещают вдоль поверхности, а при перпендикулярных их переносят с поверхности на острие зонда и обратно. В обоих случаях конечной целью является перестройка поверхности на атомном уровне. Такую перестройку можно рассматривать как серию последовательных действий, приводящих к селективному разрыву химических связей между атомами и к последующему образованию новых связей. С другой точки зрения, это эквивалентно движению атома по некоторой потенциальной поверхности от начального состояния к конечному.
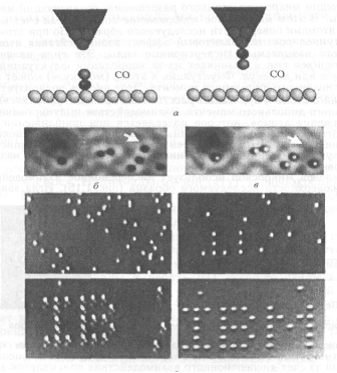

Зондовые методы формирования наноструктур. Возможность создания высоких напряженностей электрического поля у острия зонда (до 1010 В/м) и высоких плотностей тока между зондом и подложкой (до 107 А/см2) позволяет осуществлять локальное анодное окисление полупроводников и металлов, а также локально осаждать различные материалы. Локальное окисление металлов и полупроводников Сканирующие зонды позволяют проводить локальное окисление материала подложки. Окисление осуществляется на воздухе с использованием изготовленного из проводящего материала зонда сканирующего туннельного микроскопа или атомного силового микроскопа. Процесс во многом аналогичен обычному электрохимическому анодному окислению. Примеры локального окисления кремния и пленки металла схематически показаны на рис. 2.16. В режиме анодного окисления на зонд подается отрицательное относительно подложки смещение. Влага из окружающей среды служит электролитом. Вследствие капиллярного эффекта и под действием сильного электрического поля вода конденсируется на острие зонда и обволакивает его.
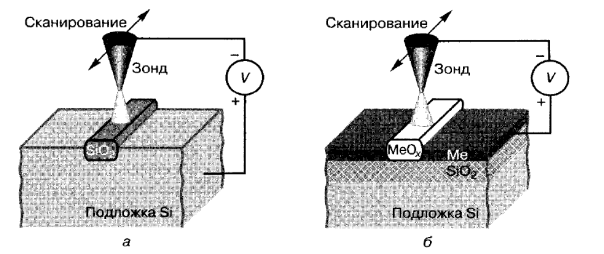
Рис. 2.16.Локальное зондовое окисление кремния (а) и пленки металла (6)
Там молекулы воды диссоциируют (Н2О ↔ Н+ + ОН-) и находятся в равновесии с продуктами своей диссоциации Н+ и ОН-. Электрическое поле разделяет эти ионы, направляя ОН--группы к подложке, где они вступают в химическую реакцию с материалом подложки, неизбежно приводя к его окислению. Толщина образующегося при этом оксидного слоя зависит от напряженности электрического поля (которое понижает потенциальный барьер для диффузии отрицательных ионов через растущий оксид) и от скорости сканирования. Индуцированная высокой плотностью тока атомная перестройка поверхности и локальный разогрев также могут влиять на процесс окисления. Закономерности окисления имеют достаточно общий характер для большинства твердых тел, поэтому методика локального зондового окисления применима ко всем материалам, которые допускают электрохимическое анодное окисление, а таких материалов очень много. Бездефектные полоски оксидов толщиной 1-10 нм получают на кремнии, алюминии, ниобии, титане и других материалах при скорости сканирования от 1 до 10 мкм/с. Их используют как элементы наноэлектронных приборов, а также в качестве маски при последующем селективном травлении. Это позволяет создавать электронные приборы с размерами элементов менее 1 нм.
Зондовое локальное химическое осаждение материалов из газовой фазы обычно проводят при комнатной температуре в сканирующем туннельном микроскопе, оснащенном газовым инжектором, сопло которого располагают в непосредственной близости от острия зонда (рис. 2.17). Этот метод опробован на металлах и полупроводниках. В качестве исходных реагентов обычно используют те же соединения, что и при традиционном осаждении материалов из газообразных металлоорганических соединений.
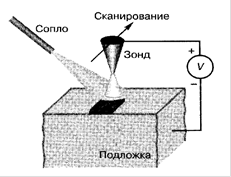
Рис. 2.17.Зондовое локальное химическое осаждение материала из газовой фазы
Процесс осаждения материала под зондом микроскопа регулируется несколькими механизмами, связанными с действием электрического поля в зазоре зонд-подложка. Сначала в сильном электрическом поле или за счет электронной бомбардировки происходит диссоциация исходных реагентов. Молекулы газа могут также ионизироваться за счет присоединения электронов. Продукты диссоциации дрейфуют в электрическом поле, создаваемом зондом, и адсорбируются только на расположенной непосредственно под острием зонда области поверхности подложки, поскольку напряженность неоднородного электрического поля в этой области максимальна и ионы мигрируют в нее. Хотя эффективность различных механизмов диссоциации и возбуждения расположенных под зондом молекул газа остается предметом научных дискуссий, это не ограничивает разработку различных вариантов практического использования локального зондового осаждения материалов. Метод обеспечивает нанесение полосок материала толщиной несколько нанометров и шириной 3-5 нм. Скорость осаждения составляет около 3 нм3/с. Для контроля процесса локального осаждения в сверхвысоком вакууме могут быть использованы механизмы хемосорбции. Они основаны на селективной десорбции атомов водорода с поверхности кремния сканирующим зондом. Различие химических свойств чистой и пассивированной водородом поверхности кремния позволяет осуществлять пространственно-селективные химические реакции в нанометровых дегидрогенизированных областях. Эти области затем служат трафаретом для селективного окисления, нитрирования и металлизации путем химического осаждения из газовой фазы. Нанотехнологические методы, использующие сканирующие зонды, достаточно перспективны для создания наноразмерных элементов из различных материалов. Они обеспечивают формирование твердотельных квантовых шнуров и квантовых точек с размерами порядка 10 нм и менее. Однако существенным ограничением для широкого применения этих методов является низкая скорость обработки подложек. Она остается недостаточной для массового производства.
Дата добавления: 2015-12-22; просмотров: 1475;
