Методи формування наноелектронних структур. 1 страница
Формирование наноразмерных структур для электроники осуществляется как с использованием традиционных микроэлектронных технологий, так и нанотехнологий. Нанотехнология (nanotechnology) - совокупность методов и средств, обеспечивающих создание контролируемым образом структур с размерами хотя бы в одном направлении менее 100 нм, а также материалов и функциональных систем на их основе. Рассматриваемые ниже технологические методы формирования наноэлектронных структур представляют собой практическую реализацию подходов «снизу-вверх» и «сверху-вниз».
ТРАДИЦИОННЫЕ МЕТОДЫ ФОРМИРОВАНИЯ ПЛЕНОК Ряд методов формирования тонких пленок, первоначально разработанных для технологии микроэлектроники, нашли широкое применение при создании наноэлектронных приборов и интегральных микросхем на их основе. К ним относятся химическое осаждение из газовой фазы и молекулярно-лучевая эпитаксия для создания планарных гетероструктур с нанометровыми размерами составляющих их слоев, а также электрохимические методы осаждения и окисления металлов и полупроводников для формирования пленок наноструктурированных материалов.
Химическое осаждение из газовой фазы (chemical vapor deposition, CVD)представляет собой группу технологических методов, в которых получение твердых веществ осуществляют с помощью химических реакций с участием газообразных реагентов. При этом используются следующие физико-химические процессы:
1) термическое разложение или диспропорционирование газообразных химических соединений;
2) взаимодействие двух или более газообразных веществ, приводящее к образованию твердого осадка;
3) пиролиз газообразных углеводородов, отличающийся от термического разложения многостадийностью и разветвленностью;
4) химическое взаимодействие газообразных веществ с твердыми подложками.
Технология химического осаждения из газовой фазы широко используется для получения пленок как одноэлементного состава, так и химических соединений. Их структура может варьироваться от аморфной до монокристаллической в зависимости от физико- химических свойств осаждаемого материала и материала подложки, а также от режима осаждения. Особенно широко эта группа методов применяется для создания полупроводниковых эпитаксиальных структур. Их формирование включает рост ориентированной монокристаллической пленки на подходящей для этих целей монокристаллической подложке. Материал пленки поступает из газовой фазы. Газовая среда может содержать как пары кристаллизующегося материала, так и газообразные реагенты, способные в процессе химических реакций образовывать на подложке необходимый для эпитаксиального роста материал. Осаждение пленок обычно проводится в проточных камерах при атмосферном или пониженном давлении, где газ-носитель, содержащий соответствующие реагенты, пропускается над нагретой монокристаллической подложкой. Химический состав газовой смеси и температура подложки являются главными параметрами, обеспечивающими процесс осаждения и свойства осажденных пленок. Применение металлоорганических соединений в качестве исходных газообразных реагентов дает наилучший результат при создании совершенных сверхрешеток с резкой границей раздела и толщиной вплоть до одного моноатомного слоя. Термин «металлоорганика» относится к обширной группе соединений, имеющих химические связи металл-углерод и металл-кислород-углерод, а также координационные связи между металлами и органическими молекулами. На практике используются преимущественно алкилы металлов с метильной (СН3) и этильной (С2Н5) группами. Подходящие для этих целей соединения и их основные свойства приведены в табл. 2.1. При комнатной температуре большинство из них представляют собой жидкости. Их вводят в реакционную камеру в потоке газа-носителя, предварительно насыщенного парами данного соединения в барботере, где газ-носитель проходит («пробулъкивает») через жидкое металлоорганическое соединение.
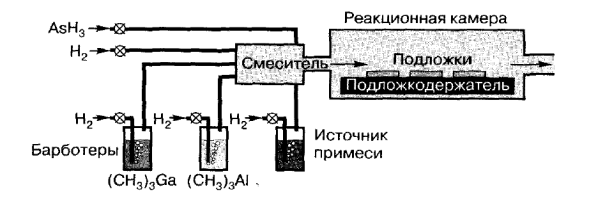
Рис. 2.1.Принципиальная схема установки для химического осаждения пленок из газовой фазы металлоорганических соединений при атмосферном давлениина примере осаждения GaAs и гетероструктур GaAlAs.
В качестве газа-носителя чаще всего применяют водород, чтобы предотвратить неконтролируемый пиролиз алкилов и гидридов. Химические превращения, происходящие на нагретой поверхности подложки, схематически можно представить следующей реакцией:

Акцепторные примеси, такие как Zn или Cd, могут быть введены в реакционную камеру в составе алкилов, а донорные, такие как Si, S, Se - в составе гидридов. Для осаждения пленок полупроводниковых нитридов третьей группы (AlN, GaN, InN) в качестве источника азота используется аммиак (NH3). Для формирования резких границ раздела путем изменения химического состава осаждаемого материала или легирующей примеси необходимо быстро изменять состав газовой смеси в реакционной камере. Для этого объемы смесительной камеры и самой реакционной камеры должны быть минимизированы. Изменение состава газовой смеси должно происходить без изменения общего потока газа через реакционную камеру. Наиболее резкие межфазные границы удается сформировать, используя режимы скоростного нагрева, когда продолжительность поддержания подложки при необходимой для осаждения температуре ограничена 30-60 с (при этом значительно уменьшается диффузионное перераспределение компонентов в окрестностях границ раздела).
Химическое осаждение из газообразных металлоорганических соединений обеспечивает формирование пленок практически всех бинарных, тройных и четверных полупроводниковых соединений А11IВV с высокой степенью их стехиометричности. Этот метод успешно применяется и для осаждения других полупроводников, таких как А11ВVI, а также оксидов. С его помощью формируются не только сплошные эпитаксиальные пленки, но и квантовые шнуры, и квантовые точки. Механизмы образования таких структур рассмотрены ниже.
Химическое осаждение из газовой фазы при пониженном давлении ( low pressure chemical vapor deposition, LPCVD)обычно осуществляют в откачиваемом горизонтальном цилиндрическом реакторе, принципиально аналогичном показанному на рис. 2.1, помещенном в двух- или трехзонную печь. Реактивный газ, содержащий осаждаемые компоненты в виде химических соединений, подают в «низкотемпературную» зону реактора, где происходит их разложение (декомпозиция); продукты реакций откачивают с противоположной стороны реактора. Подложки располагают в «высокотемпературной» зоне вертикально, т. е. перпендикулярно газовому потоку. Давление в реакционной камере поддерживают в пределах 0,1-2,0 Торр, что обеспечивает равномерное распределение осаждаемого материала по поверхности загруженных в реактор подложек (при этом осаждение происходит на обе поверхности подложек). Кинетика химических реакций в газовой фазе при пониженном давлении определяется теми же основными закономерностями, что и при атмосферном давлении, однако за счет пониженного давления в реакционной камере активируются диффузионные процессы на поверхности подложки. Это позволяет проводить осаждение материалов при более низких температурах и более равномерно покрывать рельеф ступенек на поверхности подложки. Повышается и точность управления составом осаждаемого материала.
Более значительные преимущества дает химическое осаждение из газовой фазы, стимулированное газоразрядной плазмой (plasma enhanced chemical vapor deposition, PECVD). В этом методе, реализуемом также при пониженном давлении (0,1-10 Торр), газоразрядная плазма служит источником дополнительной энергии для диссоциации молекул реакционных газов. Реактор типичной установки для проведения этого процесса включает диодную газоразрядную систему, на нижнем горизонтальном электроде которой размещают подложки. Плазму возбуждают подачей ВЧ-напряжения на электроды. В состав газовой среды помимо основных реагентов обычно добавляют инертный газ, обеспечивающий стабильность горения плазмы. Для улучшения равномерности осаждения материала на подложки нижний электрод вращают вокруг своей оси. Применение различных приемов возбуждения плазмы в реакционном объеме и изменение ее параметров позволяют управлять формированием заданного микрорельефа, структуры и примесного состава покрытия. Основными стимулирующими факторами при плазменном осаждении являются: - ускорение электронов в плазме при передаче энергии от внешнего источника; - возбуждение нейтральных атомов посредством столкновений с электронами; - ионизация нейтральных атомов под действием столкновений с электронами; - ионизация нейтральных атомов из-за столкновений с другими атомами или ионами; - рекомбинация ионов и электронов, сопровождаемая излучением. Важной характерной особенностью газоразрядной плазмы является присутствие в ней атомов и ионов водорода, являющихся продуктами диссоциации реактивных газов, особенно когда в качестве таковых используются гидриды. Они инициируют травление уже осажденного на подложку материала путем удаления радикалов, слабо связанных с подложкой. Благодаря этому происходит формирование более компактной структуры пленки, а в случае высокой концентрации водорода усиливается и процесс ее кристаллизации. По этой причине реактивные газы часто разбавляются водородом, если требуется сформировать поликристаллический материал. Недостатком разбавления водородом является снижение скорости роста пленки. Метод химического осаждения из газовой фазы, стимулированного газоразрядной плазмой, позволяет проводить формирование пленок и наноструктуры на их основе в диапазоне температур 250-400°С. Основным ограничением применения газоразрядной плазмы в качестве стимулирующего осаждение фактора является существенное усложнение технологичесkого оборудования, а следовательно, снижение его экономической эффективности.
Другим важным направлением развития технологии химического осаждения из газовой фазы при пониженном давлении реагентов является типично нанотехнологический метод осаждения атомарных слоев (atomic layer deposition, ALD). В нем формирование пленок химических соединений осуществляется с использованием хемосорбции и повторения самоограничивающихся реакций на поверхности твердых подложек. Метод предполагает следующие основные операции: 1) подготовительная обработка поверхности подложки с целью придания ей необходимых хемосорбционных свойств; 2) термообработка подложки в среде первого реакционного газа для формирования моноатомного слоя определенного компонента осаждаемого соединения; 3) очистка камеры от остатков первого реакционного газа и продуктов реакций; 4) термообработка подложки в среде второго реакционного газа для формирования моноатомного слоя другого компонента осаждаемого соединения и придания его поверхности хемосорбционных свойств, необходимых для повторного осаждения атомов первого компонента; 5) очистка камеры от остатков второго реакционного газа и продуктов реакций. Операции 2-5 повторяют до тех пор, пока не будет получена пленка необходимой толщины. В качестве реакционных газов пригодны уже отмеченные выше металлоорганические соединения и гидриды, а также алкоголяты, дикетонаты, амиды и хлориды. Главное требование к их выбору состоит в том, чтобы эти соединения не взаимодействовали друг с другом при последовательном введении в реакционную камеру. Температуру подложки в процессе осаждения поддерживают постоянной в интервале значений 100-500 °С. Осаждение одного моноатомного слоя продолжается от десятых долей до единиц секунд. Этого времени достаточно для завершения химических реакций и установления термодинамического равновесия на поверхности подложки. Очистку реакционной камеры обычно осуществляют азотом или аргоном. Применение метода осаждения атомарных слоев на примере формирования пленки А12О3 проиллюстрировано на рис. 2.3. В качестве газообразного источника алюминия используется триметилалюминий (CH3)3Al, а источником кислорода служат пары воды. Подложка может быть выполнена из кремния. Метод осаждения атомарных слоев позволяет формировать пленки обширной гаммы материалов - оксидов, нитридов, полупроводниковых соединений А11IВV, А11ВVI. Благодаря его саморегулирующейся природе толщина и состав осаждаемых пленок контролируется с атомарной точностью. Осаждаемые пленки равномерно (конформно) покрывают все ступеньки и неровности на поверхности подложки, что актуально при изготовлении интегральных микросхем с многоуровневой развитой конфигурацией составляющих ее элементов. Ограничением метода является его невысокая производительность, связанная с поатомным формированием пленки, требующим многократного повторения одних и тех же операций. Важный фактор - и качество подготовки исходной поверхности подложки. Любые дефекты атомарного масштаба на ней «прорастают» в пленку, что особенно критично при формировании эпитаксиальных наноструктур.
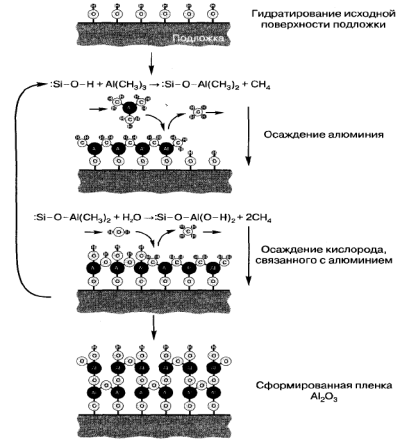
Рис. 2.3. Формирование nленки Аl2Оз нанесением атомарных слоев. В уравнениях химических реакций знаком «:» отмечены соединения, образующиеся на подложке
Уникальные возможности создания наноструктур, включая их трехмерные конфигурации, предоставляет метод химического осаждения, стимулированного электронным лучом (electron beam-induced deposition, EBID).Суть метода заключается в том, что молекулы относительно летучего исходного вещества (предшественника - прекурсора), содержащего атомы подлежащего осаждению материала, вводят в вакуумную камеру в газообразном виде вблизи подложки, поверхность которой сканируют электронным лучем. Этот процесс можно осуществить как в стандартном сканирующем электронном микроскопе, так и на специально сконструированном оборудовании. Энергию электронов задают в пределах 10-200 кэВ. Бомбардирующие поверхность подложки электроны передают свою энергию адсорбированным молекулам в области сканирования. Диссоциация молекул исходного вещества обусловлена главным образом вторичными электронами с энергией порядка 1 кэВ, испускаемыми подложкой, и сопровождается образованием летучих и нелетучих компонентов. Нелетучие осаждаются на облучаемой поверхности подложки, тогда как летучие соединения покидают реакционную область и удаляются из системы средствами откачки. В качестве исходных реакционных материалов используют традиционные для химического осаждения металлоорганические соединения. Например, для осаждения вольфрама и золота хорошие результаты дает W(CО)6 (гексакарбонил вольфрама) и Me2Au(tfac) (диметилтрифторацетилацетонат золота) соответственно. Данный метод можно рассматривать как вариант аддитивной литографии с использованием прямого осаждения без применения маскирующих слоев резиста. Скорость локального осаждения материалов может достигать 10 нм/с. Недостатком этого метода является невысокая чистота осаждаемых покрытий, что связано с неполным разложением молекул исходного вещества и загрязнением осаждаемого материала компонентами остаточного газа в вакуумной камере. Металлоорганические соединения содержат большое количество углерода и кислорода, входящих в состав продуктов их распада. Продукты распада, а также не продиссоциировавшие молекулы осаждаются на подложку вместе с металлом, загрязняя его. Для преодоления этого недостатка используют: 1) отжиг структур после осаждения или осаждение на нагретую подложку; 2) введение второго газа в камеру во время осаждения с целью удаления побочных продуктов реакции; 3) применение исходных веществ, не содержащих углерод; 4) проведение процесса осаждения в условиях сверхвысокого вакуума. Более чистые структуры можно получить путем замены электронов ионами. Этот метод получил название «химическое осаждение, стимулированное ионным лучом» (ion-beam-induced deposition, IBID).Он обычно реализуется в микроскопах с тонким пучком ионов галлия, ускоренных до энергии в несколько десятков килоэлектронвольт. Повышение степени чистоты осаждаемого материала происходит благодаря более высокой массе бомбардирующих частиц - ионов, а также локальному нагреву под действием пучка ионов, что позволяет большему числу компонентов расщепляться в результате реакции. Однако возникают другие проблемы, например, внедрение бомбардирующих ионов в подложку, повреждение поверхности и ухудшение разрешения. Осаждение, стимулированное электронным или ионным лучом, обычно применяется для безлитографического формирования наношнуров и наноточек из металлов и полупроводников, углеродных нанотрубок, получения наноострий катодов устройств полевой эмиссии, ферромагнитных наноструктур и других структур с размерами менее 10 нм. По экономическим показателям использование этих методов в массовом производстве изделий наноэлектроники представляется низкоэффективным. Главное же преимущество химического осаждения - возможность одновременной обработки большого числа подложек, что как нельзя лучше соответствует требованиям массового производства. Общим ограничением для всех описанных разновидностей метода остается плохо контролируемое загрязнение осаждаемого материала углеродом, а также необходимость строгого соблюдения мер безопасности при работе с металлорганическими соединениями и гидридами, которые токсичны и взрывоопасны.
Молекулярно-лучевая эпитаксия (molecu/ar Ьеат epitaxy)появилась как развитие метода химического осаждения пленок в сверхвысоком вакууме (давление остаточных газов ниже 10-7 Торр считается высоким вакуумом, а давление 10-11 Торр и ниже относится к сверхвысокому вакууму). Длина свободного (без взаимных соударений) пробега атомов и молекул в таких условиях достигает десятков метров. При молекулярно-лучевой эпитаксии реагенты вводятся в рабочую камеру в виде молекулярных или атомных потоков. Эти потоки формируются путем испарения материала внутри замкнутой ячейки с очень малым выходным отверстием. Она называется эффузионной (effusion) ячейкой, или ячейкой Кнудсена. Молекулы и атомы, выходя из отверстия ячейки в сверхвысокий вакуум, движутся без соударений (баллистически), создавая таким образом направленные, хорошо коллимированные потоки частиц (Коллимация — создание тонкого параллельно идущего потока излучения при помощи щелей, через которые он проходит). Для молекулярно-лучевой эпитаксии обычно используют несколько эффузионных ячеек - по одной на каждый конгруэнтно испаряющийся (без нарушения стехиометрии) материал. Кроме ячеек для осаждения основных материалов должны присутствовать и источники легирующих примесей. Наряду с испарением осаждаемого материала внутри эффузионной ячейки, молекулярные потоки могут формироваться по такому же принципу также из паров или газообразных соединений. Для этого их вводят в сверхвысоковакуумную камеру через специальные подогреваемые сопла. Конструкция типичной установки для молекулярно-лучевой эпитаксии схематически показана на рис. 2.4. Ее основными частями (помимо уже упомянутых эффузионных или газовых ячеек) являются подогреваемый подложкодержатель и система контроля за процессом осаждения. Все эти устройства размещены в сверхвысоковакуумной камере. Конденсация атомов и молекул на нагретой подложке в требуемых стехиометрических соотношениях представляет достаточно сложную задачу. Однако проведение осаждения в сверхвысоком вакууме позволяет использовать современные методы ионного и электронного исследования твердого тела непосредственно в процессе осаждения или сразу же после его завершения.
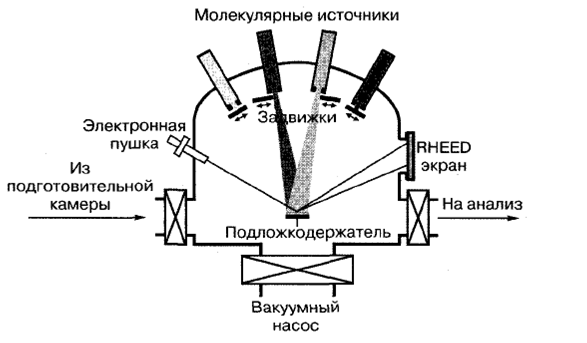 Рис. 2.4.Принципиальная схема установки для молекулярно-лучевой эпитаксии 2.1.
Рис. 2.4.Принципиальная схема установки для молекулярно-лучевой эпитаксии 2.1.
Для этих целей в сиетему мониторинга включают: Оже-электронную спектрометрию (Auger electron spectrometry, AES), дифракцию низкоэнергетических электронов (low energy electron dijfraction, LEED), дифракцию отраженных высокоэнергетических электронов (rejlection high energy e/ectron dijfraction, RНEED), спектроскопию возбужденной рентгеновским или ультрафиолетовым издучением фотоэмиссии (x-ray and ultraviolet photoemission spectroscopy, XPS and UPS), вторичную ионную масс-спектрометрию (secondary ion mass spectrometry, SIMS). Проведение анализа осажденной пленки непосредственно в рабочей камере называют in situ-анализом, что означает «по месту», т. е. в данном случае - там же, где изготовлен образец. Для оперативного контроля и управления процессом осаждения обычно используют дифракцию отраженных высокоэнергетических электронов (RHEED). Для этого электроны с энергией 10-15 кэВ направляют под скользящим углом на подложку с осажденной пленкой, как это показано на рис. 2.4. Дифракция отраженных электронов регистрируется на экране, расположенном на противоположной от электронной пушки стенке камеры. Положение и интенсивность дифракционных максимумов содержат информацию о структуре и толщине поверхностного слоя, что и используется для мониторинга процесса осаждения. Молекулярно-лучевая эпитаксия широко применяется для формирования высококачественных сверхрешеток. Следует напомнить, что для этих целей подходит и более производительный метод - химическое осаждение из металлоорганических соединений. Однако по степени дефектности, концентрации неконтролируемых примесей и резкости межфазных границ этот метод уступает молекулярно-лучевому осаждению. Как и в случае химического осаждения из газовой фазы, молекулярно-лучевая эпитаксия обеспечивает при определенных условиях осаждения формирование и сплошных наноразмерных пленок, и квантовых шнуров, и квантовых точек.
Электрохимическое осаждение металлов и полупроводников ( electrochemical deposition, electroplating)состоит в нанесении материала на токопроводящую поверхность подложки за счет пропускания тока через контактирующую с ней жидкую среду, содержащую химические элементы осаждаемого материала. Оно позволяет формировать как однородные по составу, так и многокомпонентные аморфные и наноструктурированные покрытия из металлов, их сплавов и полупроводников с хорошей адгезией к подложке. Ключевой элемент оборудования для электрохимического осаждения материалов - электролитическая ячейка, принципиальную конструкцию и основные элементы которой иллюстрирует рис. 2.6. Она включает три электрода, помещенных в ванну, заполненную жидкой электропроводящей средой - электролитом. В качестве одного из электродов выступает подложка, на которую производится осаждение материала. На нее подается отрицательное по полярности напряжение, т. е. она является катодом по отношению к другому электроду - аноду. Пропускание тока по цепи анод-электролит-катод и обеспечивает электрохимическое осаждение материала. Анод может быть двух типов: жертвенный (расходуемый анод) или инертный (нерасходуемый анод). Расходуемые аноды изготавливаются из материала, который необходимо осадить на катоде. Нерасходуемые аноды предназначены только для замыкания электрической цепи и не являются источником атомов материала, замещающих в электролите ушедшие на катод атомы. В качестве материала инертных анодов обычно используют платину или углерод (графит). Третий электрод - электрод сравнения, служит для контроля потенциала катода во время процесса осаждения. Наиболее распространенными электродами сравнения являются ртутный, каломельный и хлорсеребряный электроды. Поскольку их собственные потенциалы отличаются друг от друга, за точку отсчета принимается потенциал стандартного водородного электрода, который принимается равным нулю. Потенциалы указанных выше электродов сравнения относительно водородного электрода, представляющие собой справочные данные, учитываются в измерениях.
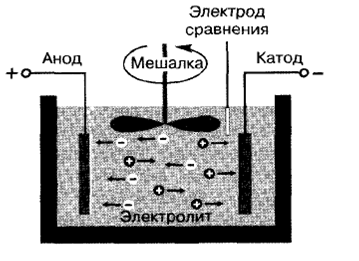
Рис. 2.6.Электролитическая ячейка для электрохимического осаждения материалов
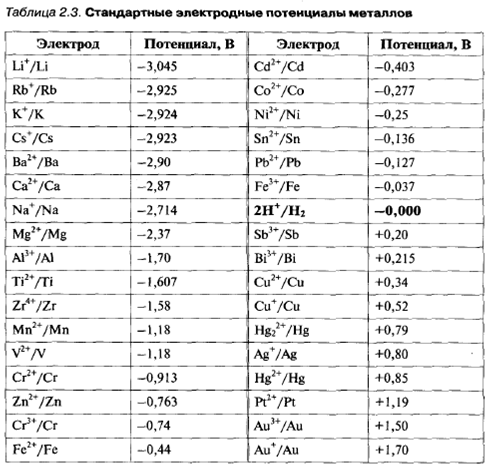
Потенциал электрода, измеренный относительно стандартного водородного электрода, называют стандартным электродным потенциалом (standard electrode potential). Если расположить все металлы в ряд по мере возрастания величины стандартного электродного потенциала, как это сделано в табл. 2.3, получается так называемый ряд напряжений металлов, который характеризует их способность отдавать и принимать электроны в электрохимических процессах. С возрастанием величины стандартного электродного потенциала металлов увеличивается окисли - тельная способность соответствующих им катионов (катионы металла легче принимают электроны). Восстановительная же способность металлов (атомы металла легче отдают электроны) в этом ряду уменьшается. С понижением стандартного электродного потенциала наблюдается противоположная зависимость. Все металлы, расположенные в электрохимическом ряду напряжений до водорода, т. е. имеющие электродный потенциал меньше, чем у водорода, в стандартных условиях могут быть окислены ионами Н+. По этой причине эти металлы могут вытеснять водород из воды или растворов кислот. Металлы с потенциалом меньшим, чем -0,4 В (Fe, Cr, Zn, ... ), могут восстанавливать водород из воды. Однако на практике это не всегда достижимо из-за того, что происходит их окисление, и на поверхности образуются беспористые механически прочные и обладающие хорошей адгезией к поверхности металла нерастворимые (пассивирующие) пленки, препятствующие дальнейшему взаимодействию. Металлы, расположенные после водорода, т. е. имеющие электродный потенциал больше, чем у водорода, не вытесняют водород из растворов кислот. Такие металлы, как Ti, А1 можно осадить только из органических электролитов, тогда как Mg, Nb, Та, W можно осадить из электролитов на основе расплавов солей (при температуре 700 °С и выше). Типичный электролит представляет собой проводник, в котором электрический заряд переносится ионами (проводник второго рода). В электролитической ячейке электролит замыкает внутреннюю электрическую цепь между анодом и катодом. При протекании электрического тока через электролит положительно заряженные ионы ‒ катионы, а это обычно ионы металлов, перемещаются к катоду, а отрицательно заряженные ‒ анионы, к аноду. Когда катионы достигают катода, поступающие к нему из внешней цепи электроны нейтрализуют положительный заряд катионов, приводя к осаждению металла на катоде. Количественно электрохимическое осаждение материалов описывается закономерностями, открытыми М. Фарадеем. Первый закон Фарадея: при электрохимическом осаждении количество вещества, участвующего в химических превращениях, пропорционально количеству электричества, проходящему через электролит.
Второй закон Фарадея: массы различных веществ, выделяемых или растворяемых одним и тем же количеством электричества, пропорциональны их электрохимическим эквивалентам (химическим эквивалентным массам). Количество электричества, соответствующее превращению одного химического эквивалента вещества, получило название «Число, или постоянная, Фарадея», F. Толщина d металла, осажденного в идеальных условиях, т. е. без побочных реакций, приводящих к отклонениям от законов Фарадея, может быть оценена из выражения
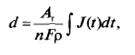 d =А_ J J(t)dt, nFp (2.1.2) где Аг - атомная масса; ρ - объемная плотность металла; п - число электронов, принимающих участие в единичном акте восстановления; J(t) - плотность электрического тока, при которой осуществлялось катодное осаждение. (Электрохимический эквивалент элемента - это атомная масса элемента, деленная на величину изменения валентности данного элемента в результате реакции. Например, для реакции Fe2+ ~ Fe0 величина изменения валентности 2, тогда электрохимический эквивалент железа равен 55,85/2 = 27 ,925. В зависимости от типа реакции один элемент может иметь различные электрохимические эквиваленты). Важной характеристикой процесса электрохимического осаждения является эффективность (выход0 по току (current efficiency, current yield).Это израсходованная на осаждение металла доля носителей заряда, прошедших через электролит. Она определяется как отношение количества реально осажденного на катоде (или растворенного на аноде) металла к количеству металла, которое следовало бы ожидать из расчетов согласно законам Фарадея. Эффективность по току менее 100% свидетельствует о протекании в электролите и на электродах побочных реакций, приводящих к отклонениям от этих законов. Основными параметрами электрохимического осаждения, определяющими структуру и свойства катодных покрытий, являются состав и температура электролита, плотность пропускаемого электрического тока и продолжительность процесса осаждения, условия перемешивания электролита. На качество осаждаемых покрытий существенное влияние оказывают подготовка поверхности катода и свойства электролита. При электрохимическом осаждении из водных электролитов металлов, имеющих стандартные потенциалы меньше, чем у водородного электрода, следует считаться и с высокой вероятностью параллельно протекающего восстановления водорода на катоде. Структура осажденной пленки определяется скоростью образования и роста кристаллических зародышей на катоде. Образованию новых зародышей и осаждению мелкозернистого осадка способствует сохранение высокой концентрации разряжающихся ионов металла в прикатодном слое электролита. Увеличение плотности тока и связанный с этим рост поляризации катода также способствуют образованию компактного мелкокристаллического осадка. При высоких плотностях тока из-за обеднения прикатодного слоя электролита реагирующими ионами происходит усиленный рост выступающих областей осадка навстречу потоку разряжающихся ионов. При этом образуются рыхлые пористые пленки, а иногда и четко выраженные дендриты (ветвистые или игольчатые древовидные кристаллы). Для формирования высококачественных пленок применяют электролиты сложного состава, включающие: 1) соль осаждаемого металла; 2) комплексообразователь; 3) фон - нейтральную соль, увеличивающую электропроводность; 4) буферную добавку, способствующую сохранению оптимального значения рН электролита; 5) добавки, уменьшающие пассивацию анода; 6) поверхностно- активные вещества, повышающие поляризацию катода и таким образом способствующие образованию мелкокристалли ческих осадков. В наноэлектронике метод электрохимического осаждения используется для создания многослойных структур из металлов и полупроводников, а также наношнуров, нанотрубок и наноточек из этих материалов. Основные металлы и сплавы, наносимые этим методом представлены в табл. 2.4.
d =А_ J J(t)dt, nFp (2.1.2) где Аг - атомная масса; ρ - объемная плотность металла; п - число электронов, принимающих участие в единичном акте восстановления; J(t) - плотность электрического тока, при которой осуществлялось катодное осаждение. (Электрохимический эквивалент элемента - это атомная масса элемента, деленная на величину изменения валентности данного элемента в результате реакции. Например, для реакции Fe2+ ~ Fe0 величина изменения валентности 2, тогда электрохимический эквивалент железа равен 55,85/2 = 27 ,925. В зависимости от типа реакции один элемент может иметь различные электрохимические эквиваленты). Важной характеристикой процесса электрохимического осаждения является эффективность (выход0 по току (current efficiency, current yield).Это израсходованная на осаждение металла доля носителей заряда, прошедших через электролит. Она определяется как отношение количества реально осажденного на катоде (или растворенного на аноде) металла к количеству металла, которое следовало бы ожидать из расчетов согласно законам Фарадея. Эффективность по току менее 100% свидетельствует о протекании в электролите и на электродах побочных реакций, приводящих к отклонениям от этих законов. Основными параметрами электрохимического осаждения, определяющими структуру и свойства катодных покрытий, являются состав и температура электролита, плотность пропускаемого электрического тока и продолжительность процесса осаждения, условия перемешивания электролита. На качество осаждаемых покрытий существенное влияние оказывают подготовка поверхности катода и свойства электролита. При электрохимическом осаждении из водных электролитов металлов, имеющих стандартные потенциалы меньше, чем у водородного электрода, следует считаться и с высокой вероятностью параллельно протекающего восстановления водорода на катоде. Структура осажденной пленки определяется скоростью образования и роста кристаллических зародышей на катоде. Образованию новых зародышей и осаждению мелкозернистого осадка способствует сохранение высокой концентрации разряжающихся ионов металла в прикатодном слое электролита. Увеличение плотности тока и связанный с этим рост поляризации катода также способствуют образованию компактного мелкокристаллического осадка. При высоких плотностях тока из-за обеднения прикатодного слоя электролита реагирующими ионами происходит усиленный рост выступающих областей осадка навстречу потоку разряжающихся ионов. При этом образуются рыхлые пористые пленки, а иногда и четко выраженные дендриты (ветвистые или игольчатые древовидные кристаллы). Для формирования высококачественных пленок применяют электролиты сложного состава, включающие: 1) соль осаждаемого металла; 2) комплексообразователь; 3) фон - нейтральную соль, увеличивающую электропроводность; 4) буферную добавку, способствующую сохранению оптимального значения рН электролита; 5) добавки, уменьшающие пассивацию анода; 6) поверхностно- активные вещества, повышающие поляризацию катода и таким образом способствующие образованию мелкокристалли ческих осадков. В наноэлектронике метод электрохимического осаждения используется для создания многослойных структур из металлов и полупроводников, а также наношнуров, нанотрубок и наноточек из этих материалов. Основные металлы и сплавы, наносимые этим методом представлены в табл. 2.4.
Дата добавления: 2015-12-22; просмотров: 2707;
