Константа равновесия
Характерной гомогенной обратимой реакцией является синтез аммиака.
3H2 + N2 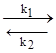 2NH3
2NH3
k1 и k2 – константы скоростей прямой и обратной реакций соответственно. Запишем выражения для скоростей прямой и обратной реакций:
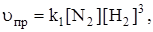
[N2] и [H2] – концентрации азота и водорода в состоянии равновесия, т.е. равновесные концентрации.
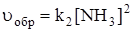 .
.
В начальный момент времени uобр = 0, т.к. [NН3]= 0. По мере увеличения концентрации аммиака и уменьшения концентраций исходных веществ uпр уменьшается, а uобр увеличивается. В определенный момент времени наступает динамическое равновесие, т.е. uпр = uобр и 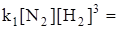
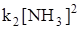 . Отношение констант скоростей прямой и обратной реакции называется константой равновесия. Она равна произведению концентраций продуктов реакций в степенях их стехиометрических коэффициентов. Деленному на произведение концентраций исходных веществ, также в степенях их стехиометрических коэффициентов.
. Отношение констант скоростей прямой и обратной реакции называется константой равновесия. Она равна произведению концентраций продуктов реакций в степенях их стехиометрических коэффициентов. Деленному на произведение концентраций исходных веществ, также в степенях их стехиометрических коэффициентов.
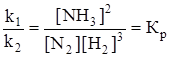
Рассмотрим случай обратимой гетерогенной реакции:
СО2(г) + С(тв) 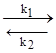 2СО.
2СО.
В реакторе лежит уголь, над которым пропускают СО2. СО2 взаимодействует с верхним слоем угля, при этом открывается следующий слой угля, т.е. концентрация атомов углерода не меняется:
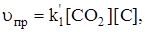
[C] = const, 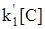 = const = k1,
= const = k1,
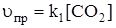 .
.
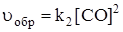
uпр = uобр и 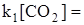
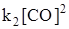 .
.
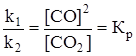
Концентрация твердых фаз не входит в выражение для константы скорости.
Дата добавления: 2015-10-21; просмотров: 973;
