Химические свойства. Гадогенокарбоновые кислоты более сильные кислоты, чем карбоновые
Гадогенокарбоновые кислоты более сильные кислоты, чем карбоновые. Введение галогенов в молекулу увеличивает силу кислот.
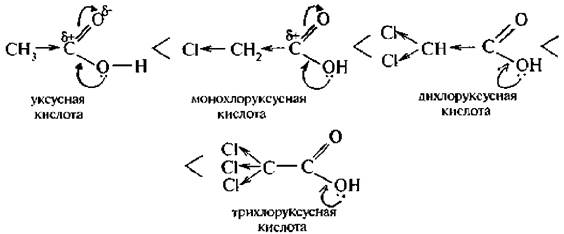
Сила кислот зависит от величины дробного положительного заряда на атоме углерода карбоксильной группы. А величина δ+ увеличивается с введением галогенов, которые обладают отрицательным индуктивным эффектом. Например, трихлоруксусная кислота по силе приравнивается к серной кислоте. Значит, сила кислоты зависит от количества атомов галогена в углеродном радикале. Кроме того, сила кислоты зависит от положения галогена в цепи. Поскольку индуктивное смешение эффективно на протяжении четырех – пяти σ-свкзей, то α-галогенокарбоновые кислоты более сильные, чем β-, а β– сильнее, чем у-гадогенокарбоновые кислоты.
Для галогенокарбоновых кислот характерны реакции по карбоксильной группе и реакции с участием атома галогена.
По карбоксильной группе они образуют все функциональные производные карбоновых кислот: соли, сложные эфиры, ангидриды, галогенангидриды, амиды и др.
Например:
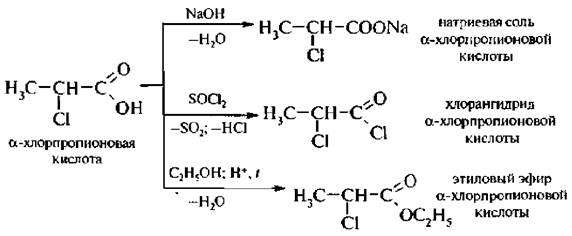
Алифатические галогенокарбоновые кислоты, подобно галогеналканам, вступают в реакции замещения галогена по механизму нуклеофильного замещения (SN). Причем, подвижность галогена зависит от взаимного расположения галогена и карбоксильной группы. Карбоксильная группа, как электроакцепторная группа (-I), увеличивает подвижность атома галогена в молекуле:
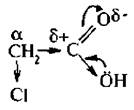
Больше всего галоген будет подвижен при α-углеродном атоме. Подвижность атома галогена можно подтвердить целым рядом реакций:
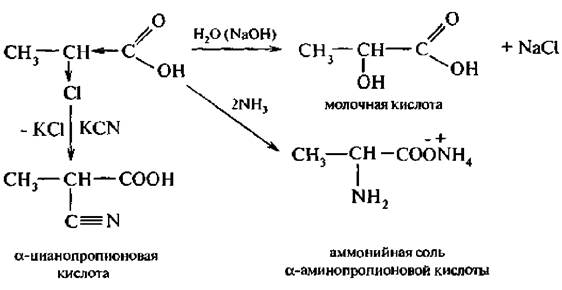
Галоген в β-положении менее подвижен, а в γ-положении влияние карбоксильной группы практически не сказывается.
Галогенокарбоновые кислоты находят широкое применение для получения окси- и аминокислот, широко используются в органическом синтезе лекарственных препаратов, например: уреид α-бромизовалериановой кислоты – бромизовал – это снотворный препарат
ГИДРОКСИКИСЛОТЫ (СПИРТОКИСЛОТЫ, ФЕНОЛОКИСЛОТЫ)
Гидроксикислоты – это производные карбоновых кислот в молекуле которых помимо карбоксильной группы содержится одна или несколько гидроксилъных групп. Для них вводятся понятия основность и атомность. Основность определяется числом карбоксильных групп в молекуле, а атомность – общим числом гидроксилькых групп, включая гидроксильную группу карбоксила.
Например:
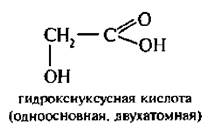
Для названия гидроксикислот наряду с заместительной номенклатурой широко применяются тривиальные названия. По заместительной номенклатуре ИЮПАК за родоначальную структуру принимается кислота, а положение гидроксильной группы в молекуле обозначают буквами греческого алфавита или цифрами.
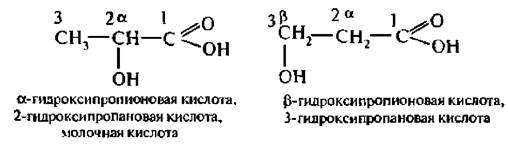
По положению гидроксильноЙ группы относительно карбоксильной гидрокислоты делятся на α, β, γ и т. д.
Дата добавления: 2015-09-29; просмотров: 3244;
