Приклади розв’язку задач. Приклад 1. Визначити число молекул, що містяться в 1 см3 води, і масу молекули води
Приклад 1. Визначити число молекул, що містяться в 1 см3 води, і масу молекули води. Виходячи з того, що молекули води мають вигляд кульок, що стикаються одна з одною, знайти діаметр молекул.
Дано: V = 10-6 м3, 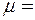 18·10-3 кг/моль,
18·10-3 кг/моль, 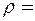 103 кг/м3.
103 кг/м3.
Знайти: N, m1, d.
Розв’язок. Спочатку, користуючись таблицями фізичних величин, знайдемо густину, а потім і молярну масу води. Молярна маса пов’язана з відносною молекулярною масою речовини Mr формулою
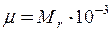 кг/моль. (1)
кг/моль. (1)
Відносна молекулярна маса речовини дорівнює сумі відносних атомних мас всіх елементів, атоми яких входять до складу молекули даної речовини, і визначається формулою
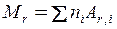 , (2)
, (2)
де Ar,i – відносна атомна маса i-го елемента, а ni – число атомів i-го елемента, що входять у молекулу.
Хімічна формула води має вигляд H2O. Звідси випливає, що до складу даної молекули входять два атоми водню (n1 = 2) і один атом кисню (n2 = 1). Значення відносних атомних мас водню і кисню знайдемо з таблиці Д.І. Менделєєва: Ar,1 = 1; Ar,2 = 16.
Таким чином, з (1) і (2) для води маємо
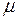 = (n1Ar,1 + n2Ar,2)·10-3 = (2·1 + 1·16)·10-3 = 18·10-3 кг/моль.
= (n1Ar,1 + n2Ar,2)·10-3 = (2·1 + 1·16)·10-3 = 18·10-3 кг/моль.
Відповідно до визначення, кількість однорідної речовини 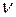 даної маси m дорівнює
даної маси m дорівнює
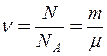 , (3)
, (3)
де NA – число Авогадро.
Виразивши масу як добуток густини 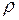 на об’єм V, з виразу (3) одержимо
на об’єм V, з виразу (3) одержимо
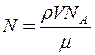 . (4)
. (4)
Масу однієї молекули легко знайти, поділивши молярну масу на число Авогадро
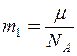 . (5)
. (5)
Для визначення діаметру молекули води приблизно будемо вважати, що в рідині молекули мають форму кульок, що щільно прилягають одна до одної. Згідно з цими уявленнями на кожну молекулу приходиться об’єм V1, що дорівнює об’єму кубічного осередку зі стороною d
V1 = d3. (6)
З іншого боку, об’єм V1 можна знайти, розділивши повний об’єм на число молекул
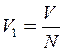 . (7)
. (7)
Таким чином, підставляючи вираз (7) у (6) і використовуючи (4), можна одержати
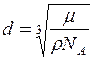 . (8)
. (8)
Дата добавления: 2015-09-28; просмотров: 1330;
