Тема: Ферменти як біологічні каталізатори. Механізм дії ферментів
План
1.Ферменти, їх будова .
2.Механізм дії ферментів.
3.Застосування ферментних препаратів у медицині.
Час виконання: 2 години
Мета роботи: ознайомитися з механізмом дії ферментів та застосуванням ферментних препаратів у медицині.
Усі хімічні процеси в умовах фізіологічного середовища організму можуть відбуватися тільки за участю каталізаторів, які називають ферментами ( від лат. fermentum - закваска ), або ензимами.
Ферменти - це речовини білкової природи, які виробляються клітинами тих організмів і значно збільшують швидкість біохімічних процесів.
Нині відомо кілька тисяч таких речовин, дуже багато з яких виділено у чи-ому вигляді. Вважають, що в клітині міститься близько 10 тис. молекул різних ферментів, які прискорюють понад 2 тис. реакцій. Четверта частина всіх вивчених ферментів містять йони різних металів, тому їх називають металоферментами.
Дію ферментів довго вважали загадковою, а тому віталісти2 пояснювали її виявом особливої життєвої сили, яка відрізняє живу і неживу речовини. Нині доведено, що ферменти - це біокаталізатори, дія яких не відрізняється від штучно добутих колоїдних систем. І ферменти, і неорганічні каталізатори підпорядковуються загальним законам каталізу.
Будова ферментів. Ферменти складаються з великого числа амінокислот, сполучених між собою пептидними зв'язками (первинна структура). Молекули містять гідрофобний ланцюг (вуглеводневий радикал) і полярні групи: - СООН, - NH2 , = NH, - ОН, - SH. Між окремими ділянками поліпептидного ланцюга за участю цих полярних груп утворюються водневі зв'язки і тому макромолекули ферментів по-різному згинаються, утворюючи нещільні клубки. Виникає чітко визначена й індивідуальна для кожного взятого ферменту вторинна структура. На певній ділянці такої структури утворюється активний каталітичний центр, тобто частина ферменту, яка бере участь у безпосередній взаємодії з субстратом. Активний центр складається лише з кількох залишків амінокислот, а в металоферментах - ще з йонів металу, які надають макромолекулі ферменту чіткої геометричної конфігурації. Тому ферменти характеризуються високою специфічністю, вибірково прискорюючи тільки певні типи біохімічних реакцій. Наприклад, фермент декарбоксилаза відщеплює від амінокислоти карбоксильну групу і не діє на аміногрупу цієї кислоти. Для відщеплення від амінокислоти аміногрупи існує фермент трансаміназа.
Ферменти характеризуються і високою специфічністю відносно певних
хімічних сполук, з якими цей фермент взаємодіє. Зокрема, є ферменти, які
діють тільки на один з ізомерів хімічної сполуки.
Другою характерною особливістю ферментів, порівняно зі звичайними каталізаторами, є їх висока каталітична активність у досить м'яких умовах (температура, тиск і кислотність середовища). Збільшення швидкості біохімічних перетворень, що досягається під дією ферментів, дуже велике. Так, реакція гідролізу сечовини за наявності ферменту уреази прискорюється в 1 млрд разів, а процес гідратації вуглекислого газу під дією карбоангідрази - у 10 млн разів. Такої швидкості реакцій за участю звичайних неорганічних каталізаторів досягти неможливо.
Крім того, швидкість ферментативних реакцій прямо пропорційна концентрації ферменту, тоді як для звичайного каталізу такої чіткої залежності немає. Тому якщо в організмі не вистачає якогось ферменту, це призводить до зменшення швидкості метаболізму тієї чи іншої речовини, що негативно впливає на стан здоров'я людини.
Назву ферментів за тривіальною номенклатурою утворюють так. Спочатку називають субстрат, на який діє фермент, потім тип реакції, яку він каталізує, і додають закінчення -аза. Наприклад, назва ферменту, що каталізує процес окиснення спиртів, утворюється так:
Алкоголь + дегідрогенізація + аза = Алкогольдегідрогеназа.
Для деяких давно відомих ферментів залишилися раніше вживані традиційні назви, наприклад: пепсин (відкритий у шлунковому соку в 1836 p.), трипсин, каталаза, амілаза та ін.
Назви ферментів за систематичною номенклатурою дещо складніші і розглядаються в курсі біохімії.
Для речовин, що беруть участь у ферментативних реакціях, прийнято такі терміни та їх позначення:
S, субстрат - хімічна речовина або тип речовин, на яку діє фермент;
Е, фермент (ензим) - каталітично активна речовина, що прискорює реакцію;
Р - продукт реакції;
І - інгібітор каталітичної реакції.
Механізм дії ферментів. Як зазначалося вище, ферментативні реакції відбуваються зі швидкостями у 108—1020 разів більшими, ніж без каталізатора. Таке істотне зростання швидкості пов'язане зі зміною енергії активації біохімічних реакцій. Істотне зменшення енергії активації каталітичних реакцій пов’язане із зміною механізму їх перебігу, який включає утворення однієї або кількох проміжних сполук. На уявленнях про утворення проміжних комплексів ґрунтується сучасна теорія ферментативного каталізу. За теорією Михаеліса – Ментен процес ферментативного каталізу складається з кількох стадій:
а) утворення активних центрів ферменту Е з субстратом S, що призводить до утворення фермент – субстратного комплексу ES;
б) розпад проміжного комплексу на вихідний субстрат S і фермент E;
в) розпад проміжного комплексу з утворенням кінцевих продуктів реакції Р і вивільненням ферменту Е. Цей процес можна проілюструвати так:
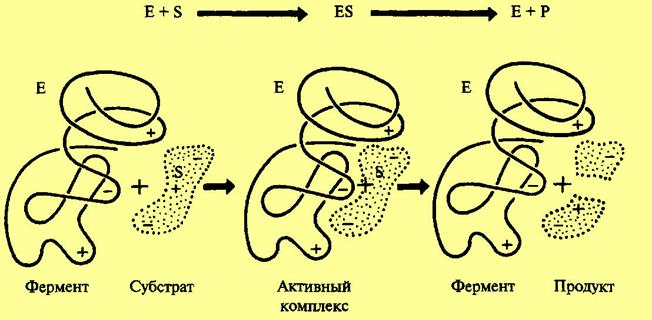
За теорією Фішера, утворення проміжного комплексу може настати тільки в тому разі, якщо просторова будова молекули субстрату точно відповідає структурі активного центру ферменту. Якщо субстрат підходить до активного центру ферменту як «ключ до замка», то реакція відбудеться, але якщо субстрат («ключ») дещо інший і не відповідає активному центру («замку»), то реакція не відбудеться. Таким чином, теорія Фішера просто і наочно пояснює специфічність дії ферментів.
Проте подальші дослідження Кошланда показали, що молекула ферменту не є жорсткою, а досить гнучка і еластична. Субстрат часто сам спонукає фермент до утворення відповідного активного центру, тобто конформації ферменту та його активного центру змінюються в процесі приєднання субстрату. Це дає можливість пояснити пояснити групову субстратну специфічність ферментів, тобто явище, коли дещо різні за будовою «ключі» (субстрати) підходять до одного «замка» (активного центру ферменту).
Кожен фермент характеризується певною молекулярною активністю. Під молекулярною активністю ферменту розуміють кількість молекул субстрату, що перетворюються впродовж 1 хв на одному активному центрі ферменту за стандартних умов.
Молекулярна активність більшості вивчених ферментів перебуває у межах 1∙104 - 6∙106 хв-1 . Активність ферментів визначають у медичній практиці для діагностики захворювань (ензимодіагностика) і контролю за процесом лікування, оскільки зміна активності ферментів є виявом функціональних змін в організмі. Нині розроблено методики кількісного визначення багатьох поширених ферментів, встановлено рівні їх активності і межі коливань у нормі та при різних патологіях.
Так, за зміною активності ферменту аспартатамінотрансферази у крові можна діагностувати інфаркт міокарда в перші години захворювання з більшою точністю, ніж за допомогою ЕКГ. Збільшення активності ферменту аланін амінотрансферази є надійним діагностичним критерієм гострої стадії гепатиту, а підвищення активності діастази в сечі – ознакою запалення підшлункової залози.
На каталітичну активність впливають температура і рН середовища
Каталітична активність більшості ферментів виявляється у вузькому
інтервалі температур - від 10 до 56 °С. За вищих температур руйнується білкова основа ферменту, тобто відбувається процес коагуляції білків, а за нижчих - перебіг і ферментативних процесів сповільнюється, що пов'язано зі зростанням в'язкості внутрішньо- та міжклітинних рідин.
На каталітичну активність ферментів істотно впливає значення рН
середовища. При цьому, швидкість ферментативних реакцій при збільшенні рН різко зростає і, досягнувши певного максимуму, знову різко знижується. Концентрація йонів Гідрогену Н+ , за якої швидкість ферментативної реакції і досягає максимального значення, є оптимальною для функціонування цього і ферменту. Для більшості ферментів оптимальне значення рН перебуває в межах 4-10.
Слід зазначити, що каталітична дія деяких ферментів не підпорядковується наведеним вище закономірностям. Зокрема, рибонуклеаза виявляє активність за температури як понад 60 °С (практично до 100 °С), так і нижче 0 °С. Фермент пепсин є найактивнішим у кислотному середовищі при рН = 1,0—2,2
Дата добавления: 2015-09-18; просмотров: 3859;
