Примеры решения задач. Пример 28.1. Написать уравнения реакций, при помощи которых из метана и неорганических реагентов можно получить бутан.
Пример 28.1. Написать уравнения реакций, при помощи которых из метана и неорганических реагентов можно получить бутан.
Решение. 1. Бромированием метана можно получить бромметан:
CH4 + Br2 → CH3Br + HBr
2. При нагревании бромметана с натрием образуется этан:
2CH3Br + 2Na → C2H6 + 2NaBr
3. При взаимодействии этана с бромом образуется бромэтан:
C2H6 + Br2 → C2H5Br + HBr
4. Бутан получается из бромэтана по реакции Вюрца:
2C2H5Br + 2Na → C4H10 + 2NaBr
Пример 28.2. При сжигании газообразного углеводорода объемом 2,24 л было получено оксида углерода (IV) массой 13,2 г и воды массой 7,2 г. Плотность газа по воздуху составляет 1,52 (н.у.). Определить молекулярную формулу газа.
Решение. 1. Молярная масса газа равна:
М (возд.) = 29 г/моль; Dвозд.(газа) = 1,52;
М (газа) = 29 г/моль ∙ 1,52 = 44 г/моль.
2. Масса углерода и водорода в 2,24 л углеводорода составляет:
12 г углерода образует 44 г СО2
х « углерода « 13,2 « СО2 х = 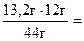 3,6 г С,
3,6 г С,
2 г водорода образует 18 г Н2О
y « водорода « 7,2 « Н2О у =  0,8 г Н.
0,8 г Н.
3. Масса углерода и водорода в сожженном газе составляет:
3,6 + 0,8 = 4,4г.
4. Рассчитаем массу 2,24 л углеводорода:
44 г углеводорода занимает объем 22,4 л
х « углеводорода « « 2,24 « х = 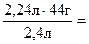 4,4 г.
4,4 г.
5. Значит, газ состоит тлько из углерода и водорода. Следовательно,
С:Н = 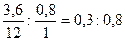 = 1:2,66,
= 1:2,66,
Откуда простейшая формула СН2,66 (М = 14,66). Отношение истинного соединения к массе простейшего соединения составляет 44/14,66 = 3. Следовательно, простейшую формулу надо увеличить в 3 раза, откуда истинная формула газа С3Н8.
Пример 28.3. Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
этиловый спирт → Х → Y → Z → бутен-1
Указать условия протекания реакций.
Решение. 1. При нагревании этилового спирта до 180 – 200 оС с концентрированной серной кислотой должен образоваться продукт, реагирующий с бромоводородом. Это этилен (вещество Х). Уравнение реакции:
С2Н5ОН 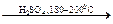 С2Н4 + Н2О
С2Н4 + Н2О
2. В результате присоединения бромоводорода к этилену образуется бромэтан (Y):
С2Н4 + НBr → C2H5Br
3. При нагревании бромэтана в присутствии натрия образуется бутан (Z)
C2H5Br + 2Na → C4H10 + 2NaBr
4. Дегидрирование бутана в присутствии катализатора, например никеля – один из способов получения алкенов, в частности бутена-1.
CH3−CH2−CH2−CH3 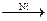 CH2=CH−CH2−CH3 + Н2
CH2=CH−CH2−CH3 + Н2
Пример 28.4. Написать уравнения реакций, которые надо провести для осуществления следующих превращений:
циклогексан → бензол → толуол → бензойная кислота
Указать условия протекания реакций.
Решение. 1. Циклогексан превращается в бензол при пропускании его паров над нагретым платиновым катализатором:
С6Н12 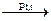 С6Н6 + 3Н2
С6Н6 + 3Н2
2. Ввести алкильную группу в бензольное кольцо можно действием галогеналкила в присутствии хлорида алюминия:
C6H6 + CH3Cl 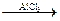 C6H5−CH3 + HCl
C6H5−CH3 + HCl
3. При действии раствора перманганата калия на толуол образуется бензойная кислота:
C6H5−CH3 + 3[O] 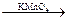 C6H5−COOH + H2O
C6H5−COOH + H2O
Задачи
№ 28.1.Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
Al4C3 → CH4 → CH3Br → C2H6 → CO2 → CO → CH4
Указать условия протекания реакций.
№ 28.2. При сгорании 4,3 г образца алкана выделились 6,72 л СО2 и 6,3 г воды (н.у.). Определить формулу алкана.
№ 28.3. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
СН3−СН3 → СН2=СН2 → СН3−СН2ОН
Указать условия протекания реакций.
№ 28. 4.Сколько граммов 1,6 %-ной бромной воды может обесцветить
1,12 л пропилена при нормальных условиях? (Ответ: 500 г).
№ 28.5.20 г карбида кальция обработали избытком воды, выделившийся ацетилен пропустили через бромную воду, получив 86,5 г
1,1,2,2-тетрабромэтана. Определить выход продукта реакции. (Ответ: 80 %).
№ 28.6.При помощи каких реакций можно различить следующие газы: пропан, пропен и пропин? Написать уравнения реакций.
№ 28.7. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
метан → Х → бензол
Назвать вещество Х. Указать условия протекания реакций.
№ 28. 8. Из 3,36 л ацетилена (условия нормальные) получили 2,5 мл бензола. Определить выход продукта. Плотность бензола равна 0,88 г/мл.
(Ответ: 56,4 %).
№ 28.9. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
CH3−CH2−CH2Br → CH3−CH=CH2 → CH3−CH2Br−CH3
Указать условия протекания реакций.
№ 28.10.Какой объем метана (н.у.) выделится: а) при гидролизе 72 г Al4C3; б) из 4,1 г безводного ацетата натрия? (Ответ: 33,6 л; 1,12 л).
№ 28.11.При помощи каких реакций можно осуществить следующий цикл превращений:
CH4 → CH3Cl → C2H6 → C2H5Cl → C3H8.
№ 28.12.Как, исходя из метана, можно получить бензол? Сколько литров метана (н.у.) необходимо затратить на получение 7,8 г бензола?
(Ответ: 13,4 л).
№ 28.13.Какой объем 90 %-ного раствора азотной кислоты (плотность
1,483 г/мл) потребуется для нитрования бензола, чтобы получилось 24,6 г нитробензола? (Ответ: 9,44 мл).
№ 28.14. Состав соединения выражается формулой С4Н6. Известно, что это вещество легко взаимодействует с бромной водой, не реагирует с аммиачным раствором оксида серебра, но присоединяет воду в присутствии солей ртути (II). Написать структурную формулу соединения и назвать его.
№ 28.15. Написать уравнения реакций, при помощи которых можно осуществить превращения:
Al4C3 → X → Y → Cu2C2.
Назвать соединения Х и Y.
№ 28.16.Алкен нормального строения содержит двойную связь при первом углеродном атоме. 0,7 г этого алкена присоединил 1,6 г брома, Определить формулу алкена и назвать его.
№ 28.17.Углеводород, состав которого выражается формулой С3Н4, взаимодействует с бромной водой и с натрием с выделением водорода. Определить структурную формулу углеводорода и назвать его.
№ 28.18.При сгорании 3,6 г алкана образуется 5,6 л СО2. Какой объем кислорода (н.у.) потребуется для реакции? (Ответ: 8,96 л).
№ 28.19. Органическое вещество содержит углерод (массовая доля 84,21 %) и водород (15,79 %). Плотность паров вещества по воздуху составляет 3,93 (н.у.). Определить формулу этого вещества.
№ 28.20.Массовая доля углерода в углеводороде составляет 83,33 %. Плотность паров углеводорода по водороду равна 36 (н.у.). Определить формулу углеводорода.
Дата добавления: 2015-09-11; просмотров: 3972;
