Вандерваальсові взаємодії
Навіть у межах неполяризованої молекули розподіл електронної щільності є рівномірним лише в разі його усереднення за часом. У кожний момент часу внаслідок флуктуацій щільності виникають локальні неоднорідності, тобто парціальні заряди різного знаку, і молекула являє собою тимчасовий диполь. При наближенні іншої молекули такий тимчасовий диполь першої молекули індукує диполь у межах другої молекули, унаслідок чого виникає притягання електричної природи (рис. 7).
Квантова механіка свідчить, що енергія пари молекул, електронні системи яких поляризовані, є нижчою за енергію пари неполяризованих молекул. У результаті всі молекули та атоми на близьких відстанях притягуються один до одного. Взаємодії такого типу були описані Ван дер Ваальсом (Johannes Van der Waals) і носять його ім’я.
Вандерваальсові взаємодії між неполяризованими молекулами називають дисперсійними; взаємодії між двома поляризованими молекулами (постійними диполями) – орієнтаційними (або диполь-дипольними); між неполяризованою молекулою та постійним диполем індукційними (або взаємодіями типу диполь-індукований диполь).
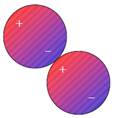
Рис. 7. Взаємодія міжтимчасовими диполями двох молекул.
Основні властивості вандерваальсових взаємодій:
• Вандерваальсові взаємодії, які призводять до притягання на малих відстанях, реалізуються між будь-якими молекулами й атомами незалежно від їхньої природи.
• Вандерваальсові взаємодії є короткодіючими: енергія взаємодій швидко знижується з відстанню між молекулами чи атомами r (пропорційно до 1/r6). Тобто вандерваальсові взаємодії є суттєвими при безпосередньому контакті між молекулами (атомами, хімічними групами).
• Слова безпосередній контакт означають, що існує певна оптимальна величина r0 – відстань, на якій енергія взаємодій є мінімальною. При зниженні r притягання між молекулами змінюється на відштовхування: електронні оболонки різних молекул (уже насичені валентними електронами) не можуть проникати одна в одну (відповідно до принципу заборони Паулі). Величина r0 характеризує розмір кожного атома (вандерваальсів радіус), який використовується при побудові молекулярних моделей (як, наприклад, на рис. 3). Непроникність атомів один для одного (стеричні обмеження) має велике значення для структури біополімерів: серед великої кількості конформацій можливими є лише ті, для яких не спостерігається проникнення однієї частини ланцюга в іншу (два атоми не можуть займати одну область простору).
• Вандерваальсові взаємодії є найслабшими серед усіх нековалентних взаємодій. Для порівняння: величина середньої кінетичної енергії теплового руху RT при 27 °С становить 0,6 ккал/моль; типові значення енергії вандерваальсових взаємодій (на відстані r0) варіюють у межах 0,1 – 0,5 ккал/моль. Останнє твердження потребує уточнення стосовно макромолекул. Коли взаємодіють досить великі поверхні, між якими реалізується велика кількість міжатомних контактів, вандерваальсові взаємодії стають суттєвим фактором стабілізації структури макромолекул і макромолекулярних комплексів. Для того, щоб таких контактів було справді багато (щоб не було пустот), дві поверхні повинні добре відповідати одна одній (як ключ до замка) – бути просторово комплементарними. Просторова комплементарність між поверхнями макромолекул є одним із важливих механізмів специфічної взаємодії між ними.
Дата добавления: 2015-09-11; просмотров: 1269;
