Уравнение Лайнуивера-Берка
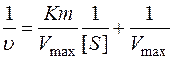
 Y = Kx + b
Y = Kx + b
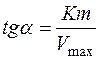
Km - это характеристика фермента, чем больше Km, тем менее чувствителен фермент к данному субстрату.
Например, фермент каталаза расщепляет перекись водорода на воду и кислород, константа для него 25 ммолей.
Гексакиназа мозга, под действием этого фермента происходит

 Скорость активности фермента в зависимости от концентрации фермента – обычная линейная зависимость. Чем больше концентрация, тем больше скорость реакции.
Скорость активности фермента в зависимости от концентрации фермента – обычная линейная зависимость. Чем больше концентрация, тем больше скорость реакции.
По международному соглашению за единицу активности фермента принимается такое количество фермента, которое катализирует превращение одного микромоля субстрата в минуту при 25 градусов при оптимальных значения Ph..
Число оборотов фермента – число молекул субстрата претерпевающих превращение в единицу времени в расчете на 1 молекулу фермента. Пример: карбонатдегидратаза – это фермент, который работает в эритроцитах и является одним из наиболее активных ферментов, его число оборотов 36 млн. в минуту.
CO2 + H2O = H2CO3
Ингибирование ферментов.Действие многих ферментов моно подавлять определенными химическими реагентами. Изучение ингибиторов ферментов является предметом изучения науки токсикологии. Механизм действия некоторых лекарственных препаратов состоит в том, что они ингибируют определенные ферменты в клетках.
Рассматривают два типа ингибирования:
1. Обратимое ингибирование.
2. Необратимое ингибирование. Пример: химический препарат диизопропилфторфосфат, это вещество влияет на ферменты эстеразной активности. Самым первым на поверхности является фермент ацетилхолинэстераза.
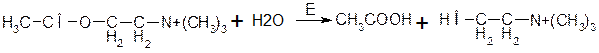
Под действием фермента расщепляют ацетилхолин на уксусную кислоту и холин. Ацетилхолин является медиатором нервных импульсов. Активный центр необратимо связывается с ингибитором.

Дата добавления: 2015-08-20; просмотров: 1887;
