Адсорбция. Изотерма адсорбции. Уравнение Гиббса.
ПН растворов обычно отличается от ПН растворителя.
Растворенное вещество может не изменять  , повышать и понижать его.
, повышать и понижать его.
Поверхностная свободная энергия стремится к минимуму, поэтому при повышении  вещество будет удаляться с поверхности внутрь жидкости. Полному удалению молекул растворенного вещества с поверхности препятствует тепловое движение, под действием которого вещество стремится к равномерному распределению в объеме.
вещество будет удаляться с поверхности внутрь жидкости. Полному удалению молекул растворенного вещества с поверхности препятствует тепловое движение, под действием которого вещество стремится к равномерному распределению в объеме.
Под влиянием этих двух факторов устанавливается равновесие, в результате которого концентрация вещества в поверхностном слое уменьшается по сравнению с концентрацией в объеме.
Если растворенное вещество снижает 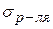 , то концентрация его в поверхностном слое увеличивается.
, то концентрация его в поверхностном слое увеличивается.
Самопроизвольное изменение концентрации вещества в поверхностном слое, отнесенное к единице поверхности, называется адсорбцией, обозначается через Г и выражается в кмоль/м2, или моль/см2.
Если Г>0 адсорбцию называют положительной, если Г<0 - отрицательной.
Если растворенное вещество не изменяет 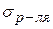 , адсорбция Г=0 и вещество равномерно распределено между поверхностным слоем и объемом.
, адсорбция Г=0 и вещество равномерно распределено между поверхностным слоем и объемом.
Простое термодинамическое соотношение между поверхностной концентрацией Г и изменением ПН с активной концентрацией растворяемого вещества 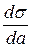 было выведено Гиббсом:
было выведено Гиббсом:

где  - активность раствора;
- активность раствора;
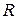 - универсальная газовая постоянная;
- универсальная газовая постоянная;
 - абсолютная температура.
- абсолютная температура.
Для разбавленных растворов активность заменяют концентрацией С:
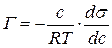
Из уравнения следует, что только те вещества показывают положительную адсорбцию, с повышением концентрации которых ПН понижается, 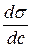 <0.
<0.
Если 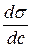 >0, концентрация растворенного вещества в поверхностном слое будет уменьшаться: Г<0.
>0, концентрация растворенного вещества в поверхностном слое будет уменьшаться: Г<0.
Вещества, повышающие ПН, называются отрицательно поверхностно-активными веществами (инактивными, ими являются неорганические соли).
Вещества, понижающие ПН называют поверхностно-активными (ПАВ) (см. стр. 98-102).
К ПАВ относятся органические вещества, молекулы которых построены из участков с резко различающимися свойствами. Одна часть молекулы полярная, другая – неполярная (углеводородный радикал).
Полярная: -OH, -COOH, -SO3Na, -SO3H, -NH2, -SO2H.
Полярная часть гидрофильна, неполярная – гидрофобна.
ПАВ характеризуются величиной ГЛБ (гидрофильно-липофильного баланса).
Величина 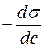 , согласно Ребиндеру, является мерой способности вещества понижать поверхностную энергию, она называется поверхностной активностью и обозначается
, согласно Ребиндеру, является мерой способности вещества понижать поверхностную энергию, она называется поверхностной активностью и обозначается  . Ее размерность – Н/м.
. Ее размерность – Н/м.
В гомологическом ряду жирных кислот, спиртов и аминов понижение  тем больше, чем длиннее цепь.
тем больше, чем длиннее цепь.
Согласно правилу Дюкло-Траубе, при удлинении цепи на группу СН2 поверхностная активность  возрастает на границе раствор-воздух в 3-3,5 раз.
возрастает на границе раствор-воздух в 3-3,5 раз.
Для определения этой характеристики строят зависимость  . Используя уравнение Гиббса, строят зависимость
. Используя уравнение Гиббса, строят зависимость  .
.
Дата добавления: 2015-08-08; просмотров: 2520;
