Трансформация азотсодержащих веществ
Важнейшим минеральным элементом является азот. Ведущая роль в процессах трансформации азотсодержащих соединений принадлежит микроорганизмам. Цикл трансформации азотсодержащих веществ осуществляется рядом взаимосвязанных процессов.
Аммонификация – процесс минерализации органических азотсодержащих веществ, сопровождающийся выделением аммиака. Ведут его различные группы микроорганизмов. В процессе жизнедеятельности микроорганизмов часть наиболее сложных органических азотсодержащих веществ запасается в почве в виде гумуса. Аммонификация является принципиально важным процессом в цикле трансформации азота, в результате которого наша планета очищается от продуктов растительного, животного и микробного происхождения.
Нитрификация – процесс окисления аммиака до нитритов и нитратов. Осуществляют этот процесс нитрифицирующие бактерии в строго аэробных условиях.
Денитрификация – процесс восстановления нитритов и нитратов денитрифицирующими бактериями до свободного азота. Этот процесс вреден для сельского хозяйства, так как приводит к частичному выносу (приблизительно 20%) азота из почвы.
Биологическая фиксация молекулярного азота включает процессы фиксации молекулярного азота атмосферы свободноживущими и симбиотическими формами микроорганизмов путем биологического восстановления до аммиака.
Биологическая азотфиксация является самым значительным путем пополнения запасов азота в почве. Подсчитано, что глобальная азотфиксация в водных системах ежегодно достигает 190 млн. тонн азота, а на суше она составляет 130 млн. тонн, в то время как мировое производство азотных удобрений пока не превышает 60–70 млн. тонн.
Аммонификация. Разнообразные органические азотсодержащие соединения составляют до 99% всего запаса азота. Первое место среди них занимают белки, на долю которых приходится не менее 50% от органических азотсодержащих соединений.
Процесс аммонификации белков заключается в деятельности аммонифицирующих бактерий, которые выделяют в среду протеолитические экзоферменты, катализирующие расщепление пептидных связей в молекулах белков с образованием более мелких осколков полипептидов и олигопептидов. Последние относительно легко проникают через цитоплазматическую мембрану в бактериальную клетку, где расщепляются внутриклеточными ферментами пептидазами до аминокислот. Образующиеся аминокислоты непосредственно включаются в биосинтетические процессы микробной клетки либо служат одним из основных субстратов для процессов катаболизма.
Разрушение аминокислот начинается с их дезаминирования, т.е. с отщепления аминогруппы от молекулы аминокислоты, что приводит к выделению аммиака. Процесс дезаминирования аминокислот происходит различными путями.
Наиболее часто наблюдается окислительное дезаминирование аминокислот при участии молекулярного кислорода:
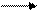 R—CHNH2—COOH + 1/202 R—CO-COOH + МНз
R—CHNH2—COOH + 1/202 R—CO-COOH + МНз
Нередко окислительное дезаминирование аминокислот сопровождается декарбоксилированием:
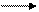 R—CHNH2—COOH + О2 R—COOH + С02 + NH3
R—CHNH2—COOH + О2 R—COOH + С02 + NH3
Многие аминокислоты подвергаются гидролитическому (в присутствии воды) дезаминированию с помощью НАД-зависимых дегидрогеназ:
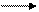 R-CHNH2-COOH + НАД + +H2O R-CO-COOH + НАД • Н + NH3
R-CHNH2-COOH + НАД + +H2O R-CO-COOH + НАД • Н + NH3
Дальнейшая судьба углеродсодержащих продуктов процесса дезаминирования аминокислот может быть различна. Некоторые из них, такие, как пировиноградная, а-кетоглутаровая, щавелево-уксусная кислоты непосредственно включаются в процессы клеточного метаболизма, остальные (большинство органических кислот) подвергаются последующей трансформации.
В аэробных условиях процесс дезаминирования аминокислот идет, как правило, энергично и завершается окислением углеродного остатка до конечных продуктов – углекислого газа, воды и сульфатов.
В анаэробных условиях некоторые аминокислоты подвергаются декарбоксилнрованию с образованием СО2 и первичных аминов. К числу последних относятся высокотоксичные соединения кадаверин, путресцин и агматин, известные под названием трупных ядов.
Анаэробное сбраживание аминокислот сопровождается накоплением в среде специфических веществ с резким неприятным запахом – аммиака, сероводорода, индола и скатола. Поэтому в быту процесс анаэробной аммонификации белков получил название гниения.
В процессе аммонификации белков принимают участие различные группы микроорганизмов, постепенно сменяющие друг друга. В аэробных условиях аммонификацию белков начиняют неспорообразующие бактерии, относящиеся к родам Micrococcus, Arthrobacter, Pseudomonas, Proteus, а также микобактерии (Mycobacterium) и плесневые грибы. На смену им приходят различные виды бацилл (Bacillus subtilis, Вас. megaterium, Вас. mycoides и др.). На завершающих этапах в процесс аэробной аммонификации включаются актнномицеты. В анаэробных условиях процесс аммонификации ведут бактерии рода Clostridium (Cl.cadaveris, Cl. paraputrificum и др.). Аммонификация сложных белков включает первоначальное расщепление молекул на основные компоненты – белок и простетическую группу. Дальнейшая аммонификация белков осуществляется по обычной схеме.
Сложными полимерными соединениями являются нуклеиновые кислоты – ДНК и РНК. Аммонификация нуклеиновых кислот начинается с гидролитического расщепления их на мононуклеотиды при участии ферментов рибонуклеазы и дезоксирибонуклеазы. Далее от мононуклеотида отщепляется сначала остаток фосфорной кислоты, затем сахар. Образовавшиеся азотсодержащие основания разлагаются до мочевины и аминокислот, а последние в конечном итоге до аммиака и органических кислот. Отщепленные от мононуклеотидов сахара в аэробных условиях окисляются до конечных продуктов углекислого газа и воды, а в анаэробных условиях подвергаются медленному сбраживанию.
Дезаминированию могут подвергаться и органические азотсодержащие вещества небелковой природы, такие, как мочевина, мочевая и гиппуровая кислоты, входящие в состав мочи человека и животных. Мочевина является одним из продуктов жизнедеятельности грибов и образуется при гидролитическом распаде аргинина. Многие микроорганизмы способны использовать мочевину в качестве источника азота для синтеза собственных белков.
Под действием фермента уреазы, выделяемой микроорганизмами, происходит гидролиз мочевины с. образованием углекислого аммония, который почти тотчас же разлагается на составные компоненты – аммиак, углекислый газ и воду.
Бактерии, разлагающие мочевину, получили название уробактерий. К ним относятся Sporosarcina ureae, Micrococcus ureae и Bacillus pasteurii. Специфической чертой уробактерий является их способность развиваться в щелочной среде. Мочевая и гиппуровая кислоты также разрушаются рядом микроорганизмов в процессе реакций их энергетического метаболизма.
Нитрификация. Аммиак, образующийся в процессе аммонификации в почве и воде, сравнительно быстро окисляется нитрифицирующими бактериями до нитритов и нитратов. О микробиологической природе процесса нитрификации впервые высказал предположение Л. Пастер. Позднее, в 1890–1892 гг., С.Н. Виноградский выделил нитрифицирующие бактерии в чистую культуру и показал, что процесс нитрификации протекает в две фазы. Первую фазу нитрификации – окисление аммиака или солей аммония до нитритов – ведут нитрозные бактерии, относящиеся к родам Nitrosomonas, Nitrosococcus, Nitrosolobus, Nitrosospira.
Из нитрозных бактерий наиболее подробно изучен вид Nitrоsomonas europaea. Клетки его имеют форму коротких палочек, размером 1,0–
1,5 мкм; подвижные или неподвижные, одиночные либо в коротких цепочках. В настоящее время предполагается, что первая фаза нитрификации включает несколько этапов. Очевидно, на первом этапе аммиак окисляется до гидроксиламина при участии фермента монооксигеназы, катализирующей присоединение к молекуле аммиака одного атома кислорода:
МН3 + О2 + НАД • Н2 -> NН2ОН + Н2О + НАД+
Далее гидроксиламин под действием фермента гидроксиламиноксидоредуктазы окисляется до нитрита через промежуточный продукт – нитроксил.
Энергия, освобожденная в реакциях окисления и аккумулированная клеткой в АТФ, расходуется для фиксации СО2 и других биосинтетических процессов. Вторую фазу нитрификации – окисление нитритов в нитраты – осуществляют нитратные бактерии родов Nitrobacter, Nitrospira, Nitrococcus. Лучше других нитратных бактерий изучен Nitrobacter winogradskyi, клетки которого имеют грушевидную форму. Размножается почкованием, дочерняя клетка, имеющая один латерально расположенный жгутик, обычно подвижна.
Все нитрифицирующие бактерии – облигатные аэробы. Большинство из них хемолитоавтотрофы. Присутствие органических веществ в среде, в концентрациях, обычных для гетеротрофов, ингибирует рост нитрифицирующих бактерий. Наилучшим образом нитрифицирующие бактерии развиваются при температуре 25–30 °С и рН 7,5–8,0. Они обитают во всех типах почв, в морской и пресной воде озер, морей и океанов.
Нитрификация – второе важное звено в цикле трансформации азотсодержащих веществ. Нитраты служат одной из форм минерального азота, необходимого для питания растений. Накопление нитритов и нитратов в почве вызывает подкисление почвенного раствора, что положительно сказывается на повышении растворимости некоторых соединений фосфора и железа и способствует лучшему усвоению их растениями.
Денитрификация. Нитраты в почве расходуются весьма интенсивно. Часть их потребляется в процессе питания растений и самих микроорганизмов, часть вымывается из почвы, а некоторое количество нитратов восстанавливается до газообразной формы азота в процессе денитрификации.
Следует различать денитрификацию прямую и косвенную. Под прямой денитрификацней принято понимать биологическое восстановление нитратов и нитритов, осуществляемое микроорганизмами. Косвенная денитрификация – это чисто химический процесс взаимодействия нитритов с аминокислотами, в результате которого образуется молекулярный азот. Косвенная денитрификацня характерна для кислых почв при рН среды ниже 5,5.
В природе более распространена прямая денитрификация. Она подразделяется на ассимиляционную и диссимиляционную. При ассимиляционной денитрификацин нитраты потребляются в качестве источника азота и восстанавливаются до аммиака, который расходуется клеткой в процессе биосинтеза. К ассимиляционной денитрификацни способны растения и многие бактерии. В процессе диссимиляционной денитрнфикации нитраты и нитриты выступают в роли акцепторов электронов в реакциях катаболизма денитрифицирующих бактерий. Диссимиляционную денитрификацию ведут хемоорганогетеротрофные бактерии, относящиеся к родам Pseudomonas, Bacillus, Corynebacterium и др.
В зависимости от вида микроорганизма, ведущего процесс, конечными продуктами восстановления нитратов являются молекулярный азот, оксид азота (I) или оксид азота (II).
Клетки денитрифицирующих бактерий имеют достаточно совершенную дыхательную цепь, позволяющую им вести процессы катаболизма как в аэробных, так и в анаэробных условиях. Одними из важных ферментов денитрифицирующих бактерий являются нитратредуктазы, катализирующие перенос электронов па азот нитратов. Синтез нитратредуктаз в клетке происходит только в анаэробных условиях при наличии нитратов в среде.
В природе денитрифицирующие бактерии, а соответственно и процессы денитрификации, широко распространены. Денитрифицирующие бактерии обитают в пресных и соленых водоемах, в различных типах почв. Из всех видов денитрификации основной ущерб сельскому хозяйству наносит диссимиляционная денитрификация, так как именно она в основном и приводит к снижению запасов азота в почве и в водоемах. Подсчитано, что потери азотных удобрений, вносимых в почву, в результате денитрификации нередко составляют от 5 до 10%. Особо активно денитрификация протекает на тяжелых, сильно переувлажненных почвах. Для борьбы с денитрификацией рекомендуется рыхление почвы в целях создания аэробных условий жизни денитрифицирующим бактериям.
Биологическая фиксация молекулярного азота. Интерес к проблеме биологической фиксации молекулярного азота атмосферы обусловлен существенной ролью биологического азота в азотном балансе биосферы. Решение этой проблемы перспективно в плане получения дешевого и совершенно безвредного для здоровья человека и окружающей среды биологического азота для обеспечения нужд сельского хозяйства.
Запасы минерального азота в почве невелики и в среднем составляют 150 кг на 1 га пахотного слоя. Запасы молекулярного азота в атмосфере практически неисчерпаемы. Над каждым гектаром почвы содержится такой запас азота, который мог бы обеспечить высокие урожаи растений в течение миллионов лет. Однако молекулярный азот не может быть использован ни растительными, ни животными организмами. Азотфиксация – это уникальный процесс, характерный только для прокариотной клетки. Среди царства прокариот способны фиксировать молекулярный азот различные аэробные и анаэробные бактерии и некоторые актиномицеты. Все азотфиксирующие микроорганизмы условно можно подразделить на две группы: свободноживущие в почве и симбиотические, вступающие в симбиоз с высшими растениями. Согласно подсчетам ежегодно культурные растения земного шара выносят из почвы около 100 млн. т азота, в то время как вносимые в почву минеральные удобрения составляют лишь 32 млн. т. Остальной дефицит азота в почве восполняется за счет биологической азотфиксации. В земледелии нашей страны при возрастающих поставках минеральных удобрений велика роль биологического азота. Подсчитано, что свободноживущие азотфиксирующие микроорганизмы фиксируют по 15–18 кг азота на 1 га.
Молекулярный азот весьма инертное соединение. Тройная связь, связываюшая атомы азота, требует для разрыва огромной энергии. Осуществить разрыв связи могут микроорганизмы, содержащие ферментативный нитрогеназный комплекс. Первый компонент – молибдоферродоксин, вещество белковой природы. Второй компонент – азоферродоксин. Фермент функционирует при наличии АТФ, ионов магния, восстановителя-ферродоксина.
Восстановление молекулярного азота идет поэтапно, через стадии образования диимина, гидразина, и в конечном итоге, аммиака.
Для восстановления одной молекулы азота затрачивается 12 молекул АТФ, поступающих из метаболизма клетки бактерии или растения-симбионта. Аммиак вступает в реакции с органическими кетокислотами, образуя аминокислоты, идущие на построение белков бактерий и растений.
Дата добавления: 2015-08-14; просмотров: 3527;
