Строение многоэлектронных атомов.
Рассмотрим атом в невозбужденном состоянии. Состояние каждого электрона этой системы описывается квантовыми числами 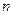 ,
, 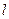 ,
, 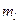 и
и 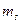 . Казалось бы, что электронам энергетически более выгоден самый нижний уровень. И с этой точки зрения (минимум энергии) все электроны в атоме должны были бы разместиться на самом нижнем из разрешенных уровней. Однако этого не происходит. Электроны в атомах распределяются по состояниям в определенном порядке в соответствии с принципом Паули, т.е. в каждом состоянии может находиться не более одной частицы с полуцелым спином.
. Казалось бы, что электронам энергетически более выгоден самый нижний уровень. И с этой точки зрения (минимум энергии) все электроны в атоме должны были бы разместиться на самом нижнем из разрешенных уровней. Однако этого не происходит. Электроны в атомах распределяются по состояниям в определенном порядке в соответствии с принципом Паули, т.е. в каждом состоянии может находиться не более одной частицы с полуцелым спином.
Энергия электрона определяется главным образом числами 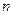 и
и 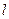 . Совокупность электронов с одинаковым
. Совокупность электронов с одинаковым 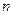 образует оболочку (оболочки принято обозначать буквами
образует оболочку (оболочки принято обозначать буквами 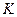 ,
, 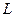 ,
, 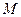 ,
, 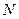 ,
, 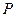 и т.д.). Число электронных состояний (уровней) в оболочке с учетом спина равно кратности вырождения, т.е. равно
и т.д.). Число электронных состояний (уровней) в оболочке с учетом спина равно кратности вырождения, т.е. равно 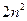 . Оболочки подразделяются на подоболочки, отличающиеся значением числа
. Оболочки подразделяются на подоболочки, отличающиеся значением числа 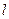 .
.
Как же заполняются электронные оболочки атомов?
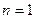 (
( 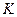 -оболочка);
-оболочка); 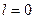 (
( 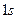 -состояние);
-состояние); 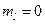 ;
; 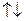 2 электрона; форма облака – сфера.
2 электрона; форма облака – сфера.
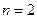 (
( 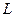 -оболочка);
-оболочка); 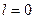 (
( 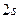 -состояние);
-состояние); 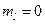 ;
; 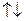
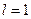 (
( 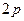 -состояние);
-состояние); 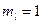 ;
; 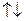 8 электронов
8 электронов
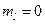 ;
; 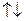
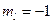 ;
; 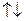
форма облака – 3 гантели, ориентированные в 3-х взаимноперпендикулярных направлениях.
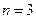 (
( 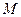 -оболочка);
-оболочка); 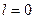 (
( 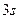 -состояние);
-состояние); 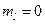 ;
; 
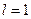 (
( 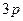 -состояние);
-состояние); 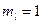 ;
; 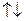 8 электронов
8 электронов
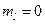 ;
; 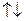
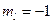 ;
; 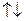
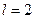 (
( 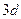 -состояние);
-состояние); 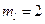 ;
; 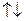
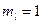 ;
; 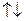
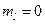 ;
; 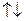 18 электронов
18 электронов
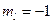 ;
; 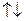
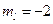 ;
; 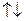
Символы 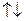 наглядно обозначают
наглядно обозначают 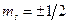 .
.
Дата добавления: 2015-08-14; просмотров: 743;
