Микрогетерогенные дисперсные системы.
Учебные вопросы:
1) Системы с газообразной дисперсионной средой – аэрозоли.
2) Пены, эмульсии и суспензии – системы с жидкой дисперсионной средой.
К микрогетерогенным дисперсным системам относятся эмульсии, суспензии, пены и аэрозоли.
Эмульсии – микрогетерогенные системы, по агрегатному состоянию фаз обозначаемые как «ж/ж». Они образованы двумя взаимно несмешивающимися жидкостями, одна из которых в виде капель раздроблена в другой.
Классифицируют эмульсии по характеру дисперсной фазы и дисперсионной среды или по концентрации дисперсной фазы в системе.
Согласно первой классификации различают в зависимости от полярности фаз два типа эмульсий: прямая эмульсия, обозначаемая как «м/в» и обратная эмульсия, которую записывают как «в/м». Полярную фазу называют «водой» (обозначают буквой «в»), а неполярную - «маслом» (обозначают буквой «м»). Определить тип эмульсии можно тремя методами по свойствам дисперсионной среды:
- методом слияния капель (на часовое стекло наносятся по одной капле эмульсии, дисперсной фазы и дисперсионной среды, после чего стекло наклоняют и проверяют с какой из капель сливается капля эмульсии);
- методом окрашивания капель (к двум каплям эмульсии добавляют по капле красителей, окрашивающих разные фазы и наблюдают в микроскоп, какая из фаз окрасилась);
- по электропроводности (в прямой эмульсии дисперсионная среда – вода – обладает хорошей электропроводностью по сравнению с маслом).
Специфическим свойством эмульсий является обращение фаз, означающее обратимый переход из одного типа в другой. Это явление может быть вызвано механическим воздействием (встряхиванием) или заменой стабилизатора эмульсии, называемого эмульгатором.
Согласно второй классификации различают разбавленные (0,1% об. д.ф.), концентрированные (74% об. д.ф.) и высококонцентрированные (более 74%. д.ф.) эмульсии.
Разбавленные эмульсии имеют размер капелек порядка 10-7м, т.е. высокую степень дисперсности, и образуются без специальных эмульгаторов. Частицы таких эмульсий, как и коллоидные частицы, несут электрический заряд в результате адсорбции ионов неорганических электролитов, всегда имеющихся в жидкой среде, или ионов Н+ и ОН-, образованных при диссоциации молекул воды. Кроме заряда, агрегативной устойчивости разбавленных эмульсий способствует и тот факт, что при малой концентрации столкновения частиц очень редки.
|
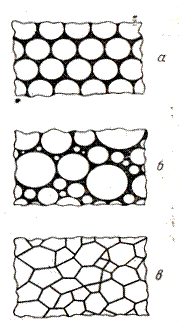
Концентрированные эмульсии получают методом диспергирования, размер их капелек велик и составляет 0,1 – 1 микрон. Эти капельки видны в обычный микроскоп (рис. 38, а и б). Они совершают броуновское движение и легко седиментируют. Агрегативная устойчивость концентрированных эмульсий определяется природой эмульгатора.
Отличительной особенностью высококонцентрированных эмульсий является взаимная деформация капель дисперсной фазы, которые приобретают форму многогранников, разделенных тонкими пленками – прослойками дисперсионной среды (см. рис. 38, в). Вследствие такой «сотообразной» структуры капельки не способны к седиментации и обладают свойствами гелей (их можно резать ножом).
 Природа эмульгатора определяет не только устойчивость, но и тип эмульсии. В качестве эмульгаторов используют обычно поверхностно-активные вещества (ПАВ): мыла, ВМС, поливиниловый спирт, метилцеллюлозу. Молекулы таких веществ содержат в своем составе две функциональные группы: одну – полярную, называемую «головой», другую – неполярную, называемую «хвостом». Условно такую молекулу можно изобразить так:
Природа эмульгатора определяет не только устойчивость, но и тип эмульсии. В качестве эмульгаторов используют обычно поверхностно-активные вещества (ПАВ): мыла, ВМС, поливиниловый спирт, метилцеллюлозу. Молекулы таких веществ содержат в своем составе две функциональные группы: одну – полярную, называемую «головой», другую – неполярную, называемую «хвостом». Условно такую молекулу можно изобразить так:
На рис. 39 показано, как молекулы ПАВ, ориентируясь своими полярными головами к частицам полярной фазы эмульсии, создают вокруг их оболочки и не дают им слипаться.

Рис. 39. Стабилизация частиц эмульсии молекулами ПАВ:
а – масло в воде; б – вода в масле
Твердыми эмульгаторами могут быть порошки, способные избирательно смачиваться полярной или неполярной жидкостями, из которых образована эмульсия (сажа, глина, гипс). В зависимости от своей природы твердый эмульгатор может стабилизировать прямую или обратную эмульсию, как показано на рис. 40.
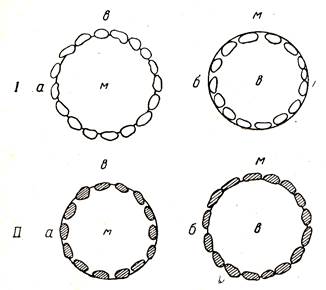
Рис. 40. Расположение частиц твердого эмульгатора у межфазной
поверхности капелек эмульсии:
I – гидрофильный эмульгатор (глина); II - гидрофобный эмульгатор (сажа)
Практическое значение эмульсий велико как в природе, так и в технике. Примерами природных эмульсий являются молоко, состоящее из капелек жира, распределенных в воде, яичный желток, латекс (млечный сок) натурального каучука, нефть. Самопроизвольное эмульгирование играет важную роль в биологических процессах усвоения и переваривания пищи. Эмульсии применяют в технике в качестве смазочноохлаждающих жидкостей (СОЖ). В сельском хозяйстве в виде эмульсий применяют средства борьбы с вредителями растений, в строительстве эмульсии битумов в воде применяют при ремонте дорог. В пищевой промышленности получают майонез, маргарин и др.
Нежелательно образование эмульсий при добыче нефти. Авторемонтные предприятия сбрасывают в сутки от 30 до 100 м3 сочных вод, содержащих масляные эмульсии, для разрушения которых применяют деэмульгирование. Разрушение эмульсий может быть достигнуто введением в систему ПАВ – веществ, вытесняющих эмульгатор из адсорбционного слоя, но неспособного стабилизировать эмульсию. Также можно разрушить эмульсию центрифугированием, фильтрованием, нагревом.
Суспензии – микрогетерогенные системы, соответствующие типу «т/ж». Разбавленные суспензии называют взвесями, к ним относится кровь (биологическая жидкость), применяемые в технике строительные (цементные, известковые) растворы и краски. Взвеси устойчивы только со стабилизаторами, роль которых могут выполнять порошки или ПАВ. Концентрированные суспензии называют пастами. В технике применяют абразивные пасты, в строительстве используют грунтовки, щпатлевки, мастики, краски. Концентрированные суспензии относятся к структурированным системам и являются устойчивыми.
Пены – грубодисперсные высококонцентрированные системы, представляющие собой дисперсии газов (обычно воздуха) в жидкой (жидкие пены) или твердой (твердые пены) дисперсионной среде. Примером природной твердой пены является пемза – продукт вулканической деятельности, искусственных твердых пен – хлеб, пенопласт, поролон.
Пузырьки газов имеют размер порядка нескольких миллиметров или сантиметров и хорошо видны невооруженным глазом. Благодаря высокой концентрации газовой фазы пузырьки теряют сферическую форму и представляют собой полиэдрические ячейки сотообразной структуры, стенки которых состоят из тонких структурированных пленок дисперсионной среды. От типичных высококонцентрированных пен отличаются низкоконцентрированные системы типа г/ж, в которых отдельные газовые пузырьки отдалены друг от друга на большие расстояния. Примером таких систем являются пиво, газированная вода, шипучие напитки. Благодаря большой разнице в плотностях жидкой и газовой фаз, такие системы имеют низкую седиментационную устойчивость и малое время жизни.
Получают жидкие пены диспергированием газов в жидкости в присутствии стабилизатора, называемого пенообразователем. Природа и количество пенообразователя, концентрирующегося при адсорбции на межфазной поверхности, определяют свойства пленочного каркаса (прочность и продолжительность существования или время жизни). Хорошими пенообразователями водных пен являются поверхностно-активные вещества (ПАВ): спирты, жирные кислоты и их соли – мыла, белки.
Методом конденсации получаются пены при химических реакциях, сопровождающихся выделением газов:
o в огнетушителях NaHCO3 + HCl = NaCl + H2O + CO2;
o при выпечке хлеба (NH4)2 CO3 = 2 NH3 + H2O + CO2;
o при изготовлении пенобетона 2Al + Ca(OH)2 + 2H2O = CaHAlO3 + 3H2.
К свойствам пены относится кратность − отношение объема полученной пены к объему жидкости, из которой она образована. Кратность хорошей пены может достигать 1000 единиц. Агрегативная устойчивость пены определяется временем с момента образования до полного ее разрушения. Она зависит от природы пенообразователя, температуры и вязкости дисперсионной среды. Разрушение пузырьков пены происходит вследствие стекания жидкости в пленках пены, поэтому роль пенообразователя сводится к замедлению стекания жидкости. Наиболее устойчивые пены со временем жизни более 20 с образуются при некоторой оптимальной концентрации спиртов и кислот и средней длине углеводородного радикала. Мыла дают более устойчивые пены в связи с наличием в их молекулах ионогенной группы. Для высокомолекулярных пенообразователей время жизни составляет тысячи секунд, и оно тем выше, чем выше концентрация высокомолекулярного пенообразователя. Повышение температуры вызывает десорбцию пенообразователя с межфазной поверхности и понижение вязкости дисперсионной среды, что приводит к быстрому разрушению пены.
Пены имеют большое практическое значение. Они используются для обогащения руд металлов методом флотации, при стирке и пожаротушении. Иногда явление пенообразования является нежелательным. Оно может также препятствовать перемешиванию при очистке сточных вод или в каких–либо технологических процессах. В этих случаях пены «гасят», добавляя специальные вещества – пеногасители, вытесняющие пенообразователь. Хорошими пеногасителями являются некоторые органические спирты.
Аэрозоли – это микрогетерогенные (или высокодисперсные) системы с газообразной дисперсионной средой, обозначаемые как ж/г или т/г. Название аэрозолей зависит от способа получения.
Полученные методом диспергирования капелек жидкости в газообразной среде аэрозоли называются «спреями», к ним относятся косметические средства (духи, дезодоранты), лекарства. При диспергировании твердых частиц горных пород в воздухе образуется пыль, разносимая ветром на огромные расстояния. Аэрозоли, таким образом, играют важную роль в круговороте химических элементов в природе.
Методом конденсации капелек влаги в воздухе получаются облака и туманы, а при конденсации твердых частичек углерода – дымы.
Аэрозоли устойчивы без стабилизатора по причине изоляционных свойств газообразной среды, не дающей слипаться рассеянным частицам, даже в том случае, если они заряжены. С коллоидными системами аэрозоли объединяет проявление светорассеивания (опалесценции). Специфическое свойство аэрозолей – явление термофореза (перемещение частиц аэрозоля от горячего к более холодному участку), вызванное большей интенсивностью ударов со стороны молекул газообразной среды на участках с повышенной температурой. Образующийся в атмосфере крупных промышленных городов, смог представляет собой аэрозоль сложного состава, состоящий из частиц твердой, жидкой и газообразной фаз, рассеянных в воздухе и обозначаемый как «т, ж, г / г».
Выводы:
1. Примером систем с более низкой, по сравнению с коллоидными, степенью дисперсности являются суспензии, эмульсии, пены и аэрозоли..
2. В отличие от коллоидных систем, микрогетерогенные системы не обладают кинетической устойчивостью, для чего в них вводят стабилизаторы (ПАВ).
3. Практическое значение таких систем в природе и технике велико.
Контрольные вопросы:
1. Перечислите способы получения эмульсий. Какие природные эмульсии вы можете назвать? К какому типу они относятся?
2. Опишите метод пенной флотации. Где он находит применение?
3. Какими количественными величинами характеризуются пены? В каких случаях пены − нежелательное явление?
4. Какими специфическими свойствами обладают аэрозоли? Почему они определяют климат на планете?
5. Охарактеризуйте оптические свойства суспензий. Приведите примеры суспензий. Где они находят применение?
Литература:
1. Глинка, Н.Л. Общая химия: учеб. пособие для вузов / Н.Л. Глинка. – М.: Интеграл-Пресс, 2002. – гл. IХ, с. 295 − 302.
2. Коровин, Н.В. Общая химия: учеб. для технич. направл. и спец.
вузов / Н.В. Коровин. – М.: Высшая школа, 2006. – § 8.7, с. 242
− 251.
| <== предыдущая лекция | | | следующая лекция ==> |
| Лекция № 35 | | | Лекция № 23 |
Дата добавления: 2015-08-14; просмотров: 5370;
