Аминокислоты, пептиды и белки.
Аминокислоты – гетерофункциональные соединения, содержащие старшую карбоксильную группу (–СООН) и аминогруппу (–NH2). По положению NH2–группы относительно СООН–группы различают a–, b–, g–кислоты. Пептиды и белки организма состоят только из a–аминокислот, в молекулах которых обе функции находятся при одном и том же атоме углерода.

Общий фрагмент
 |
 a
a

 Основная функция NH2–СН–СООН Кислотная функция
Основная функция NH2–СН–СООН Кислотная функция
 R Радикал
R Радикал
Названия a–аминокислот строятся по заместительной номенклатуре, но обычно используются их тривиальные названия, чаще связанные с источником выделения.
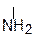 НООС – СН2 – СН – СООН 2-аминобутандиовая кислота, аспарагиновая кислота
НООС – СН2 – СН – СООН 2-аминобутандиовая кислота, аспарагиновая кислота
выделена из спаржи (от лат. asparagus - спаржа).
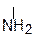 НО – СН2 – СН – СООН 2-амино-3-гидроксипропановая кислота, серин входит в
НО – СН2 – СН – СООН 2-амино-3-гидроксипропановая кислота, серин входит в
состав фиброина шелка (от лат. serieus – шелковистый).
Для записи аминокислотных остатков в макромолекулах пептидов и белков используют трехбуквенные сокращения их тривиальных названий (см. табл. 1).
a–аминокислоты – кристаллические вещества, растворимые в воде. Часть из них обладает сладким вкусом. Основным источником a–аминокислот для живого организма служат пищевые белки. Многие a–аминокислоты синтезируются в организме, некоторые же необходимые для синтеза белков a–аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, треонин, метионин, фенилаланин, триптофан (см. табл. 1).
Таблица 1. Важнейшие a–аминокислоты.

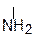 R – CH – COOH
R – CH – COOH
| Строение R | Название | Сокращенное название аминокислотного остатка |
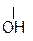 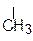 Алифатические
Н –
СН3 –
(СН3)2СН –
(СН3)2СН – СН2 –
СН3 – СН2 – СН –
Содержащие ОН–группу
НО – СН2 –
СН3 – СН –
Содержащие СООН–группу
НООС – СН2 –
НООС – СН2 – СН2 –
Содержащие NH2СО–группу
NH2СО – СН2 –
NH2СО – СН2 – СН2 –
Содержащие NH2-группу
NH2 – (СН2)3 – СН2 –
NH2 – С – NH – (СН2)2 – СН2 –
Серусодержащие
HS – CH2 –
CH3 – S – CH2 – CH2 –
Ароматические
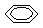
– СН2 –
НО – – СН2 –
Гетероциклические
(полная формула) Алифатические
Н –
СН3 –
(СН3)2СН –
(СН3)2СН – СН2 –
СН3 – СН2 – СН –
Содержащие ОН–группу
НО – СН2 –
СН3 – СН –
Содержащие СООН–группу
НООС – СН2 –
НООС – СН2 – СН2 –
Содержащие NH2СО–группу
NH2СО – СН2 –
NH2СО – СН2 – СН2 –
Содержащие NH2-группу
NH2 – (СН2)3 – СН2 –
NH2 – С – NH – (СН2)2 – СН2 –
Серусодержащие
HS – CH2 –
CH3 – S – CH2 – CH2 –
Ароматические
– СН2 –
НО – – СН2 –
Гетероциклические
(полная формула)
| Глицин Аланин Валин¢ Лейцин¢ Изолейцин¢ Серин Треонин¢ Аспарагиновая Глутаминовая Аспарагин Глутамин Лизин¢ Аргинин Цистеин Метионин¢ Фенилаланин¢ Тирозин Триптофан¢ Гистидин Пролин | Gly Ala Val Leu Ile Ser Thr Asp Glu Asn Gln Lys Arg Cys Met Phe Tyz Trp His Pro |
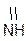
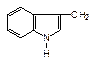
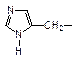
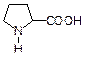
 ¢ Незаменимые a–аминокислоты.
¢ Незаменимые a–аминокислоты.
При некоторых заболеваниях, чаще врожденных, перечень незаменимых кислот расширяется. Например, при кетонурии (слабоумие) не синтезируется организмом тирозин ( у здоровых людей он получается гидроксилированием фенилаланина).
Медико-биологическое значение a–аминокислот заключается в том, что они участвуют в синтезе белков организма. Все многообразие пептидов и белков зависит от состава и различного сочетания a–аминокислот их образующих.
Дата добавления: 2015-08-11; просмотров: 1752;
