Транспортные трансмембранные рецепторные комплексы
Нейромедиаторы в клетку не проникают. Действуя на поверхностные рецепторы, они включают механизмы, обеспечивающие выработку вторичных сигналов (мессенджеров) для запуска в действие внутриклеточных реагирующих структур, сами же высвобождаются из связи с рецепторами и подвергаются разрушению, либо обратному захвату нервным окончанием и реутилизации в нем (Рис.21). Ряд веществ, выполняющих информативную функцию (белково-пептидные, стероидные, тиреоидные и другие гормоны), должны транспортироваться внутрь клетки, так как они проявляют свою лигандную функцию для соответствующих внутриклеточных (цитоплазматических и ядерных) рецепторных комплексов в нативном состоянии. Имеется достаточно большое число веществ, не несущих информативной нагрузки, но используемых клеткой в качестве энергетического и пластического материалов.
Рецепторно-опосредованный перенос химических веществ внутрь клетки получил название интернализации. Суть его заключается в следующем. Клеточная мембрана содержит углубления (ямки), покрытые со стороны цитоплазмы клатрином – белком, фиксирующим рецепторы в мембране. В ямку, двигаясь по мембране, попадают экзорецепторы. При поступлении лиганда (информативные или неинформативные молекулы) на рецепторно-эффекторные комплексы в последних вырабатываются вторичные лиганды, точкой действия которых являются протеинкиназы: цАМФ активирует А-киназу, цГМФ – G-киназу, диацилглицерин – С-киназу, Са2+ - кальмодулинзависимую киназу. Протеинкиназы катализируют перенос фосфатных групп от молекул АТФ к молекулам белка, в том числе рецепторным. Следствием фосфорилирования последних является индукция погружения рецепторов в клетку. При этом возможны два варианта. В одних случаях лиганд, связываясь со своим рецептором, вызывает фосфорилирование других рецепторных белков, нагруженных тем или иным веществом, и индуцирует их быструю интернализацию. В других случаях лиганд вызывает интернализацию своего собственного рецептора (рецепторы инсулина и ряд факторов роста) – лиганд погружается в клетку вместе со своим рецептором.
| Рис.21. Схема организации и функционирования транспортных рецепторов неинформационных молекул: х – холестерин; ▲ – ЛПНП; - рецептор; Р – фосфат; 1 – ЛПНП-рецептор, загруженный комплексом липопротеин-холестерин; 2 – интернализация загруженного рецептора; 3 –отсоединение рецептора от холестерин-ЛПНП; 4 – возвращение рецептора в плазмолемму; 5 – поступление холестерин-ЛПНП в лизосому; 6 – отсоединение ЛПНП от холестерина; 7 – возврат ЛПНП в плазму крови; 8 – внедрение холестерина в плазмолемму; 9 – фосфорилирование рецептора. | 
|
Транспортные трансмембранные рецепторы воспринимают такие лиганды, как липопротеины низкой плотности, кликопротеины, фибрин, кобаламин и др. Характерной особенностью этих рецепторов является циркуляторное движение с поверхности вглубь клетки и обратно. Наиболее изучены в настоящее время рецепторы липопротеинов низкой плотности, которые мы рассмотрим в качестве примера интернализации в клетку неинформативных лигандов.
Рецепторы липопротеинов низкой плотности имеют непосредственное отношение к обмену холестерина, который синтезируется в печени и поступает в плазму крови. В клетку он транспортируется с помощью липопротеинов низкой плотности (ЛПНП), также находящихся в плазме крови. Холестерин (х) соединяется с ЛПНП, в результате чего последний активируется и становится способным к взаимодействию с рецепторами ЛПНП, располагающимися в плазматической мембране. Аминокислотная, последовательность рецепторного белка расшифрована, но еще нет сведений о его пространственной организации, как это сделано в отношение Н-холинорецепторов. Можно предполагать, что эти рецепторы представляют собою комплексы, подобные разобранным ранее, которые в ответ на действие ЛПНП синтезируют из АТФ циклические нуклеотиды. Последние (как вторичные мессенджеры) включают механизм интернализации. Окаймленная клатрином ямка с холестерин-ЛПНП-рецепторными комплексами погружается внутрь цитоплазмы.
В цитоплазме холестерин-ЛПНП-рецепторный комплекс распадается на рецептор и холестерин-ЛПНП. Рецептор возвращается в плазмолемму, холестерин-ЛПНП поступает в лизосому, где расщепляется на холестерин и ЛПНП. Холестерин встраивается в мембрану как составной ее элемент, ЛПНП возвращается в плазму крови для захвата новой порции холестерина. Нарушение обмена холестерина лежит в основе патогенеза ряда тяжелых заболеваний, таких, как болезнь Нимана-Пика, ишемическая болезнь сердца и атеросклероз.
· Цитоплазматические и ядерные рецепторы.Управление многими морфофункциональными образованиями внутри клетки осуществляется с помощью ряда экзолигандов, не подвергающихся предварительному преобразованию в поверхностных рецепторно-эффекторных комплексах. Проведение таких лигандов к внутриклеточным эффекторам осуществляется в несколько этапов. На первом этапе молекула лиганда связывается с плазмолеммальным рецептом и в комплексе с ним погружается в цитоплазму. Там лиганд высвобождается и перебрасывается на цитоплазматический рецептор. Для одних лигандов (цитоплазматических) этот рецептор будет конечным, для других (ядерных) – промежуточным. В последнем случае лиганд в комплексе с цитоплазматическим рецептором поступает в ядро и соединяется с ядерным рецептором – конечной точкой приложения. К лигандам, взаимодействующим с расположенными внутри клеток рецепторно-эффекторных комплексами, относятся белково-пептидные, стероидные, тиреоидные и некоторые другие гормоны. Здесь мы остановимся на двух примерах, для которых достаточно хорошо известны конечные точки приложения, а именно, на инсулиновых и тиреоидных рецепторах.
· Инсулиновые рецепторы.Инсулин относится к группе белково-пептидных гормонов, продуцируемых гипофизом (адренокортикотропных, липотропный, соматотропный, тиреотропный и другие гормоны), гипоталамусом (рилизинг-факторы), поджелудочной железой (инсулин, глюкагон), щитовидной железой (тиреокальцитонин) и другие. Сюда же можно отнести физиологически активные пептиды: ангиотензины, субстанцию Р, соматомедины и др. Наиболее изученными из этой группы являются инсулиновые рецепторы. Они обнаруживаются в клетках практически всех тканей: в гепатоцитах, адипоцитах, моноцитах, эритроцитах, клетках панкреатических островков, в плаценте, ядрах клеток щитовидной железы и т.д.
Рецептор инсулинового рецепторно-эффекторного комплекса представляет собой интегральный белок, состоящий из двух альфа- и двух бета-субъединиц (Рис.22).
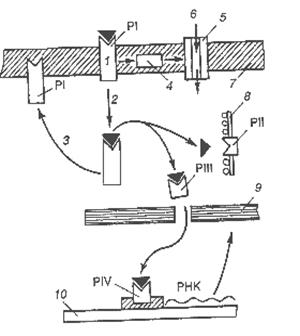
| Рис.22. Схема проведения инсулина к цитоплазматическим и ядерным рецепторным комплексам: ▲ – инсулин; - рецептор (Р); PI – плазмолеммальный рецептор; PII – цитоплазматический рецептор конечный; PIII - цитоплазматический рецептор промежуточный; PIV – ядерный рецептор; 1 – комплекс рецептор-инсулин; 2 – интернализация инсулин-рецепторного комплекса; 3 – возвращение рецептора PI в мембрану; 4 – сопрягающее звено; 5 – трансмембранный канал; 6 – аминокислоты, глюкоза, ионы; 7 – плазмолемма; 8 – мембрана эндоплазматической сети; 9 – ядерная оболочка; 10 – хромосома]. |
Рецептивный участок располагается на альфа-субъединице. Эффекторным звеном служить аденилатциклаза. Рецептор сопряжен с эффектором с помощью G-белка (участок бета-субъединицы), оказывающим, в отличие от других белково-пептидных гормонов, ингибирующее влияние на аденилатциклазу. При связывании инсулина с плазмолеммальными рецепторам PI происходят двоякого рода события: во-первых, активация инсулиновых рецепторно-эффекторных комплексов и, как следствие, поступление в клетку пластических, энергетических и других веществ; во-вторых, индукция феномена фосфорилирования самого инсулинового рецептора, молекула которого обладает протеинкиназной активностью, и, как следствие, интернализация всего инсулин-рецепторного комплекса. Пока неизвестно, один и тот же плазмолемальный рецепторный комплекс опосредует акты интернализации и транспорта метаболитов в клетку или имеются разные рецепторно-эффекторные комплексы, как в случае с холинергическими рецепторами.
В цитоплазме лиганд-рецепторный комплекс разъединяется. Рецептор PI возвращается в мембрану, а инсулин поступает либо на конечный цитоплазматический рецептор PII, либо на промежуточный цитоплазматический рецептор PIII и далее на конечный ядерный рецептор PIV, расположенный в хромосоме. Ядерные рецепторы, как правило, регулируют процессы транскрипции, то есть в конечном итоге управляют белковыми синтезами. Высказывается мнение, что раскрытием транспортных каналов сначала обеспечивается поступление в клетку энергетических и пластических материалов, которые потом будут необходимы для синтетических процессов после присоединения молекул инсулина к своим конечным рецепторам PIV.
Рецепторы гормонов, как и другие мембранные белки, подвергаются непрерывному обмену: функционально отработанные белки деградируют, вновь синтезированные встраиваются в мембрану. В клетках существует механизм регулирования скорости деградации и синтеза рецепторных белков, что создает оптимальный уровень рецепторов на плазматической мембране клеток и внутри них, так что тем самым обеспечивается необходимая для клетки чувствительность к гормональному сигналу.
Знание механизмов регуляции, как числа рецепторов, так и сопряжения их с эффекторами, имеет большее значение для практической медицины. Так, у тучных людей отмечается резистентность к инсулину. У них при стабильности метаболизма биологически активного инсулина наблюдается уменьшение его связывания, обусловленное снижением концентрации рецепторов к инсулину. Причиной резистентности к инсулину может быть наличие специфических антител к инсулиновым рецепторам, которые значительно уменьшают связывание инсулина с рецепторами. Антитела к инсулиновым рецепторам были обнаружены у пациентов с резистентными формами диабета.
· Прогестероновые рецепторы.Прогестерон, относящийся к группе стероидных гормонов, регулирует экспрессию генов, участвует в обменных процессах, в механизмах развития и морфогенеза. Рецепторы к прогестерону впервые были обнаружены в яйцеводе кур, где прогестерон индуцирует синтез белка куриного яйца – овидина; позднее они были найдены в половых органах женщин и в головном мозге. Путь продвижения лиганда из внеклеточного пространства к своему конечному рецептору на хромосоме представляется в следующем очень схематическом и во многом гипотетическом виде. На первом этапе лиганд поступает на экзорецепторы в плазмолемме. Прогестероновые экзорецепторы пока не обнаружены. Можно лишь полагать, что они относятся к интернализационному типу и доставляют лиганд в цитоплазму. На втором этапе лиганд перемещается в цитоплазме для соединения со своим цитоплазматическим рецептором. Прогестероновый рецептор состоит из двух субъединиц. На одной из них находится лиганд-связывающий участок, на другой – ДНК-связывающий. В отсутствие лиганда рецептор находится в перинуклеарной зоне. При поступлении прогестерона в цитоплазму он прикрепляется к лиганд-связывающему участку рецептора. Лиганд-рецепторынй комплекс активируется, становится мобильным и из перинуклеарной зоны через ядерную пору перемещается в ядро.
На третьем (внутриядерном) этапе продвижения лиганд вместе с цитоплазматическим прогестероновым рецептором проникает в ядро и направляется к ядерному рецептору, расположенному в хромосоме. Участки хроматина, специфически связывающие комплексы стероидов с их цитозольными рецепторами, называют еще акцепторами. В качестве ядерного рецептора можно считать специфическую лиганд-чувствительную последовательность ДНК, активирующим ген-мишень. Гормон-рецепторные комплексы в ядре обнаруживаются в конденсированном гетерохроматине, в цитоплазме – в гранулярной эндоплазматической сети. Цитоплазматический прогестерон-рецепторный комплекс своим ДНК-связывающим участком прикрепляется к прогестерон-чувствительной последовательности ДНК и через промотор включает в действие эффекторный участок ДНК, т.е. структурный ген.
· Рецепторы гормонов щитовидной железы.Гормоны щитовидной железы влияют на огромное количество метаболических процессов. Они участвуют в механизмах дифференцировки и созревания тканей, регулируют обмен веществ, в том числе белковые синтезы.
Рецепторы гормонов щитовидной железы распространены повсеместно в организме, однако их концентрация в различных тканях сильно варьирует. Считается, что тиреоидные гормоны сугубо ядерные, но пока это еще не вполне доказано. Возможно, что, как и в случае со стероидными гормонами, тиреоидные гормоны последовательно перебрасываются с экзорецептора на цитоплазматический и далее на ядреный рецептор.
Экзорецепторы к ним пока не обнаружены. По-видимому, как и в случае с прогестероном, в цитоплазме находятся рецепторы с гормон- и ДНК-связывающими участками. Тиреоидные гормоны, поступая в клетку, прикрепляются к гормон-связывающему участку рецептора и в комплексе с ним перемещаются в ядро. В ядре гормон-рецепторный комплекс соединяется своим ДНК-связывающим участком со специфической последовательностью ДНК, изменяя экспрессию гена-мишени.
Механизмы переноса информации к эффекторным структурам, заключенные в молекулах рассматриваемого семейства лигандов, сложны и многозвенны. Нарушение работы любого из звеньев способно приводить к искажению физиологического ответа на гормональный сигнал. Так, например, отсутствие гормонов щитовидной железы в период развития организма приводит к нарушению созревания мозга, проявляющемуся в форме выраженного слабоумия (кретинизма), у взрослых – к синдрому микседемы.
Имеются сведения, что при развитии рака эндометрия у женщин важную роль играет длительная эстрогенизация, которая возникает при функциональных и органических изменениях в яичниках, нарушениях метаболизма стероидов, неадекватной гормонотерапии, изменении спектра секретируемых гормонов. Вопрос о нарушениях работы рецептора и рецепторных механизмов, опосредующих управляющее влияние данной группы лигандов на внутриклеточные органеллы-мишени, подробно рассматриваются во многих эндокринологических работах.
Таким образом, жизнедеятельность клетки регулируется с помощью клеточных рецепторно-эффекторных комплексов, состоящих из собственно рецептора, эффектора и сопрягающего их элемента.
Рецепторное звено воспринимает первичный информационный сигнал и формирует собственный пострецепторный сигнал, предназначенный для специфического прохождения по остальным звеньям комплекса.
Сопрягающее звено воспринимает пострецепторный сигнал и передает его на исполнительную структуру – эффектор. В качестве эффектора выступают ионные каналы, ферментные молекулы, каналы для метаболитов. Первые для образования формируют вторичные информационные молекулы (Са2+, цАМФ и др.), предназначенные для введения в действие внутриклеточных органелл, обеспечивающих физиологический ответ клетки.
Часть первичных сигналов (нейромедиаторы) действует на экзорецепторы и не требует непосредственного проникновения в клетку, другая часть (инсулин, гормоны щитовидной железы ид р.) проходит в нативном состоянии внутрь клетки (интернализация) для приведения в действие цитоплазматических и ядерных морфофункциональных образований. Визуализация клеточных рецепторов на морфологическом уровне осуществляется с помощью мечения сигнальных молекул (лигандов), а также антител к рецепторам белкам. В основе многих заболеваний человека и животных существенную роль играют нарушения лиганд – рецепторно–эффекторных взаимоотношений.
Дата добавления: 2015-08-08; просмотров: 1819;
