Электролитами называют вещества, при взаимодействии с растворителем подвергающиеся диссоциации на ионы и сообщающие раствору способность проводить электрический ток.
Основные понятия теории растворов электролитов
Различают слабые и сильные электролиты. Сильные электролиты в растворе полностью распадаются на ионы. К таким электролитам относятся сильные кислоты и основания, а также соли.
Слабые электролиты в растворе распадаются на ионы частично. К слабым электролитам относятся карбоновые кислоты, аммиак, амины, фенолы и др.
Количество ионов каждого знака определяется стехиометрическими коэффициентами в формуле электролита при соблюдении закона электронейтральности, в соответствии с которым сумма положительных зарядов должна быть равна сумме отрицательных. Например, СаCI2→Ca2++2CI-.
Электролиты, молекулы которых распадаются на два иона, называются бинарными или симметричными.Если при этом образуются однозарядные ионы, электролит относится к типу 1, 1-валентных (NaCl и т.д.), если двухзарядные — к типу 2, 2-валентных (MgSO4 и т.д.). Для несимметричных электролитов (K2SO4 и т.д.) тип электролита также устанавливается по заряду ионов и относится к типу 1,2.
2. Теория С Аррениуса/
Согласно теории С. Аррениуса (1883—1887), процесс распада растворенного вещества на ионы называют электролитической диссоциацией. Распад на ионы происходит независимо от того, подвергается или не подвергается вещество действию электрического тока.
Способность электролитов распадаться на ионы количественно оценивают степенью диссоциации (а).
Степенью электролитической диссоциации называют отношение числа молекул распавшихся на ионы пi, к исходному числу молекул пΣ:
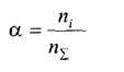
Для сильных электролитов а = 1, а для слабых много меньше единицы. Степень диссоциации слабых электролитов зависит от концентрации электролита в растворе.
Дата добавления: 2015-08-08; просмотров: 1215;
