Влияние катализатора на скорость химических реакций
Вещества, которые участвуют в реакциях и увеличивают ее скорость, оставаясь к концу реакции неизменными, называются катализаторами.
Явление изменения скорости реакции под действием таких веществ называется катализом. Реакции, протекающие под действием катализаторов, называются каталитическими.
В большинстве случаев действие катализатора объясняется тем, что он снижает энергию активации реакции. В присутствии катализатора реакция проходит через другие промежуточные стадии, чем без него, причем эти стадии энергетически более доступны. Иначе говоря, в присутствии катализатора возникают другие активированные комплексы, причем для их образования требуется меньше энергии, чем для образования активированных комплексов, возникающих без катализатора. Таким образом, энергия активации резко понижается: некоторые молекулы, энергия которых была недостаточна для активных столкновений, теперь оказываются активными.
Для ряда реакций промежуточные соединения изучены; как правило, они представляют собою весьма активные нестойкие продукты.
Механизм действия катализаторов связан с уменьшением энергии активации реакции за счет образования промежуточных соединений. Катализ можно представить следующим образом:
А + К = А...К
А...К + В = АВ + К,
где А...К - промежуточное активированное соединение.
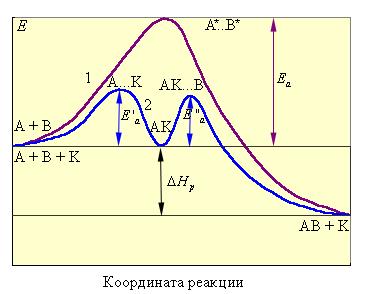
Рисунок 13.5 - Изображение реакционного пути некаталитической A + B → AB реакции (кривая 1) и гомогенной каталитической реакции (кривая 2).
В химической промышленности катализаторы применяются весьма широко. Под влиянием катализаторов реакции могут ускоряться в миллионы раз и более. В некоторых случаях под действием катализаторов могут возбуждаться такие реакции, которые без них в данных условиях практически не протекают.
Различают гомогенный и гетерогенный катализ.
В случае гомогенного катализа катализатор и реагирующие вещества образуют одну фазу (газ или раствор). В случае гетерогенного катализа катализатор находится в системе в виде самостоятельной фазы.
Примеры гомогенного катализа:
1) окисление SO2 + 1/2O2 = SO3 в присутствии NO; NO легко окисляется до NO2, а NO2 уже окисляет SO2;
2) разложение пероксида водорода в водном растворе на воду и кислород: ионы Сг2О2=7, WO2-4, МоО2-4, катализирующие разложение пероксида водорода, образуют с ним промежуточные соединения, которые далее распадаются с выделением кислорода.
Гомогенный катализ осуществляется через промежуточные реакции с катализатором, и в результате происходит замена одной реакции с высокой энергией активации несколькими, у которых энергии активации ниже, скорость их выше:
CO + 1/2O2 = CO2 (катализатор - пары воды) .
Широкое применение в химической промышленности находит гетерогенный катализ. Большая часть продукции, вырабатываемой в настоящее время этой промышленностью, получается с помощью гетерогенного катализа. При гетерогенном катализе реакция протекает на поверхности катализатора. Отсюда следует, что активность катализатора зависит от величины и свойств его поверхности. Для того чтобы иметь большую («развитую») поверхность, катализатор должен обладать пористой структурой или находиться в сильно раздробленном (высокодисперсном) состоянии. При практическом применении катализатор обычно наносят на носитель, имеющий пористую структуру (пемза, асбест и др.).
Как и в случае гомогенного катализа, при гетерогенном катализе реакция протекает через активные промежуточные соединения. Но здесь эти соединения представляют собой поверхностные соединения катализатора с реагирующими веществами. Проходя через ряд стадий, в которых участвуют эти промежуточные соединения, реакция заканчивается образованием конечных продуктов, а катализатор в результате не расходуется.
Все каталитические гетерогенные реакции включают в себя стадии адсорбции и десорбции.
Каталитическое действие поверхности сводится к двум факторам: увеличению концентрации на границе раздела и активированию адсорбированных молекул.
Примеры гетерогенного катализа:
2H2O = 2H2O + O2 (катализатор – MnO2,) ;
Н2 + 1/2 О2 = Н2О (катализатор - платина) .
Очень большую роль играет катализ в биологических системах. Большинство химических реакций, протекающих в пищеварительной системе, в крови и в клетках животных и человека, являются каталитическими .реакциями. Катализаторы, называемые в этом случае ферментами, представляют собою простые или сложные белки. Так, слюна содержит фермент птиалин, который катализирует превращение крахмала в сахар. Фермент, имеющийся в желудке, — пепсин — катализирует расщепление белков. В организме человека находится около 30 000 различных ферментов: каждый из них служит эффективным катализатором соответствующей реакции.
Селективность действия катализатора заключается в том, что продукты реакции могут быть разными в зависимости от того, каким катализатором мы пользуемся.
Резко замедлить протекание нежелательных химических процессов в ряде случаев можно, добавляя в реакционную среду ингибиторы (явление «отрицательного катализа»).
Дата добавления: 2015-08-08; просмотров: 3038;
