Методы мокрой минерализации
Первый метод минерализации биологического материала при химико-токсикологических исследованиях с использованием в качестве окислителя концентрированной кислоты азотной предложил русский ученый Нелюбин А.П. Этот метод сыграл большую роль в развитии химико-токсикологического анализа. Однако разрушение биологического материала при нагревании с концентрированной HNO3 требует большой затраты времени, реагент слабо окисляет жиры. В дальнейшем в качестве окислителя использовалась концентрированная кислота серная, действующая одновременно и как дегидратирующий агент. Однако, этот процесс тоже был весьма продолжительным по времени, и в процессе минерализации образовывались неразлагающиеся обуглившиеся остатки. Для устранения этих недостатков в 1821 году М.Ж.Орфила предложил применять смесь концентрированных серной и азотной кислот. Этот метод был модифицирован и применен для целей химико-токсикологического анализа в 1908 году П.К. Равданикисом. До настоящего времени этот, метод находит применение в практике Бюро СМЭ и является по сути дела основным методом минерализации.
Метод минерализации смесью концентрированных серной,
азотной кислот и воды (1:1:1)
Процесс разрушения биологического объекта протекает в 2 стадии:
1. Стадия деструкции, на которой происходит разрушение биологических субстратов организма (белков, жиров, углеводов) на составные части: белки разрушаются до аминокислот, углеводы (полисахариды) до ди- и моносахаридов жиры до глицерина и жирных кислот. Менее всего подвержены разрушению на первой стадии жиры. На первой стадии нагревание не должно быть сильным, чтобы избежать подгорания объекта или сильного пенообразования и выброса частиц объекта из колбы. Поэтому, в начале процесса колбу Къельдаля закрепляют над плиткой на расстоянии 1-2 см. Температура не должна превышать 110°С. Эта стадия непродолжительна по времени, длится от 15 до 40 минут. По окончании деструкции получается прозрачная желтовато-бурая жидкость, иногда с пленкой жира, т.к. на этой стадии все элементы объекта разрушены, кроме жиров.
На стадии деструкции концентрированная H2SO4 выполняет роль водоотнимающего средства, что приводит к нарушению структуры клеток и тканей, деформирует их. При этом она способствует повышению температуры кипения смеси и тем самым повышает окислительное действие концентрированной HNO3.
Роль окислителя на первой стадии выполняет концентрированная HNO3.
Кислота азотная, свободная от окислов азота, что наблюдается в самом начале минерализации, почти инертна. Под влиянием индуцирующих веществ в процессе окисления биоматериала часть кислоты азотной разлагается до кислоты азотистой и оксидов азота, которые являются катализаторами окисления. Под их влиянием и с повышением температуры азотная кислота проявляет себя как сильный окислитель. Идет интенсивный автокаталитический процесс окисления органических веществ:
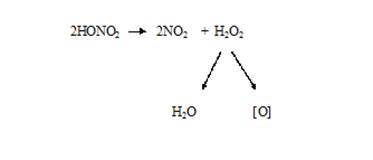
2. Стадия глубокого жидкофазного окисления. Колбу Къельдаля опускают на плитку и усиливают нагревание. На этой стадии происходит окончательное разрушение органических веществ. Полностью разрушаются и жиры, которые на первой стадии почти не пострадали под действием кислоты азотной. В процессе окисления необходимо по каплям постоянно добавлять в колбу разведенную кислоту азотную из капельной воронки, но при этом скорость добавления реактива должна быть такова, чтобы бурые пары окислов азота, образующиеся при минерализации, не выходили из колбы. Эта стадия длится 3-4 часа и считается законченной тогда, когда:
- начинает выделяться белый туман (пары SО2);
- жидкость остается бесцветной;
-минерализат не темнеет в течение 30 минут без добавления кислоты азотной.
Роль окислителя на этой стадии играет концентрированная кислота серная (её концентрация повышается в смеси до 60-70%, температура превышает 110 °С). Она разлагается с выделением оксида серы (IV) и активного кислорода.
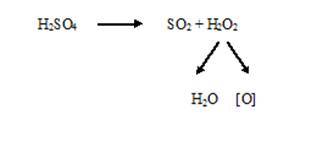
В процессе минерализации происходит не только разрушение органических веществ, но и ряд побочных реакций, имеющих негативное значение:
А) Кислота серная в высоких концентрациях сульфирует органические вещества, а кислота азотная, особенно в присутствии кислоты серной, - нитрует их. Сульфо- и нитросоединения очень прочные, трудно поддаются воздействию окислителей, что влечет за собой неполное разрушение биообъекта. Эти негативные процессы можно значительно уменьшить. Это достигается использованием не концентрированных кислот, а частично разбавленных добавлением в окислительную смесь воды (вспомните соотношение реагентов в окислительной смеси). При разбавлении Н2SO4 и HNO3 водой степень нитрования - сульфирования значительно снижается.
Б) Ещё одна побочная реакция связана с образованием нитрозилсерной кислоты при взаимодействии оксидов азота с концентрированной серной кислотой.
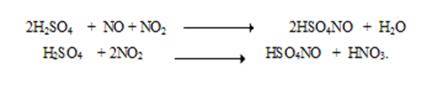
Нитрозилсерная кислота очень устойчива к температуре, однако легко гидролизуется. Реакция гидролиза обратима.

Нитрозилсерная кислота является источником окислителей в минерализате, что мешает в дальнейшем обнаружению некоторых катионов металлов. Чтобы избавиться от негативного воздействия нитрозилсерной кислоты, её удаляют путем проведение денитрации.
Достоинства метода:
1. Сравнительно быстрое достижение полноты разрушения органических веществ.
2. Полнота разрушения объекта обусловливает большую чувствительность методов анализа катионов металлов.
3. Малый объем получаемого минерализата, что также повышает чувствительность методов анализа.
Основным недостатком метода являются большие потери Нg (до 90-98%) за счет её летучести. Поэтому изолирование ртути в виде ионов проводят в отдельной навеске биообъекта частным методом изолирования, который исключает использование высоких температур, процесс ведется в присутствии катализатора (этанола).
Метод минерализации смесью серной, азотной и хлорной кислот (1:1:1)
Кислоту хлорную в качестве окислителя в аналитической химии впервые применил А.Щербак в 1893 году.
В качестве окислительной смеси при изолировании этим методом используют смесь из равных объемов концентрированной H2SO4 и концентрированной HNO3 и 37% или 42% НСlO4. Методика выполнения изолирования аналогична первому методу, однако второй метод имеет ряд несомненных достоинств:
1. Высокая скорость минерализации, сокращение в 2-3 раза затрат времени в сравнении с первым методом.
2. Очень высокая степень окисления органических веществ (до 99 %), что обусловлено способностью хлорной кислоты разрушать вещества стойкие или медленно разлагающиеся другими окислителями.
3. Окисление большинства поливалентных металлов до высших степеней окисления.
4. Небольшой расход окислителей.
5. Малый объем получаемого минерализата, что повышает чувствительность методов анализа.
Основной недостаток тот же, что и у первого метода – практическая полная потеря ртути. Однако есть еще одна опасность при использовании кислоты хлорной в составе окислителей - это взрывоопасность и токсичность хлорной кислоты. Безводная кислота хлорная нестойкая, может взрываться при хранении при повышенной температуре или при соприкосновении с некоторыми органическими соединениями. Это требует соблюдения особых мер предосторожности при работе с кислотой хлорной.
При любом способе минерализации следует соблюдать меры предосторожности, т.к. возможны термические ожоги, выбрасывание горячих кислот из колб и даже взрывы (особенно при использовании в качестве окислителей пергидроля, хлорной кислоты и хлората калия). Поэтому следует пользоваться защитными очками, работать в вытяжных шкафах с хорошей тягой.
Нельзя не остановиться ещё на одном очень важном этапе исследования «металлических ядов» - проверке чистоты реактивов. Недостаточно чистые кислоты - окислители могут загрязнять минерализаты соединениями металлов, при этом количество примесей может оказаться весьма значительным, что послужит основанием для ошибочного заключения о наличии «металлических ядов в биоматериале и причине отравления. Чтобы исключить ошибку, необходимо применять кислоты, свободные от примесей. Если степень их чистоты неизвестна, то проводят «холостой опыт», т.е. берут реактивы в нужных для методики количествах и полностью воспроизводят её. Только при отрицательных эффектах реакций обнаружения металлов, делают вывод о пригодности кислот для использования в процессе минерализации.
Независимо от того, каким методом проводилась минерализация биологического материала, минерализат в большинстве случаев содержит окислители, которые помешают дальнейшему проведению анализа. Это азотная, азотистая кислоты, оксиды азота, нитрозилсерная кислота. Для их удаления используются методы денитрации. Применяемые ранее гидролизный метод, метод денитрации мочевиной, натрия сульфитом практически вытеснены методом денитрации формальдегидом. Метод предложен в 1952 году Т.В.Зайковским. Процесс денитрации заканчивается за 1-2 минуты, избыток непрореагировавшего формальдегида легко удаляется при нагревании в течение 5-10 минут. Для проверки полноты денитрации минерализата проводят реакцию с дифениламином в среде концентрированной кислоты серной.
Полученную после минерализации жидкость, в которой металлы находятся в виде сернокислых солей, разбавляют водой до определенного объема в мерной колбе (200мл) и используют для проведения качественного анализа "дробным" методом и количественного определения.
3.3.2. Методика изолирования металлических ядов из биологического материала общим методом минерализации
100 г биологического объекта в колбе Къельдаля заливают 75 мл окислительной смеси (кислоты серной концентрированной, кислоты азотной концентрированной, воды дистиллированной в соотношении 1:1:1). Колбу закрепляют в штативе вертикально на расстоянии 1-2 см от асбестовой сетки. Над колбой помещают капельную воронку с разбавленной азотной кислотой (1:1). Колбу осторожно взгревают на плитке, добавляя при необходимости (потемнение жидкости) разбавленную азотную кислоту (1:1) по каплям до просветления жидкости. Концом минерализации считается момент, когда в колбе остается 15-20 мл бесцветной или окрашенной жидкости, которая не темнеет в течение 30 минут при постоянном нагревании, без добавления кислоты азотной. Охлажденный минерализат осторожно выливают в химический стакан, содержащий 30 мл дистиллированной воды, колбу Къельдаля ополаскивают два раза дистиллированной водой по 10мл и присоединяют промывные воды к разбавленному минерализату. Разбавление минерализата способствует затем более легкому протеканию процесса денитрации.
В маленькой фарфоровой чашке в 2-3 каплях концентрированной кислоты серной растворяют 2-3 кристалла дифениламина и к полученному бесцветному раствору прибавляет одну каплю разбавленного минерализата. В случае появления сине-голубого окрашивания проводят денитрацию раствора.

Дифениламин

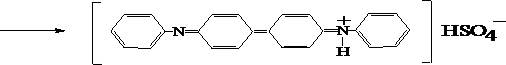
Стакан с содержимым ставят на плитку, нагревают до кипения и вносят одну каплю формалина; кипятят 10 минут и вновь проделывают реакцию дифениламином.
Химизм денитрации:

4 HNO2 + 2 H2CO ® 2 NO + N2 + 2 CO2 + 4 H2O
4 HNO3 + 3 H2CO ® 4 NO + 3 CO2 + 5 H2O
4 HNO3 + 5 H2CO ® 2 N2 + 5 CO2 + 7 H2O
В случае отсутствия голубого окрашивания в результате реакции с дифениламином жидкость кипятят до исчезновения запаха формалина, охлаждают, количественно переносят в мерную колбу на 200 мл и доводят водой очищенной до метки. Жидкость из мерной колбы переносят в чистую сухую склянку и используют для обнаружения катионов (100 мл) и количественного определения (100 мл). Если при разбавлении минерализата водой выпадает осадок, то независимо от того, проводилась денитрация или нет, жидкость в стакане нагревают до кипения, кипятят 10 минут и оставляют стоять на сутки для получения более плотного осадка. На второй день белый кристаллический осадок отфильтровывают через плотный фильтр
В осадке после проведения минерализации могут находиться нерастворимые в воде сульфаты бария, свинца и кальция. Химико-токсикологический интерес представляют только барий и свинец, которые необходимо до обнаружения разделить.
Для этого осадок отфильтровывают через плотный фильтр, промывают 2 – 3 раза водой очищенной и присоединяют промывные воды к фильтрату, доводя его до метки в мерной колбе.
Осадок на фильтре 2 раза промывают водой, подкисленной 1 % раствором кислоты серной. Промывные воды отбрасывают. Затем осадок на фильтре многократно обрабатывают 5 мл горячего насыщенного раствора аммония ацетата, подкисленного кислотой уксусной (каждый раз нагревая фильтрат).
PbSO4 + 2 CH3COONH4 ® (CH3COO)2Pb + (NH4)2SO4
Этот, второй фильтрат, исследуют на ионы свинца, а осадок на фильтре – на ионы бария.
3.4. ДРОБНЫЙ МЕТОД АНАЛИЗА «МЕТАЛЛИЧЕСКИХ ЯДОВ»
Теоретические основы дробного метода анализа в аналитической химии были разработаны профессором Н.А.Тананаевым в 30-е годы прошлого века. Для целей судебно-химического анализа дробный метод разработала и внедрила А.Н.Крылова. Дробный метод полностью вытеснил ранее применявшийся систематический сероводородный метод.
Дробный метод предусматривает определение одних ионов металлов в отдельных небольших порциях исследуемого раствора в присутствии других без их предварительного разделения на группы, что достигается использованием соответствующих аналитических приемов и проведением анализа по определенной схеме, в которой обозначена последовательность обнаружения ионов.
Обнаружение искомых ионов дробным методом проводится в 2 этапа: вначале устраняется влияние мешающих ионов с помощью соответствующих приемов и реактивов, а затем, на втором этапе - прибавляют реактив, дающий какой-либо аналитический сигнал (окраску, осадок и др.) с открываемым ионом.
Дробный метод анализа особенно удобен в случаях с «лимитированными заданиями», т.е. когда задача эксперта ограничена заданием провести исследование только на определенные ионы или исключить тот или иной ион. Таким образом, дробный метод вполне удобен и экономичен, как нельзя лучше подходит для решения практических задач судебно-химической экспертизы.
Специфические особенности судебно-химического анализа на металлические яды:
1. Необходимость выделения из большого количества биологического объекта малых количеств (мг-мкг) веществ, которые могли послужить причиной отравления.
2. Необходимость исследования на сравнительно большую группу ядов (13 элементов), обладающих некоторой общностью химических свойств (d-элементы).
3. Специфический характер объектов исследования. Ими чаще всего являются внутренние органы трупа, которые могут содержать в качестве естественных почти все химические элементы, известные как «металлические яды» (за исключением Ba, Bi, Sb, Tl). Поэтому всегда встает вопрос о количественном определении. Данные количественного анализа позволяют судебно-медицинским экспертам решать вопрос, являются ли найденные металлы введенными в организм или естественно содержащимися.
Учитывая специфические особенности судебно-химического анализа А.Н.Крылова при разработке дробного метода предъявила ряд требований, чтобы анализ был достаточно быстрым, надежным и экономичным:
1. Должна быть возможность сочетания качественного и количественного определения в одной навеске исследуемого органа на все токсикологически важные элементы (за исключением ртути, которая определяется в отдельной навеске навеске специфическим деструктивным методом).
2. Должна быть обеспечена высокая доказательность и надежность метода. Это достигается применением, как правило, не одной, а, по меньшей мере, двух реакций: основной и подтверждающей. В качестве основных чаще всего используются жидкофазные реакции образования окрашенных комплексов с различными реагентами, извлекаемых в слой органического растворителя (дитизонатов, диэтилдитиокарбаминатов, комплексов с 8-оксихинолином, красителями трифенилметанового ряда и др.). Большинство подтверждающих реакций - микрокристаллоскопические или осадочные.
3. Реакции должны быть высоко специфичными, чтобы определять катион в присутствии других. Однако абсолютно специфичных реакций очень мало, поэтому необходимо создавать селективные условия и устранять мешающее влияние посторонних ионов. Для этого разработаны следующие приемы:
- маскировка мешающих ионов. Осуществляется путем введения комплексообразователей, применения окислительно-восстановительных реакций и др.;
-строгое соблюдение определенных значений рН среды при проведении реакций;
-селективная экстракция металлов в органический растворитель в виде комплексов или ионных ассоциатов с последующей реэкстракцией ионов металлов в водную фазу.
4. Реакции должны быть высокочувствительны, но не должны открывать естественно содержащиеся количества элементов. Поэтому для выполнения реакций на отдельные катионы объем минерализата строго лимитирован. Кроме того, применяют прием разбавления минерализата до пределов чувствительности реакции. При этом снижается влияние мешающих ионов и концентрация кислот, исключается обнаружение большинства естественно содержащихся элементов.
5. Методики, разработанные для обнаружения «металлических ядов» быть простыми, доступными, а их проведение не требовать больших затрат времени на анализ, и дорогостоящего оборудования и реагентов.
Таким, образом, А.Н.Крылова рассматривает дробный метод обнаружения «металлических ядов» как сумму отдельных наиболее характерных и чувствительных реакций на катионы. Дробный метод разработан на 13 наиболее важных в токсикологическом отношении элементов. Он обязательно сочетается с параллельно проводимым частным методом обнаружения и количественного определения иона ртути после деструкции отдельной навески биоматериала.
При составлении схемы проведения дробного анализа необходимо учитывать ограниченную специфичность отдельных реакций:
1. Чувствительность реакций на хром и марганец снижается при большом количестве в минерализате хлорид-ионов, поэтому исследование на хром и марганец рекомендуется проводить до осаждения Аg в виде АgCl с помощью NaCI.
2. Обнаружению мышьяка мешает присутствие в минерализате катионов сурьмы, в связи с чем исследование на сурьму предшествует анализу на мышьяк.
3. Большие количества меди мешают обнаружению сурьмы по реакции образования её сульфида Sb2S3 (черный осадок CuS маскирует оранжевую окраску Sb2S3). Следовательно, в ряду катионов по схеме дробного анализа медь должна стоять раньше сурьмы.
Для повышения надежности обнаружения «металлических ядов» А.Н. Крылова предлагает определенный порядок их анализа в минерализате. А именно: свинец, барий, марганец, хром, серебро, медь, сурьма, таллий, мышьяк, висмут, кадмий. Параллельно проводится анализ на ртуть после деструкции отдельной навески органов (печень, почки).
Дата добавления: 2015-08-01; просмотров: 7490;
