Абразивная струйная очистка сжатым воздухом.
- Абразивная струйная очистка с впрыскиванием влаги.
- Струйная очистка жидкостью под давлением.
В электролитической ячейке, изображенной на рис. 2, протекают те же реакции, что и в промышленных электролизерах для получения хлора и щелочи: превращение рассола (концентрированного водного раствора хлорида натрия) в хлор и гидроксид натрия NaOH:
циал (измеряемый в вольтах, В). Сила тока определяется скоростью электродных реакций, а потенциал - химической энергией протекающих в ячейке процессов. Он равен энергии (измеряемой в джоулях, Дж), отнесенной к количеству электричества (измеряемому в кулонах, Кл), т.е. 1 В = 1 Дж/Кл. Следовательно, потенциал элемента (электродвижущая сила, ЭДС) - это мера энергии, вырабатываемой в ходе протекающих в нем реакций. Если внешняя цепь разомкнута, то никакие электродные реакции не идут. Потенциал гальванического элемента при разомкнутой внешней цепи дает информацию о термодинамике его реакций. Потенциал элемента, представленного на рис. 1, при концентрациях растворов 1 М и температуре 25° С - его стандартный потенциал E° - равен 1,10 В. Соответствующая ему энергия, термодинамический потенциал Гиббса, DG°, определяется выражением
 >
>
где n - число электронов, переносимых в ходе реакции (в данном случае 2), F - число Фарадея (96 485 Кл/моль). Потенциал гальванического элемента равен разности потенциалов двух его полуэлементов, т.е. разности его электродных потенциалов. Электродные потенциалы измеряют относительно потенциала электрода сравнения, который условно принимается за нуль (см. таблицу).
Электродные реакции. Потенциометрические измерения проводят в условиях, когда ток в электрохимической ячейке отсутствует. Это значит, что в ней не происходит никаких суммарных химических изменений, а измеряемый потенциал (равновесный) определяется термодинамикой реакций. В этих условиях такие факторы, как размер и форма электродов или интенсивность перемешивания раствора, не влияют на измеряемый потенциал. Если же через электрохимическую ячейку течет ток, то скорость электродных реакций зависит не только от термодинамических параметров, но и от силы тока в соответствии с уравнением
<> 
где n - число электронов, участвующих в данной электродной реакции, F - число Фарадея. В этом случае потенциал электрохимической ячейки зависит от кинетических факторов, а также от материала, из которого сделан электрод, размеров и формы электрода, интенсивности перемешивания раствора и многих других факторов. Нельзя пренебречь внутренним сопротивлением ячейки. Кроме разности потенциалов на обеих границах электрод/электролит возникает падение напряжения в самом растворе, обусловленное его сопротивлением. Это падение напряжения затрудняет исследование эффектов, связанных с протеканием реакций на обоих электродах. Обычно изучают реакцию на одном электроде, который называют рабочим или индикаторным, используя для этого трехэлектродную ячейку (рис. 3): третий электрод (например, насыщенный каломельный) помещают в тот же отсек, что и рабочий, как можно ближе к нему, чтобы свести к минимуму эффект омического падения напряжения. Измеряя ток через рабочий электрод как функцию потенциала этого электрода относительно электрода сравнения, строят т.н. поляризационную кривую.
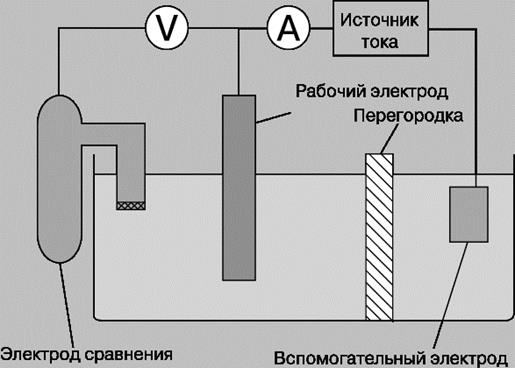
Рис. 3. ТРЕХЭЛЕКТРОДНАЯ ЯЧЕЙКА, используемая для электрохимических исследований. Потенциал рабочего электрода измеряется относительно электрода сравнения с помощью высокоомного вольтметра (V). Ток между рабочим и вспомогательным электродами измеряется амперметром (А).
При пропускании внешнего тока потенциал электрода отличается от равновесного. Это отклонение называется поляризацией, а его величина - перенапряжением. Перенапряжение зависит от нескольких факторов, лимитирующих скорость электродных реакций. Быстрые электродные реакции при данной плотности тока (сила тока на единицу поверхности электрода) идут при потенциалах, близких к термодинамическим, а следовательно, при малом перенапряжении. Для медленных реакций характерно высокое перенапряжение. Скорости электродных реакций, а значит, и перенапряжение зависят от концентрации реагентов, температуры, растворителя, материала электрода, способа и скорости переноса массы, плотности тока. Суммарное перенапряжение можно разложить на несколько компонентов: концентрационное, активационное и реакционное. Концентрационное перенапряжение обусловливается тем, что при прохождении тока изменяется концентрация реагирующего иона на поверхности электрода, поскольку в этой области расходуются электроактивные вещества и образуются продукты реакции. Рассмотрим восстановление Cu2+ на медном электроде. Вначале концентрация Cu2+ в растворе равна 1M. В отсутствие тока в цепи потенциал медного электрода близок к стандартному потенциалу пары Cu/Cu2+, т.е. 0,34 В относительно н.в.э. (см. уравнение (6)). По мере прохождения катодного тока концентрация ионов Cu2+ на поверхности электрода уменьшается, а катодный потенциал в соответствии с уравнением Нернста (10) становится все более отрицательным. Свежие порции реагента поступают из раствора к электроду разными способами: в результате диффузии, конвекции, миграции. Чем больше скорость этих процессов (например, чем интенсивнее перемешивание), тем меньше концентрационное перенапряжение. Эту составляющую суммарного перенапряжения часто удается рассчитать. Если концентрационная поляризация дает основной вклад в общее перенапряжение (это означает, что скорость остальных этапов электродной реакции велика), то реакция называется обратимой или нернстовской. Активационное перенапряжение возникает в результате того, что перенос электронов на поверхности электрода осуществляется не мгновенно, а с конечной скоростью. Рассмотрим обобщенную электродную реакцию ox + ne- = red. Чтобы переносить электроны на окисленные соединения с заданной скоростью (т.е. при данной плотности тока), необходимо преодолеть энергетический барьер, называемый энергией активации электродной реакции. Эту энергию поставляет приложенный потенциал. Связь между плотностью тока и активационным перенапряжением описывается уравнениями Батлера - Фольмера и Тафеля, с помощью которых можно определить кинетические параметры электродных реакций. Многие электродные реакции, такие, как восстановление воды до водорода и ее окисление до кислорода, протекают медленно. Скорость электродной реакции может сильно зависеть от материала, из которого сделан электрод, и свойств его поверхности. Например, на ртутном электроде восстановление воды до водорода существенно затруднено: для него характерно высокое водородное перенапряжение. Значительно быстрее и с меньшим перенапряжением эта реакция идет на платине; именно по этой причине платину используют в водородном электроде сравнения. Скорость реакций зависит также от веществ, которые адсорбируются или связываются с поверхностью электрода; так, цианид-ион и ряд органических соединений снижают скорость выделения водорода на поверхности платинового электрода. В то же время некоторые поверхностно-активные вещества могут значительно увеличивать скорость электродной реакции - их называют электрокатализаторами. Реакционное перенапряжение возникает в том случае, когда перенос электронов на электроде сопряжен с химической реакцией в растворе. Такая реакция может служить источником частиц, участвующих в переносе электронов, и при этом лимитировать скорость всего электродного процесса. Вот почему так важно знать детали механизма (т.е. стадии и промежуточные состояния) электродных реакций. Во многих случаях исходное вещество, прежде чем стать конечным продуктом на электроде, претерпевает несколько превращений, как в случае восстановления кислорода до воды - процесса, имеющего большое прикладное значение. Суммарная реакция имеет вид

и состоит из нескольких стадий, на одной из которых разрывается связь кислород-кислород. Вследствие этой многостадийности реакция на большинстве электродов идет медленно, и в промышленных масштабах ее проводят в присутствии электрокатализаторов. Механизм электродных реакций исследуют с помощью электроаналитических методов, описанных ниже. Часто ход реакции изменяется при изменении состава раствора и природы растворителя. Например, восстановление кислорода в ацетонитриле, где имеет место дефицит протонов, протекает в соответствии с простым одноэлектронным механизмом: 
Законы электролиза
Расчеты при электролизе
Схема электролиза
Электролиз расплавов
Электролиз растворов
Процессы окисления на инертном аноде
Процессы окисления на растворимом (металлическом) аноде
Процессы восстановления на катоде
Условие проведения электролиза
Зависимость тока от напряжения на электродах (график)
ЭДС обратного гальванического элемента
Перенапряжение
Потенциал разложения
Применение электролиза
Гальванопластика
Гальваностегия
Получение и очистка металлов
Дата добавления: 2015-07-30; просмотров: 1715;
