Химические свойства альдегидов и кетонов
Химические свойства карбонильных соединений определяются свойствами карбонильной группы.
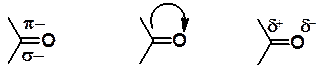
Двойная связь кислород-углерод похожа на углерод-углеродную двойную связь. Обе представляют собой комбинации s- и p-связей. Как уже было показано, для такой связи характерны реакции присоединения. Высокая электроотрицательность атома кислорода приводит к сдвигу в его сторону электронной плотности, а у атома углерода электронная плотность понижена. Следует ожидать, что позитивированный атом углерода в ходе реакций присоединения способен подвергаться атаке частицами, способными предоставить пару электронов для образования ковалентной связи с карбонильным углеродом.
Таким образом, строение карбонильной группы указывает на способность альдегидов и кетонов участвовать в реакциях нуклеофильного присоединения (AN).
Некоторые AN реакции рассматривались в предыдущих разделах курса. Так, реакции карбонильных соединений с реактивами Гриньяра, приводящая к спиртам (см. раздел «Спирты») и взаимодействие с ацетиленами (реакция Фаворского, см. «Алкины»), – типичные примеры нуклеофильного присоединения к карбонильной группе
Какова относительная реакционная способность альдегидов и кетонов в реакциях AN?
Из общих соображений можно выдвинуть следующее предположение:
· чем ниже электронная плотность на карбонильном углероде, тем легче нуклеофилу атаковать этот электрофильный центр.

Алкильные группы, как и атом водорода, обладают +I (донорным) эффектом, т.е. увеличивают электронную плотность на карбонильном углероде, уменьшая его электрофильность. Известно, что донорные свойства алкильных групп выражены в гораздо большей степени, чем аналогичные свойства атома водорода. Поэтому, альдегиды обладают большей реакционной способностью в реакциях AN.
Поскольку донорные свойства всех алкильных групп примерно одинаковы, следует ожидать, что все альдегиды и все кетоны будут иметь примерно одинаковую реакционную способность внутри ряда. Однако, реакции нуклеофильного присоединения к ацетону идут во много раз быстрее, чем аналогичные реакции с ди-трет-бутилкетоном. Для оценки реакционной способности следует рассматривать также стерические (пространственные) факторы. Чем больше размер, связанных с карбонильной группой, заместителей, тем труднее нуклеофилу подойти на расстояние стандартной длины связи. Поскольку размер атома водорода много меньше размера любой алкильной группы, стерический фактор, также как и индуктивный, указывает на более высокую активность альдегидов по сравнению с кетонами в реакциях AN. Самый активный среди карбонильных соединений – формальдегид.
Дата добавления: 2015-07-30; просмотров: 1080;
