Венозный угол; б) в подключичную вену; в) в яремную вену; г) в безымянную вену.
в венозный угол Пирогова. Этот вариант хода ГЛП объясняет возникновение Вирховских метастазов в надключичной области слева при раке желудка и поджелудочной железы.
По месту впадения ГЛП считаем целесообразным делить его на 4 варианта (рис. 42): 1) впадение ГЛП в венозный угол Пирогова (50,7%); 2) впадение ГЛП в подключичную вену (24,7%); 3) впадение ГЛП в яремную вену (10,96%); 4) впадение ГЛП в безымянную вену (4,11%).
В особую группу мы выделили редкие варианты впадения ГЛП, знание которых облегчает поиски протока и может предотвратить излишнюю травматизацию как ГЛП, так и вены (рис. 43).
Методика дренирования. Операцию можно выполнить под местной анестезией или под наркозом. Последнее, с нашей точки зрения, более предпочтительно, так как новокаин затрудняет ориентировку в тканях, а беспокойство больных во время операции ухудшает обзор операционного поля. На операционном столе под плечевой пояс кладут валик, голову больного поворачивают вправо, а левую руку укладывают вдоль туловища. Разрез делается выше и параллельно левой клю- 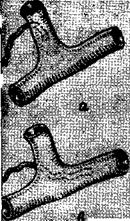

в * " 4ff"r'W«*. л. ч - ' •* -ч v^ъ*
Рис. 43. Редкие варианты впадения терминального отдела ГЛП в сочетании с анатомическими особенностями венозного утла:
Я) впадение лимфатического протока в венозное русло на задней поверхности яремной вены- б) яремная вена представлена двумя стволами, которые соединяются в единый ствол у места слияния с подключичной веной в сочетании с впадением ГЛП яа задвгв поверхности яремной вены; в) вариант впадения ГЛП на задней поверхности подключичной вены.
чице. Рассекают кожу, подкожную клетчатку, поверхностную фасцию вместе с платизмой. Рассекают поверхностный листок 1-й фасции шеи, образующей влагалище для грудино-ключично-сосковой мышцы. Поскольку наружная ножка этой мышцы прикрывает венозный угол Пирогова, целесообразно частично ее пересечь и отвести мышцу кнутри. После этого обнажают собственную фасцию шеи, отводят лопаточно-подъязычную мышцу кнаружи и рассекают фасцию на протяжении 5—6 см вдоль наружного края внутренней яремной вены. Вена выделяется на протяжении 3—4 см и берется на турникет. Этот прием ведет к гипертензии в протоке, его увеличению в диаметре и более четкому кон-турированию (рис. 44). Поиски ГЛП облегчаются при выделении шейного лимфатического ствола, который бывает легче обнаружить по наружному краю внутренней яремной вены. Шейный лимфатический ствол в 42,5% случаев сливался с ГЛП перед впадением его в венозное русло. При отсутствии ГЛП в «типичном» месте внутреннюю яремную вену отводят кнаружи, а выделенную сонную артерию и блуждающий нерв — кнутри и продолжают поиск протока в предлестничной

Рис.44. Методика дренирования ГЛП:
а) взятие внутренней яремной вены на держалку; б) взятие грудного лимфатического протока на держалку; в) канюляция ГЛП; г) турникет на устье ГЛП с фиксацией к коже на марлевом шарике.
клетчатке. Далее проток не следует выделять на значительном протяжении (не более 1,5 см), так как это приводит в дальнейшем к его облитерации. При магистральном типе ГЛП канюляцию его по возможности производили по типу дренажа Мейо, как при дренировании холедоха. Дренаж в стенке протока фиксировался П-образным швом атравматической иглой. При подобном методе канюляции сохраняется естественный ток лимфы после удаления трубки. При древовидном типе ГЛП производилась канюляция наиболее широкого ствола по методу Мейо, если позволял диаметр протока. При недостаточном для введения катетера по Мейо диаметре протока он пересекался, проксимальная часть его канюлировалась, а дистальная — перевязывалась. Подобной же методики мы придерживались и при рассыпном типе ГЛП.
Усиление эффективности лимфодренажа. Одной из важнейших задач дренирования ГЛП является максимальный сброс лимфы в первые часы и дни после операции для получения выраженного дезинтоксикационного эффекта. Оказалось, что выведение лимфы в объеме 500—700 мл часто не оказывает выраженного влияния на клинические и лабораторные показатели. Поэтому нужны дополнительные меры для увеличения коэффициента полезного действия лимфодренажа. Сотрудники нашей клиники Ф. А. Давлеткильдеев и Б. X. Ким разработали и применили на практике методику дозированного и управляемого дренирования ГЛП. Управляемое дренирование ГЛП складывается из следующих элементов: 1) вышеуказанным расположением трубок в протоке в зависимости от типов его строения; 2) изменением высоты расположения катетера по отношению к больному; 3) медикаментозной стимуляцией протока; 4) наложением турникета на концевую часть протока; 5) лимфосорбцией.
При этом установлено, что лимфоток можно усилить лекарственным путем. Для этих целей была применена интенсивная водно-электролитная нагрузка, полиглюкин, преднизолон, маннитол, используя способность этих препаратов быстро повышать осмотическое давление плазмы (А. Н. Шанская, 1975.). Это приводит к усиленному притоку интерстициальной жидкости в сосудистое русло, увеличивает объем циркулирующей крови, улучшает гемодинамику и снижает гематокрит. Введение маннитола из расчета 1,0 г на кг веса приводит через 10—15 минут после его введения к увеличению лимфотока на 100% и более в течение 4—5 часов. Особенно эффективен этот способ при несколько пониженной лимфопродукции, наблюдающейся в токсической фазе перитонита.
Следовательно, используя маннитол, можно усилить дезинтоксикационный эффект дренирования грудного протока, ускоряя лимфоток и увеличивая объем выводимой лимфы. Это позволяет более интенсивно проводить предоперационную подготовку и сократить время до операции. Этим методом целесообразно пользоваться в случаях, когда естественный лимфоток снижен, выделяется густая и вязкая лимфа, что имеет место при холангитах, или содержит большое количество эритроцитов, как это бывает при панкреатитах и перитонитах.
При ранее описанном методе канюляции различных типов ГЛП лимфодренаж часто бывает недостаточным за счет сохранения естественного тока лимфы при магистральном типе и по дополнительным путям при древовидном и рассыпном типах, что снижает дезинтоксикационный эффект операции. Поэтому мы разработали методику усиления лимфотока с помощью наложения временного турникета на устье протока при магистральном и древовидном типах ГЛП, а также на дополнительные ветви при рассыпном типе. Нами установлено, что лишь одно перекрытие протока с помощью турникета ведет к увеличению лимфотока по катетеру на 30% по отношению к исходному уровню. Для этого турникет, наложенный на проток, подтягивается к кожной ране и фиксируется на коже к марлевому шарику. При сочетании турникетного метода с медикаментозной стимуляцией лимфотока выделение лимфы можно увеличить в 2,5 раза.
В последующем, когда необходимость в лимфостомии отпадает, турникет удаляется и восстанавливается естественный ток лимфы. Однако в связи с массивной потерей белка вместе с лимфой возникает опасность нарушения гемодинамики и угнетения за счет гипопро-теинемии антитоксической функции печени.
Осложнения при дренировании ГЛП и их профилактика. Операции дренирования ГЛП опасны осложнениями, связанными как с самим оперативным вмешательством, так и с проведением лимфодренажа в послеоперационном периоде, с прекращением лимфодренажа . и деканюляцией ГЛП.
Осложнения, связанные с оперативным вмешательством. Повреждение сосудов в нашей практике встретилось 2 раза. Один раз была повреждена подключичная вена при редком варианте впадения ГЛП (проток впадал в заднюю поверхность подключичной вены). Второй раз была травмирована стенка внутренней яремной вены, которая была представлена в виде двух стволов. Дефекты в стенках вен после их сдавления были сшиты атравматическими иглами. Воздушной эмболии не наблюдалось, и послеоперационный период протекал без осложнений. Профилактикой подобных осложнений являются знание анатомических вариантов ГЛП, вкрытие фасциального влагалища внутренней яремной вены со взятием последней на турникет. Повреждение плевры имело место в одном случае с развитием незначительного пневмоторакса, который самостоятельно разрешился.на третьи сутки. Указанное осложнение было связано с высоким стоянием купола плевры у больной с пикнической конституцией и редким вариантом ГЛП.
Подтекание лимфы между швами раны помимо катетера встретилось в нашей практике 3 раза и прекратилось спонтанно без дополнительных вмешательств.
Осложнения, связанные с проведением лимфодренажа. Острая гипотония наблюдалась дважды, сочетаясь с активной стимуляцией лимфотока и большой потерей лимфы. При этом отмечалось резкое падение артериального давления на почве гиповолемии из-за неадекватной инфузионной терапии. После интенсивной коррекции ОЦК, которая включала введение полиглюкина, реополиглюкина, гидрокортизона, растворов белка, глюкозы и реинфузии очищенной лимфы, состояние больных нормализовалось.
Выпадения катетера из ГЛП мы наблюдали в 3 случаях. Оно во всех случаях было следствием технических ошибок — фиксации катетера к кивательной мышце, что вызывало натяжение катетера при движении больного шеей и выпадение его. С целью профилактики подобных ошибок нужно пользоваться фиксацией катетера к коже рядом с наложенными на рану швами.
Осложнения, связанные с прекращением лимфо-дренажа и деканюляцией протока. Лимфоистечение, продолжающееся через раневой канал после деканюляции протока, наблюдалось дважды. Оба больных были оперированы повторно с целью ревизии раны и остановки лимфоистечения. Для профилактики этого осложнения мы производили поэтапную деканюляцию, включающую снятие превентивного турникета, ранее наложенного на устье ГЛП, создание градиента давления за счет поднятого катетера над уровнем койки больного на 1—2 суток. Далее катетер полностью перекрывается и при отсутствии жалоб на усиление болей в животе удаляется.
Лимфосорбция и влияние ее на некоторые иммунологические показатели. Дренирование ГЛП наряду с выраженным дезинтоксикащюнным эффектом имеет и теневые стороны. Недостатки дренажа ГЛП клинически проявляются неярко, часто проходят незаметно, но не становятся отсюда безразличными для больного. Одним из них и наиболее существенным является большая потеря белка, электролитов, ферментов и иммунокомпетентных клеток. В среднем в каждыми 1000 мл выведенной лимфы теряется 50—60 г аутобелка, вместо которого приходится вводить 1000—1200 мл 4% раствора протеина или 500—600 мл 10% альбумина. Но при стимуляции лимфореза за сутки выделяется от 1500 до 3000 мл лимфы, что ведет неизбежно к увеличению заместительной терапии чужеродными белками, которые не могут полноценно заменить потерянное. Отсюда и возникла идея очищения лимфы и реинфузии ее обратно в организм. Этот метод, разработанный Р. Т. Панченко и соавт. (1976), получил название лимфосорбции.
В процессе лимфосорбции решаются 3 основные задачи: 1) сбор и консервация лимфы; 2) методика очищения лимфы с выбором оптимальных сорбентов и их сочетаний; 3) выбор метода реинфузии.
Лимфосорбция нами была применена у 48 больных:у 23 — с механической желтухой, у 20 — с панкреатитом, у 3— с перитонитом, у 2 — с кишечной непроходимостью. Для лимфосорбции использовались активированные угли типа СКТ-6 и БАУ и катионит КУ-2-8 в натриевой форме (О. С. Кочнев, А. П. Цыбулькин, \, Ф. А. Давлеткильдеев, Ф. X. Гимадутдинова). Лимфа для реабилитации собиралась в стерильные 0,5 л сосуды с герметичной крышкой, которые обычно используются для хранения стерильных инфузионных растворов. В пробку вставляли две короткие иглы Дюфо, вводили 1 мл гепарина и в одну из игл проводили катетер из ГЛП. После наполнения сосуда лимфой его хранили в холодильнике. Реинфузию начинали после выведения 1000 мл лимфы. В ходе лимфосорбции проводился контроль за общим белком и белковыми фракциями, А/Г коэффициентом, показателями билирубина, диастазы, аммиака.
При использовании активированных углей существенных изменений со стороны белковых фракций до и после очищения лимфы не наступает. Более того, наблюдается тенденция к нормализации А/Г коэффициента. При этом белковые потери составляли в среднем 7%, очищение лимфы от билирубина происходило на 32%. Аммиак поглощается активированными углями на 50%, а диастаза — на 87%. Таким образом, сорбция билирубина и аммиака при использовании активированных углей явно недостаточна.
При применении катеонита КУ-2-8 в качестве сорбента белковые потери составляли 2,2, сорбция билирубина — 14,4%. Очищение лимфы от аммиака при этом методе происходило на 77,3, диастазы — на 84%. Поскольку этот метод сорбции применялся у больных с механической желтухой и панкреатитом, осложненном желтухой, его результаты нельзя считать хорошими, так как лимфа в недостаточной степени очищается от одного из основных компонентов токсемии характерных для этих патологических состояний.
Для повышения эффективности детоксикация лимфы нами у 25 больных применен комбинированный фильтр с одновременным использованием двух сорбентов — КУ-2-8 и СКТ-6. Лимфосорбция проводилась путем фильтрования лимфы через два слоя сорбентов в стеклянной колонке емкостью до 1 литра. Количество используемых сорбентов составляло 50 г. На каждые 500 мл лимфы с добавлением 1 млн. ЕД пенициллина. Очищенная лимфа вводилась через подключичный катетер со скоростью 40—60 капель в минуту. При использовании комбинированного фильтра белковые потери увеличивались до 29,3%, в то же время сорбция билирубина составляла 42,1, освобождение лимфы от аммиака возрастало до 29,2, а от амилазы — до 91,7%. Таким образом, применение данного фильтра облегчало процесс лимфосорбции и реинфузии лимфы и увеличивало дезинтоксикационный эффект.
Сотрудник нашей клиники Ф. А. Давлеткильдеев совместно с А. П. Цыбулькиным и Ф. X. Гимадутдиновой изучил степень лимфоцитарных популяционных потерь и распределение Т- и В-лимфоцитов в системе периферическая кровь — лимфа в динамике дренирования ГЛП с использованием для лимфосорбции комбинированного фильтра. Проводился ежесуточный количественный анализ объема Т- и В-лимфоцитарных популяций потерь при лимфосорбции и сопутствующих изменений в числе популяций лимфоцитов в периферической крови и лимфе грудного протока. Т-лимфоциты определялись в тесте спонтанного розеткообразования с эритроцитами барана, В-лимфоциты тестировались по наличию на их поверхности рецепторов к СЗ компоненту комплемента (Р. В. Петров и саавт., 1976). Кроме того, измерялся объем выделяемой лимфы, npoцент задержки Т- и В-популяций лимфоцитов на колонке адсорбентов, а также функциональная активностьсть Т-лимфоцитов фильтрата лимфы в тесте митогенной трансформации с морфологическим учетом образующихся бластов (Н. Р. Линг, 1971).
Результаты исследования по величине популяционныхлимфоцитарных потерь приведены в табл. 12. Интересной особенностью процесса на ранних сроках дренажа является уменьшенный выход лимфоидных клеток через ГЛП. Данный факт не был связан со снижением объема выделяемой лимфы, он объясняется временным подавлением рециркуляции малых лимфоцитов на ранних сроках после операционной травмы. Подтверждением тому является отчетливая лимфоцитопения
Таблица 12
Дата добавления: 2015-07-24; просмотров: 1693;
