Примеры решения задач. Задача 1.Рассчитать концентрацию ионов водорода в растворе HCN (См = 10-3 М ), если a = 4,2∙10-3.
Задача 1.Рассчитать концентрацию ионов водорода в растворе HCN (См = 10-3 М ), если a = 4,2∙10-3.
Решение:Диссоциация цианистоводородной кислоты протекает по уравнению HCN ↔ H+ + CN-; концентрации ионов [H+] и [CN-] в растворе равны между собой ( т.к. nН+ : nСN- = 1:1, где
n - стехиометрические коэффициенты) т.е. [H+] = [CN-] = a Cм, моль/л; Тогда [H+] = [CN-] = 4,2∙10-3∙ 10-3 = 4,2×10-7 моль/л.
Задача 2.Рассчитать концентрацию ионов водорода и гидроксид-ионов в рстворе NH4OH, концентрацией См= 0,01М, если Кд= 1,8×10-5.
Решение: Гидроксид аммония диссоциирует следующим образом:
NH4OH ↔ NH4+ + OH-, константа диссоциации имеет вид
Кд= 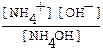 ;
;
концентрации ионов аммония [NН4+] и гидроксида [OH-] совпадают (n (NH4+) :n (OH-) = 1:1), обозначим их за х:
[NH4+] = [OH-] = х моль/л, тогда выражение для Кд примет вид
1,8×10-5 = х2/ 0,01-х. Считая, что х << См, решаем уравнение
1,8×10-5=x2/ 0,01, относительно х: х = 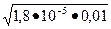 =4,2∙10-4моль/л; [OH-]= 4,2∙10-4 моль/л.
=4,2∙10-4моль/л; [OH-]= 4,2∙10-4 моль/л.
Концентрации ионов водорода и гидроксида связаны через ионное произведение воды Кw= [H+][OH-] =10-14, выразим концентрацию ионов водорода [H+] = Kw/[OH-] и рассчитаем её значение:
[H+]=1×10-14/4,2×10-4 = 2,3×10-11моль/л.
Задача 3. Определить рН раствора НСl (a=1), если См =2∙10-3 М
Решение: Диссоциация соляной кислоты протекает по уравнению
HCl ® H+ + Cl-, концентрация ионов водорода [H+] = a Cм =1∙2∙10-3 = =2∙10-3 моль/л. Водородный показатель рН = - lg[H+] = - lg2∙10-3 = 2,7.
Задача 4. Определить молярную концентрацию гидроксида аммония, если рН=11, а Кд=1,8∙10-5.
Решение: Концентрация ионов водорода [H+]=10-pH=10-11моль/л. Из ионного произведения воды определяем концентрацию [OH-] = Kw / [H+] = 10-14/10-11=10-3моль/л. Гидроксид аммония - слабое основание и характеризуется уравнением реакции диссоциации
NH4OH ↔ NH4+ + OH-. Выражение для константы диссоциации
Кд=. 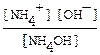
из закона Оствальда следует, что [NH4+ ] = [OH-] = a∙Cм, а Кд = a2См. Объединяя уравнения, получимСм=[OH-]2/Kд = 10-6/ 1.8∙10-5 = 0,056 моль/л
Дата добавления: 2015-07-22; просмотров: 1255;
