Неорганические вещества клетки
| Вода |
Вода — самое распространенное в живых организмах неорганическое соединение. Ее содержание колеблется в широких пределах: в клетках эмали зубов вода составляет по массе около 10%, а в клетках развивающегося зародыша — более 90%.
Без воды жизнь невозможна. Она не только обязательный компонент живых клеток, но и среда обитания организмов. Биологическое значение воды основано на ее химических и физических свойствах.
| Физические и химические свойства воды |
Химические и физические свойства воды необычны. Они объясняются, прежде всего, малыми размерами молекул воды, их полярностью и способностью соединяться друг с другом водородными связями.
В молекуле воды один атом кислорода ковалентно связан с двумя атомами водорода. Молекула полярна: кислородный атом несет частичный отрицательный заряд, а два водородных — частично положительные заряды. Это делает молекулу воды диполем. Поэтому при взаимодействии молекул воды друг с другом между ними устанавливаются водородные связи. Они слабее ковалентной, но, поскольку каждая молекула воды способна образовывать 4 водородные связи, они существенно влияют на физические свойства воды. Большая теплоемкость, теплота плавления и теплота парообразования объясняются тем, что большая часть поглощаемого водой тепла расходуется на разрыв водородных связей между ее молекулами. Вода обладает высокой теплопроводностью. Вода практически не сжимается, прозрачна в видимом участке спектра. Наконец, вода — единственное вещество, плотность которого в жидком состоянии больше, чем в твердом.
| Биологическое значение воды |
Физические и химические свойства делают ее уникальной жидкостью и определяют ее биологическое значение.
© Вода — хороший растворитель ионных (полярных) соединений, а также некоторых не ионных, в молекуле которых присутствуют заряженные (полярные) группы. Если энергия притяжения молекул воды к молекулам какого-либо вещества больше, чем энергия притяжения между молекулами вещества, то молекулы гидратируются и вещество растворяется (рис. 256). По отношению к воде различают:
¨ гидрофильные вещества — вещества, хорошо растворимые в воде;
¨ гидрофобные вещества — вещества, практически нерастворимые в воде.
|
© Большая теплоемкость и теплопроводность воды препятствуют возникновению "горячих точек" в организме, так как способствуют равномерному распределению тепла в клетке.
© Благодаря большой теплоте испарения воды, происходит охлаждение организма.
© Плотность льда меньше плотности воды. Поэтому при замерзании водоемов подо льдом остается жизненное пространство для водных организмов.
© Благодаря силам адгезии[7] и когезии[8], вода обладает свойством капиллярности, то есть способности подниматься по капиллярам (один из факторов, обеспечивающих движение воды в сосудах растений) (рис. 254).
© Вода является непосредственным участником многих химических реакций (гиролитическое расщепление белков, углеводов, жиров и др.).
© Несжимаемость воды определяет напряженное состояние клеточных стенок (тургор), а также выполняет опорную функцию (гидростатический скелет, например, у круглых червей).
| Минеральные вещества |
Минеральные вещества клетки в основном представлены солями, которые диссоциируют на анионы и катионы, некоторые — в неионизированной форме в микродозах (Fe, Mg, Cu, Co, Ni и др.)
Для процессов жизнедеятельности клетки наиболее важны катионы Na+, Ca2+, Mg2+, анионы HPO42-, Cl-, HCO3-. Концентрации ионов в клетке и среде ее обитания, как правило, различны. Например, во внешней среде (плазме крови, морской воде) K+ всегда меньше, а Na+ всегда больше, чем в клетке. Существует ряд механизмов, позволяющих клетке поддерживать определенное соотношение ионов в протопласте и внешней среде.
Различные ионы принимают участие во многих процессах жизнедеятельности клетки:
© катионы К+, Na+, Ca2+ обеспечивают раздражимость живых организмов;
© катионы Mg2+, Mn2+, Zn2+, Ca2+ и др. необходимы для нормального функционирования многих ферментов;
© образование углеводов в процессе фотосинтеза невозможно без Mg2+ (составная часть хлорофилла);
© слабощелочная реакция содержимого клетки поддерживается анионами слабых кислот (НСО3-, НРО4-) и слабыми кислотами (Н2СО3);
© От концентрации солей внутри клетки зависят ее буферные свойства. Буферностью называют способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне. Внутри клетки буферность обеспечивается главным образом анионами H2PO4- и НРО42-. Во внеклеточной жидкости и в крови роль буфера играют Н2СО3- и НСО32-.
Фосфатная буферная система:
Низкий pH Высокий pH
НРО42- + Н+ ←―――――――→H2PO4-
Гидрофосфат — ион Дигидрофосфат — ион
Бикарбонатная буферная система:
Низкий pH Высокий pH
НСО3- + Н+ ←―――――――→H2СO3
Гидрокарбонат — ион Угольная кислота
Некоторые неорганические вещества содержатся в клетке не только в растворенном, но и в твердом состоянии. Например, Са и Р содержатся в костной ткани, в раковинах моллюсков в виде двойных углекислых и фосфорнокислых солей.
Дата добавления: 2015-07-22; просмотров: 977;

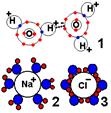 Рис 254. Свойства молекулы воды:
1 — когезия молекул воды; 2 — гидратация катиона; 3 — гидратация аниона.
Рис 254. Свойства молекулы воды:
1 — когезия молекул воды; 2 — гидратация катиона; 3 — гидратация аниона.