ГЛАВА 65. НЕБЛАГОПРИЯТНЫЕ РЕАКЦИИ НА ВВЕДЕНИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Алестер Дж. Дж. Вуд, Джон Л. Оутс (Alastair J. J. Wood, John A. Oates)
Желаемое действие лекарственных средств связано с неизбежным риском того, что они могут вызвать и неблагоприятные эффекты. Заболеваемость и смертность, обусловленные такими последствиями, часто представляют собой диагностические проблемы, поскольку все лекарственные препараты могут действовать на любой орган или систему организма.
Большие успехи, достигнутые в исследовании, развитии и разработке правил и способов применения лекарственных средств, в большинстве случаев гарантируют однородность их свойств, эффективность и относительную безопасность, а также предупреждают возможные осложнения. Однако чрезвычайно большое число и разнообразие лекарственных средств, имеющихся в свободной продаже или назначаемых врачом, ограничивают возможность получения и удержания в памяти больным или врачом всех сведений о лекарственных препаратах, необходимых для наиболее эффективного их применения. Все это расширяет возможности бесконтрольного применения населением и не всегда обоснованного назначения медицинскими работниками многих лекарственных средств.
Большинство врачей используют в своей практике не более 50 различных лекарственных средств, на опыте приобретая осведомленность об их эффективности и безопасности. Больные, как правило, применяют достаточно ограниченное число лекарственных препаратов, однако, обращаясь за помощью к нескольким врачам одновременно, от каждого из них получают назначение на какие-либо лекарственные средства. Опросы показали, что в течение одного месяца больные употребляют более трех лекарственных препаратов, содержащих девять или более различных химических веществ.
Положение осложняется тем, что 25—50% больных, чаще это люди преклонного возраста, при самостоятельном приеме назначенных врачом лекарственных средств допускают ошибки, что, как правило, приводит к неблагоприятным последствиям. Более 30% больных вообще не выполняют назначений врача. Многие люди принимают лекарственные средства, не читая имеющихся на упаковках указаний по их применению или не выполняя их. Таким образом, врачи должны осознавать, что данные ими при назначении лекарственных средств указания не всегда гарантируют, что больные будут их выполнять.
Любое лекарственное средство может вызвать нежелательные последствия даже в тех случаях, когда его будут применять в соответствии со стандартными или рекомендованными методами введения. В случае заведомо неправильного применения эффективность препарата снижается или возникает опасность развития неблагоприятных реакций. Одновременное введение нескольких лекарственных средств может вызвать неблагоприятные взаимодействия между ними и, следовательно, различные осложнения (см. гл. 64).
В условиях стационара все вводимые больным лекарственные средства и выполнение назначений врача находятся под контролем медицинского персонала. Однако и в этом случае могут произойти ошибки при введении больному лекарственных средств, иметь место неточности в дозировке, или же лекарственный препарат может быть введен не тому больному. Тем не менее установленные в больницах системы, улучающие распределение лекарственных средств и их введение больным, снизили остроту этой проблемы. Что касается амбулаторных больных, то не существует каких-либо способов проконтролировать выполнение ими режима лекарственной терапии, рекомендованного врачом.
Эпидемиология. Эпидемиологические исследования неблагоприятных реакций на лекарственные средства принесли известную пользу для оценки общей значимости этой проблемы, в деле расчета частоты неблагоприятных реакций на отдельные лекарственные средства и выявления некоторых определяющих факторов развития побочных эффектов лекарственных препаратов.
За время пребывания в стационаре больным применяют в среднем около десяти различных препаратов. Чем тяжелее состояние больного, тем больше лекарственных средств ему назначают, и следовательно, происходит соответствующее увеличение вероятности развития неблагоприятных реакций на их введение. В том случае, когда госпитализированным больным вводят меньше 6 разных препаратов, вероятность развития неблагоприятной реакции составляет 5%, но если больше 15, то вероятность развития такой реакции превышает 40%. Ретроспективный анализ результатов лечения амбулаторных больных позволил обнаружить наличие в анамнезе некоторых неблагоприятных реакций на лекарственные средства у 20% из них'.
Таким образом, значение проблемы заболеваний, индуцированных лекарственными средствами, стало чрезвычайно важным. От 2 до 5% больных поступают в терапевтические и педиатрические отделения больниц общего профиля по поводу заболеваний, связанных с реакциями на введение лекарственных средств. Соотношение между общим числом таких заболеваний и числом смертельных исходов от них у госпитализированных больных колеблется в пределах от 2 до 12%. Некоторая доля аномалий развития плода или новорожденного обусловлена лекарственными средствами, которые вводили матери во время беременности или при родах.
У женщин проявления неблагоприятных реакций на лекарственные средства со стороны пищеварительного тракта наблюдаются в два раза чаще, чем у мужчин.
Небольшая группа широко применяемых лекарственных средств является причиной непропорционально большого числа случаев неблагоприятных реакций. В ряде исследований было показано, что ацетилсалициловая кислота, дигоксин, антикоагулянты, диуретики, антимикробные средства, стероиды и противодиабетические препараты являются причиной 90% всех случаев неблагоприятных реакций на лекарственные средства.
Этиология. Большинство неблагоприятных реакций на лекарственные средства можно отнести к одной из двух групп. Самыми частыми реакциями являются те, которые возникают в результате преувеличенного, но предсказуемого фармакологического действия того или иного из них. Другие неблагоприятные реакции обусловлены токсическим действием лекарственного средства на клетки как следствие механизмов, не связанных с его ожидаемым фармакологическим действием. Поэтому такие реакции часто бывают непредсказуемыми и очень тяжелыми; они развиваются в результате действия как ряда известных, так и неустановленных механизмов. К некоторым из механизмов экстрафармакологической токсичности относятся: прямое цитотоксическое действие, инициация аномальных иммунных реакций и расстройство процессов обмена веществ у лиц, обладающих повышенной чувствительностью в результате генетических дефектов ферментной системы.
Аномальное усиление предсказуемого фармакологического действия. Путем предварительного рассмотрения известных факторов, видоизменяющих действие лекарственных средств, часто оказывается возможным предотвратить развитие этих неблагоприятных реакций.
Ненормально высокая концентрация- лекарственного средства в месте локализации рецепторов (месте действия), обусловленная вариабельностью фармакокинетики, рассмотренной в гл. 64, — обычная причина подобных реакций. Например, такие изменения, как уменьшение объема распределения, скорости метаболизма или скорости экскреции, приводят к более высокой по сравнению с ожидаемой концентрации лекарственного средства в месте локализации рецепторов, с последующим усилением фармакологического эффекта.
Изменение кривой доза — эффект, обусловленное повышенной чувствительностью рецепторов, приведет к усилению действия лекарственного средства при неизменной его концентрации. Это можно наблюдать на примере чрезмерно сильной реакции на антикоагулянт варфарин при нормальном и ниже нормального уровнях его содержания в плазме крови у лиц преклонного возраста.
Форма кривой доза — эффект сама по себе также определяет вероятность развития неблагоприятных реакций на лекарственные средства.
Препараты, характеризующиеся крутой кривой доза — эффект, с большей вероятностью связаны с возможностью токсического действия, зависящего от величины дозы, поскольку небольшое увеличение их дозы вызывает значительное изменение фармакологического эффекта. Увеличение дозы лекарственных средств, характеризуемое нелинейными кинетическими закономерностями, таких как фенитоин (см. предыдущую главу), может вызывать пропорциональное повышение уровней содержания их в плазме крови, приводящее к токсическому действию.
Лечение сопутствующим лекарственным средством может влиять на фармакокинетику или фармакодинамику другого вводимого в те же сроки препарата. На фармакокинетику влияют изменения биодоступности, связывания с белком или скорости метаболизма или экскреции. Фармакодинамика может измениться в результате конкуренции за рецепторы — из-за предотвращения попадания лекарственного средства к месту его действия или же вследствие антагонизма или усиления фармакологического действия лекарственного средства. Эти вопросы подробно рассмотрены в предыдущей главе.
Токсичность, не связанная с первичным фармакологическим действием лекарственного средства. Цитотоксические реакции. Наше понимание этих так называемых идиосинкразических реакций значительно возросло в последнее время, как только выяснилось, что многие из таких реакций обусловлены необратимым связыванием лекарственного средства или его метаболитов ковалентными электронными связями с тканевыми макромолекулами. Некоторые химические канцерогены, такие как алкилирующие вещества, соединяются непосредственно с ДНК. Однако чаще ковалентное связывание происходит только после метаболической активации лекарственного средства в химически реактивные метаболиты. Такая метаболическая активация обычно происходит в микросомальной системе оксидазы смешанного действия, ферментной системе печени, ответственной за метаболизм многих лекарственных средств (см. гл. 64). Во время метаболизма лекарственных средств этими путями некоторые из них могут образовывать реактивные метаболиты, которые ковалентными связями соединяются с тканями макромолекулами, вызывая повреждение тканей. Вследствие высокореактивной природы этих метаболитов ковалентное связывание часто происходит вблизи места их образования, например в печени, но система оксидазы смешанного действия обнаружена также в других тканях.
Примером такого типа неблагоприятных реакций на лекарственное средство является гепатотоксическое действие изониазида, который главным образом путем ацетилирования (рис. 65-1) превращается в ацетилизониазид, затем гидролизуется, образуя ацетилгидралазин. Процесс дальнейшего метаболизма ацетилгидралазина системой оксидазы смешанного действия приводит к высвобождению реактивных метаболитов, которые ковалентными связями соединяются с макромолекулами печени, вызывая некроз. Введение больному лекарственных средств, усиливающих активность системы оксидазы смешанного действия (таких как фенобарбитал или рифампицин), вместе с изониазидом связано с образованием повышенного количества реактивных метаболитов, увеличением ковалентного связывания и повреждением печени.
Некроз печени, обусловленный передозировкой парацетамола, объясняется ковалентным связыванием реактивных электрофильных метаболитов с макромолекулами печени. В норме эти реактивные метаболиты детоксицируются, образуя комплекс с глютатионом печени. При истощении запасов глютатиона происходит связывание метаболитов с макромолекулами печеночной ткани, что влечет за собой повреждение гепатоцитов. Некроз печени, вызываемый поглощением больших количеств парацетамола, можно предотвратить или по меньшей мере ослабить введением таких веществ, как N-ацетилцистеин, который снизит приводящее к некрозу связывание электрофильных метаболитов с белками печени. Повышенному риску развития некроза печени подвержены больные, которым вводят также такие лекарственные средства, как фенобарбитал, увеличивающий скорость метаболизма лекарственного средства и скорость образования токсичных метаболитов.
Не исключено, что другие идиосинкразические реакции вызываются образованием ковалентных связей между реактивными метаболитами и тканевыми макромолекулами с последующим непосредственным цитотоксическим действием или через возбуждение иммунного ответа.
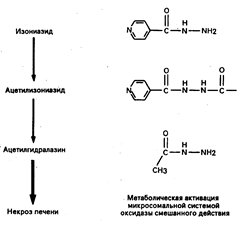
Рис. 65-1. Биотрансформация изониазида в гепатотоксический метаболит.
Иммунологические механизмы. Большинство фармакологических средств являются плохими иммуногенами, поскольку они состоят из небольших молекул с мол. массой не менее 2000. Для стимуляции синтеза антител или сенсибилизации лимфоцитов лекарственным средством или одним из его метаболитов обычно требуется активация in vivo и образование ковалентных связей с белком, углеводом или нуклеиновой кислотой.
Лекарственная стимуляция продуцирования антител может способствовать повреждению тканей посредством одного из нескольких механизмов. Антитело может атаковать лекарственное средство, прикрепленное к клетке ковалентной связью, и тем самым разрушить клетку так, как это происходит при индуцированной пенициллином гемолитической анемии. Комплексы антиген—лекарственное средство — антитело могут быть пассивно адсорбированы не участвующими в процессе клетками, которые разрушаются активацией комплемента; это происходит при тромбоцитопении, индуцированной хинином или хинидином. Лекарственные средства или их реактивные метаболиты могут изменять ткани организма хозяина, делая их антигенными, и стимулировать продуцирование аутоантител; например, апрессин и новокаинамид могут химически изменять ядерный материал клетки, стимулировать образование антиядерных антител и иногда вызывать развитие красной волчанки. Продуцирование аутоантител стимулируют такие лекарственные средства, которым не свойственно взаимодействие с антигеном хозяина или химическое сходство с тканями хозяина; например, метилдофа часто стимулирует образование антител к эритроцитам хозяина, хотя не соединяется с эритроцитами и не имеет никакого химического сходства с их антигенными детерминантами.
Сывороточная болезнь (гл. 260) является результатом отложения циркулирующих в крови комплексов лекарственное средство — антитело на эндотелиальных поверхностях. Происходит активация комплемента, локально генерируются хемотаксические факторы и в месте отложения комплекса развивается воспалительная реакция и как следствие этого — артралгии, лимфаденопатия, гломерулонефрит или энцефалит. В настоящее время самой частой причиной развития сывороточной болезни служит пенициллин. Многие лекарственные средства, особенно антимикробные вещества, индуцируют образование IgE, прикрепляющийся к мембранам тучных клеток. Контакт с лекарственным антигеном инициирует ряд последовательных биохимических процессов внутри лаброцита, в результате чего высвобождаются медиаторы, а это вызывает развитие крапивницы, стридора, ринореи, а иногда и гипотензии, характерной для анафилаксии.
Лекарственные средства также стимулируют клеточный иммунный ответ. Вещества местного применения могут взаимодействовать с сульфгидрильными или аминогруппами белков кожи и вступать в реакцию с сенсибилизированными лимфоцитами, вызывая появление сыпи, характерной для контактного дерматита. В результате взаимодействия сывороточных факторов, лекарственных средств и сенсибилизированных лимфоцитов могут появляться и другие типы сыпи. Роль активированных лекарственным средством лимфоцитов в иммунных механизмах, регулирующих разрушение тканей внутренних органов, неизвестна.
Токсичность, связаннная с генетически детерминированными дефектами ферментов. При лечении порфирии лекарственные средства, которые увеличивают активность ферментов, расположенных проксимально по отношению к недостающему ферменту в биохимической цепи синтеза порфирина, увеличивают количество его предшественников (гл. 312). Такие лекарственные средства приведены в табл. 65-1.
Таблица 65-1. Клинические проявления неблагоприятных реакций на лекарственные средства
Дата добавления: 2015-07-22; просмотров: 1242;
