Пероксиди
Крім оксидів, Оксиген здатний утворювати бінарні сполуки, які називають пероксидами. Ступінь окиснення Оксигену в пероксидах дорівнює –1, а валентність ІІ. У пероксидів атоми Оксигену сполучені між собою:
–1 –1
Н2О2 Н – О – О – Н гідрогену пероксид
–1 –1
Na2O2 Na – O – O – Na натрію пероксид
BaO2 Ba барію пероксид
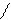 | 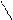 |
O – O
–1 –1
Основи
· це складні речовини, що складаються з атомів металів та гідроксогруп ОН.
Класифікація основ
1 – за розчинністю:
· розчинні (луги) – це основи лужних та лужноземельних металів:
Li Na K Rb Cs Fr
Ca Sr Ba Ra
· нерозчинні.
2 – за кількістю груп ОН:
· однокислотні NaOH, KOH
· багатокислотні Са(ОН)2, Fe(OH)2
Хімічні властивості лугів
|
| ||||
Хімічні властивості нерозчинних основ
|
|
Хімічні властивості амфотерних основ
|
|
Добування лугів:
· метал (до Мg) + вода: 2Na + 2HOH → 2NaOH + H2
Ca + 2HOH → Ca(OH)2 + H2
· оксид металу (до Мg) + вода: Na2О + Н2О → 2NaОН
CaО + Н2О → Ca(ОН)2
Добування нерозчинних основ:
· сіль + луг: CuSO4 + 2NaOH → Cu(ОН)2↓+Na2SO4
Дата добавления: 2015-08-26; просмотров: 818;
