Молочна кислота
3. Функціональні властивості вуглеводів
Найбільш важливі функціональні властивості моно - та олігосахаридів. ґрунтуються на фізико-хімічних властивостях і полягають в наступному:
- гідрофільність (гігроскопічність);
- солодкість;
- здатність зв'язувати ароматичні речовини;
- здатність утворювати продукти неферментативного потемніння;
- структуроутворювальна здатність.
Гідрофільністьзумовлена наявністю чисельних груп-ОН, які взаємодіють з водою за допомогою водневих зв'язків. Це впливає на гігроскопічність цукрів, яка є різною. Найбільшу гігроскопічність має фруктоза; сахароза і мальтоза мають приблизно однакову гігроскопічність, лактоза - найменш гігроскопічна. Це має негативне значення, наприклад, карамель, що містить багато редукувальних речовин, намокає у процесі зберігання, і позитивне використання інвертного сиропу, фруктових та зернових сиропів затримує черствіння кондитерських та хлібопекарських продуктів. Неочищені цукри більш гігроскопічні. Це пояснюється тим ,що домішки перешкоджують утворенню водневих зв'язків між молекулами цукрів і ОН-групи залишаються більш доступними для зв'язування води.
Цукри зв'язують ароматичні речовини і цим самим фіксують аромати. Особливо це важливо для летких ароматичних речовин - альдегідіів, кетонів, ефірів. Дуже важливе значення це має під час сушіння. Вищу здатність зв'язувати ароматичні речовини мають дисахариди порівняно з моносахарами. Ще вищу здатність мають вуглеводи з більшою молекулярною масою, наприклад, гуміарабік. Він утворює плівку на поверхні цих речовин і перешкоджає втраті їх за рахунок окислення та випаровування. Ця властивість використовується в технології мікрокапсулювання.
У процесі неферментативного потемніння цукрів утворюються багато летких ароматутворюючих речовин. Проте в залежності від умов реакції можуть утворюватись різні продукти: так, при реакції Д-глюкози з валіном при 100°С утворюється аромат житнього хліба, при 180°С -аромат шоколаду, при реакції Д -глюкози з проліном -при 100° С утворюється запах смаженого м'яса, а при 180°С - аромат хліба.
При одній і тій же температурі в залежності від амінокислоти, що взаємодіє з сахарами , утворюються різні продукти: при реакції Д - глюкози з метіоніном утворюються продукти , що мають запах картоплі, з цистеїном і цистіном - запах смаженого м'яса.
Солодкістьмає важливе функціональне значення. Оцінюється солодкість по відношенню до сахарози, солодкість якої приймають за 100%. Найбільшу солодкість 170% має фруктоза. Її використання дає змогу зменшити кількість цукру у харчових продуктах. Крім того, фруктоза засвоюється без інсуліну, тому вироби для діабетиків готують на фруктозі. Для створення продуктів діабетичного спрямування використовують цукрозамінники ( сорбіт, ксиліт, які є цукроспиртами), та підсолоджувачі ( сахарин, цикламати - солодкість 500 %, аспартам - солодкість 180%).
Найважливішою технологічною функцією полісахаридів у харчових продуктах є структуроутворювальна яка відіграє роль в утворенні текстури та забезпечує твердість, крихкість, щільність, в'язкість, гелеутворення. Ці властивості пов'язані з розчинністю полісахаридів. Всі розчинні полісахариди утворюють в'язкі розчини. В'язкість залежить від розміру, форми і заряду молекул. Чим більший розмір молекули, тим більша в'язкість розчину. Молекули можуть мати заряд за рахунок іонізації карбоксильних груп, присутності поліелектролітів - ефект від цього впливу на в'язкість може бути дуже великим. Усі лінійні полімери надають більшої в'язкості розчинам порівняно з розгалуженими.
В принципі, всі полісахариди можуть бути розчиненими, оскільки містять декілька функціональних груп для утворення водневих зв'язків. Але для цього треба створювати певні умови. Наприклад, молекули целюлози нерозчинні у воді, оскільки вони мають лінійну будову і взаємодіють між собою. Амілоза і амілопектин нерозчинні в холодній воді, а в гарячій амілоза розчиняється, а амілопектин набухає.
Різні полісахариди використовують у харчових технологіях як структуроутворювачі.
Целюлоза. Компонент клітинних стінок, асоціюється з різними геміцелюлозами і лігніном. В процесі дозрівання і збирання рослин відбуваються структурні зміни. Під час виготовлення харчових продуктів використовують мікрокристалічну целюлозу яка застосовується як наповнювач та структуроутворювальний компонент для виготовлення низькокалорійних продуктів , для приготування загущувачів на целюлозній основі.
Найбільш широко, як загущувач, використовуються натрієва сіль карбоксиметилцелюлози (Na - КМЦ). Її отримують шляхом обробки целюлози лугом і хлороцтовою кислотою. Вона використовується як загущувач в начинках, морозиві, фруктовому желе, приправах, сирах, м'яких сирах, у хлібопекарських виробах затримує вологу і стримує черствіння, стримує ріст кристалів цукрів у кондитерських виробах. У напоях сприяє утриманню С02. Вона також є радіозахисною та комплексоутворювальною добавкою.
Шляхом алкілювання отримують інші похідні целюлози, наприклад, метилцелюлозу, яка має підвищену розчинність і добре набухає. Для неї характерними властивостями є зниження в'язкості при підвищенні температури і здатність до гелеутворення при певній температурі, (це температура 50-100°С, при якій метилцелюлоза викристалізовується). Вона виконує функції водоутримуючого компонента), може використовуватись при виробництві продуктів з їстівними оболонками.
Крохмаль.Крохмаль здатний клейстеризуватися. У холодній воді непошкоджені крохмальні зерна нерозчинні, але можуть зв'язувати воду і частково набухати. В процесі збільшення температури руйнуються міжмолекулярні зв'язки, звільняються місця зв'язування і утворюються водневі зв'язки. Кристалічність зерен зменшується. При подальшому нагріванні в присутності великої кількості води відбувається повна втрата кристалічності, втрата обрисів крохмальних зерен, тобто відбувається клейстеризація. Температура клейстеризації залежить від розмірів зерен (великі зерна клейстеризуються при меншій температурі), від зруйнованості, від виду крохмалю (кукурудзяний, картопляний, пшеничний). Під час клейстеризації зі збільшенням температури в'язкість крохмальної суспензії зростає, що пов'язано з набуханням зерен крохмалю, а потім різко падає. Останнє пояснюється розривом і дезагрегацією крохмальних зерен. В'язкість крохмальних клейстерів, швидкість клейстеризації залежить від активності води. Присутність солей, цукрів зменшують активність води і зменшують швидкість клейстеризації та обмежують її. На швидкість клейстеризації крохмалю впливають цукри, ліпіди, жирні кислоти, які зменшують швидкість набухання крохмалю, знижують в'язкість клейстерів, зменшують силу геля.
Солі у невисоких концентраціях та кислоти ( в області рН -4,7) не справляють великого впливу на набухання крохмальних зерен. Швидкість набухання зростає при рН - 10, але такого значення рН у харчових продуктах немає. При низьких рН спостерігається частковий гідроліз крохмалю з утворенням декстринів, які не застигають. У процесі зберігання продуктів, в яких крохмаль виконує роль загущувача, може відбуватись ретроградація крохмального гелю. Цей процес пов'язаний з частковою кристалізацією клейстеру, зокрема амілози. Звільнення води, яке супроводжує ретроградацію, називається синерезисом. Така ретроградація крохмалю спостерігається при черствінні хліба. Воно пов'язана з асоціацією амілозних молекул , при тривалому зберіганні може мати місце і асоціація амілопектину. Для попередження цього процесу доцільно використовувати жир, який утворює комплекси з амілозою. Для виробів, де крохмаль використовують як загущувач, слід використовувати крохмалі, які практично не містять амілози, або фосфатні поперечно зшиті крохмалі.
В якості загущувачів використовують модифіковані крохмалі: попередньо клейстеризований крохмаль, модифікований кислотою, етерифікований крохмаль, окислені крохмалі. Вони мають здатність до швидкої регідратації, нижчу швидкість і температуру клейстеризації, меншу здатність до ретроградації. Окислені крохмалі використовуються в соусах, майонезах і як структуроутворювачі у виробництві хліба - як поліпшувачі окисної дії, які впливають на клейковину і підвищують реологічні властивості тіста, особливо, крохмаль окислений перманганатом калія (КМп 04).
Геміцелюлози.Основні геміцелюлози в харчових продуктах – крилани. Геміцелюлози мають велику здатність зв'язувати воду, приймають участь у формуванні структури тіста, позитивно впливають на об'єм хліба, затримують його черствіння. Як харчові волокна, вони не перетравлюються в шлунково-кишковому тракті, покращують перистальтику, зв'язують (адсорбують) жовчні кислоти, зменшують рівень холестерину в крові.
Пектинові речовини.Пектин походить від грецького слова "пектос" -застиглий, желеподібний. В рослинній клітині пектин відіграє структуро-утворювальну роль, а також регулює водний обмін рослин. Пектин використовується як желеутворювач при виробництві кондитерських виробів, джемів, желе. Як харчові волокна, пектин має значення у фізіології людини - поліпшує перистальтику. Крім того, пектин є детоксикантом: зв'язує токсичні елементи і радіонукліди і виводить їх із організму. Тому пектин широко використовують у виробництві продуктів лікувально-профілактичного призначення.
Комплексоутворювальна здатність пектинів залежить від ступеня метоксилювання : чим нижчий ступінь метоксилювання, тим краща комплексоутворювальна здатність. Низькометоксильовані пектини (зі ступенем метоксилювання менше 50%) наприклад, буряковий, яблучний ни-зькометоксильований (ступень метоксилювання 46%) є кращими дето-ксикантами.
Драглеутворювальна здатність пектинів залежить від:
1) ступеня полімеризації;
2) ступеня метоксилювання;
3)наявності ацетильних груп.
Чим більша молекулярна маса пектинів, тим краща желююча здатність
У високоетерифікованих пектинах водневі звязки не виникають, а проявляється ефект відштовхування, зумовлений близькістю метильних груп. Це приводить до збільшення розчинності. Драглеутворення високоетерифікованих пектинів може відбуватись завдяки двом факторам:
1) від додавання цукру ,який викликає дегідратацію пектинових молекул і сприяє їх з'єднанню;
2) зниження рН -середовища, що зменшує дисоціацію карбоксильних груп та електростатичне відштовхування (рНопт -3,2). В присутності високих концентрацій цукрів та кислот, що має місце в кондитерському виробництві, найкращу здатність до драглеутворення мають високополімеризовані пектини та високоетерифіковані пектини зі ступенем етерифікації більше 50% . У цьому разі низькоетерифіковані пектини можуть утворювати гелі за відсутності цукру або при малому його вмісті, але необхідна присутність бівалентних катіонів, наприклад, кальцію. При цьому утворюються так звані кальцієві містки, які з'єднують молекули пектину. Але небезпечним є передозування кальцію, оскільки при цьому відбувається надмірне зближення пектинових молекул і просторова структура не утворюється, може навіть мати місцеутворення осаду пектинату кальцію. Гелі цього типу використовують у технологіях низькоцукровмісних желе і джемів ,але ці гелі є крихкими та нееластичними.
Ацетильні групи (-СН3-СО-) знижують драглеутворювальну здатність пектинів. Так, в цитрусовому пектині міститься 0,37 % ацетильних груп, в яблучному - 0,45 %, в буряковому - 6-13%.
4. Роль вуглеводів в організмі
В організмі людини вуглеводи виконують цілий комплекс життєво необхідних функцій.
Найважливішими серед них слідуючі:
1. Енергетична. При змішаному типі харчування вуглеводи забезпечують понад 60% енергетичної цінності харчового раціону, тоді як за рахунок білків і жирів – лише 40%. Крім того вуглеводи, як джерело енергії, потрібні для нормального розвитку кишкової мікрофлори.
2. Пластична. Використовуються для синтезу багатьох життєво необхідних для організму людини речовин: глікогену, амінокислот, глікопротеїдів, глікозаміногліканів і інш.
3. Опірна. Глікозаміноглікани та інші вуглеводні сполуки беруть участь в утворенні органічної частини скелета, забезпечуючи його опірну функцію.
4. Регуляторна. Вуглеводи протидіють накопиченню кетонових тіл, що утворюються при окисленні жирів. Так, при порушенні обміну вуглеводів, наприклад при цукровому діабеті, розвивається ацидоз, тобто реакція міжклітинної рідини стає кислою. А клітковина, викликаючи механічне подразнення кишок, сприяє їхній перестальтиці і тим самим сприяє процесу травлення їжі.
Відчуття солодкого, яке сприймається рецепторами язика, тонізує центральну нервову систему.
5. Специфічна. Вуглеводні сполуки (гетерополісахариди) визначають антигенну відмінність груп крові. Деякі вуглеводні сполуки виконують роль рецепторів у процесах звязування різних токсинів та в проведенні нервового імпульсу. До вуглеводів, які виконують специфічні функції, належить гепарин, (полісахарид побудований з глюкуронованої кислоти, глюкозаміну і залишків сірчаної кислоти), який запобігає згортанню крові в судинах, гіалуронова кислота – перешкоджає проникненню бактерій крізь клітинну оболонку, олігосахариди материнського молока, що затримують розвиток деяких кишкових бактерій тощо.
6. Запасна. Вуглеводи здатні відкладатися у вигляді глікогену в печінці та мязах (у рослин у вигляді крохмалю та фруктозанів). У печінці глікогену може накопичуватись до 10% загальної її маси (при голодуванні вміст глікогену зменшується до 0,2%.
Середня потреба у вуглеводах складає 400-500г/добу в тому числі: крохмалю 350-400 г, у моно-та дисахаридах 50-100 г (їх слід розподілити на 3-4 прийоми по 20-25 г за один раз), у харчових баластних речовинах (целюлоза та пектинові речовини) – 25 г.
Недостатнє вживання солодких вуглеводів призводить до зменшення енергії в організмі, зниження тонусу ЦНС, послаблення уваги, зростання чутливості до холоду.
Надмірне вживання цукру сприяє карієсу зубів, порушенню нормального співвідношення між збуджувальними та гальмуючими процесами у нервовій системі дітей, що виявляється в їхній неврівноваженій поведінці. Надлишок цукру підтримує запальні процеси. Це нерідко відбувається при надмірному вживанні цукерок, коли в шлунку розвивається так звана розріджуюча секреція у відповідь на велику концентрацію цукру. Вживання значних кількостей цукру сприяє алергізації організму, спотворює нормальні реакції, наприклад на холод: замість розширення судин, яке забезпечує нагрівання шкіри, відбувається їх звуження внаслідок чого наступає охолодження з усіма наслідками.
Рекомендована норма вуглеводів повинна бути зменшена при ряді захворювань, особливо при цукровому діабеті, ожирінні, алергіях, запальних процесах.
Співвідношення між вмістом у раціоні білків, жирів та вуглеводів залежить від віку, стану здоров’я, характеру роботи.
Наприклад, для людей, зайнятих працею, що не потребує значних фізичних зусиль, оптимальним є співвідношення білків, жирів та вуглеводів як 1:0,9:4,7.
Для осіб, зайнятих фізичною працею як 1:1:5. При фізичних навантаженнях (наприклад у спортсменів) норми вуглеводів ще більш підвищені.
ПИТАННЯ ДО САМОПЕРЕВІРКИ
1. Наведіть класифікацію вуглеводів.
2. Які моноцукри мають найбільше значення в харчових технологіях?
3. Назвіть полісахариди першого порядку.
4. Яка будова полісахаридів другого порядку?
5. Назвіть найбільш важливі функціональні властивості вуглеводів.
6. Яке значення має гігроскопічність цукрів?
7. В чому проявляється структуроутворювальна дія вуглеводів?
8. Від чого залежить драглеутворювальна здатність пектинів?
9. Назвіть основні перетворення вуглеводів у харчових технологіях.
10. Поясніть механізм кислотного та ферментативного гідролізу крохмалю.
11. В яких технологіях має місце гідроліз сахарози?
12. Які реакції призводять до утворення речовин, що надають харчовим продуктам темного кольору?
13. Які фактори впливають на процес меланоідиноутворення?
14. В яких випадках реакція меланоідиноутворення є небажаною? Як можна її попередити?
15. Особливості зброджування різних вуглеводів.
16. Що таке карамелізація цукрів?
17. Перерахуйте та розкрийте функціональні властивості вуглеводів.
18. Розкрийте властивості крохмалів.
19. Розкрийте властивості пектинів.
20. Розкрийте властивості целюлози.
21. Яку роль виконують вуглеводи в організмі людини?
Рекомендована література
Основна:
1. с.122 – 184
2. с.501 – 594
3. с.41 – 51
4. с.16 – 21
Додаткова:
1. с.76 – 86
4. с.118 - 128
Тема 3
Ліпіди. Будова, властивості, їх перетворення в харчових технологіях
План
1. Будова та класифікація ліпідів, склад сирого жиру
2. Основні реакції ліпідів
3. Перетворення ліпідів у технологіях харчових продуктів
4. Біологічна цінність харчових ліпідів
5. Роль ліпідів в організмі людини
1. Будова та класифікація ліпідів
Ліпіди об’єднують велику групу різних за хімічною природою органічних речовин, які мають деякі спільні фізико-хімічні властивості.
Однією з таких спільних властивостей ліпідів є нерозчинність їх у воді і здатність добре розчинятися в органічних розчинниках – спирті, ефірі, хлороформі, ацетоні, бензолі і інших розчинниках.
За хімічним складом та фізико-хімічними властивостями ліпіди поділяють на дві групи: - прості і складні.
До простих ліпідів відносять ліпіди, які побудовані із залишків спиртів і вищих жирних кислот. Найпоширенішими з цієї групи ліпідів є нейтральні жири (гліцериди), стериди і воски.
Класифікація ліпідів

Група складних ліпідів характеризується наявністю в їхній молекулі крім спиртів і вищих жирних кислот фосфорної або сірчаної кислоти, азотистих речовин, вуглеводів та деяких інших компонентів. Основними представниками цієї групи ліпідів є фосфоліпіди, гліколіпіди.
Прості ліпіди
|
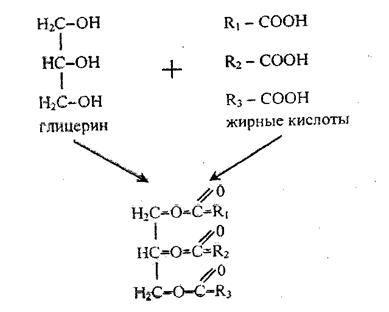
Нейтральні жири (гліцериди) – це складні ефіри трьохатомного спирту гліцерину і жирних кислот.
Утворення жирів з гліцерину та жирних кислот відбувається за слідуючою схемою:
Якщо в гліцерині всі три спиртові групи етерифіковані жирними кислотами, то такі сполуки називають тригліцеридами, якщо дві групи - дигліцеридами і якщо етерифікована одна спиртова група - моно гліцеридами:
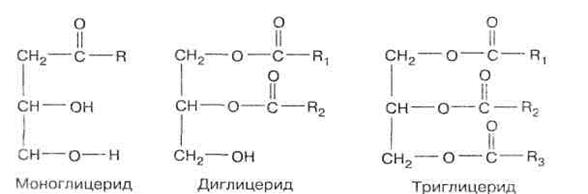
|
Вищі жирні кислоти в жирах представлені головним чином насиченими і ненасиченими ациклічними карбоновими кислотами.
Більшість карбонових кислот, що входять до склау жирів, мають парне число вуглецевих атомів.
Насичені жирні кислоти
Масляна – СН3 (СН2)2 – СООН (  )
)
Капронова – СН3(СН2)4 – СООН ( 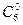 )
)
Каприлова – СН3(СН2)6 – СООН ( 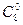 )
) 


Капринова – СН3(СН2)8 – СООН ( 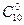 )
)
Лауринова – СН3(СН2)10 – СООН ( 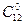 )
)
Міристинова – СН3(СН2)12 – СООН ( 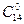 )
)
Пальмітинова – СН3(СН2)14 – СООН ( 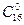 )
)
Стеаринова – СН3(СН2)16 – СООН (  )
)
Арахінова – СН3(СН2)18 – СООН ( 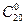 )
)
Бегенова – СН3(СН2)20 – СООН ( 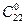 )
)
Лігноцеринова – СН3(СН2)22 – СООН ( 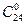 )
)
Церотинова – СН3(СН2)24 – СООН ( 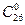 )
)
Ненасичені жині кислоти
Кротонова – СН3 – СН=СН – СООН ( 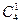 )
)
Пальмітоолеїнова – СН3 – (СН2)5 – СН=СН – (СН2)7 – СООН ( 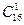 )
)
Олеїнова – СН3 – (СН2)7 – СН=СН – (СН2)7 – СООН ( 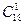 )
)
Ерукова – СН3 – (СН2)7 – СН=СН – (СН2)11 – СООН ( 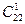 )
)
Нервонова – СН3 – (СН2)7 – СН=СН – (СН2)13 – СООН ( 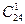 )
)
Лінолева – СН3 – (СН2)4 – СН=СН – СН2 – СН=СН – (СН2)7 – СООН ( 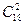 )
)
Ліноленова – СН3 –СН2– СН=СН – СН2 – СН=СН – СН2 – СН=СН – (СН2)7 – СООН ( 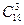 )
)
Арахідонова - СН3 – (СН2)4 – (СН=СН2)3 – СН=СН – (СН2)3 – СООН ( 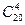 )
)
Схематично жирні монокарбонові кислоти можна представити у вигляді R-СООН, де –СООН – карбоксильна група чи карбоксил, а друга R – вуглеводневий радикал.
Карбоксил являє собою функціональну групу характерну для органічних кислот. У карбоксилі формально можна розрізнити дві групи атомів – гідроксильну і карбонільну: С= О карбоніл; ОН-гідроксил.
Гідроксил і карбоніл входять до складу молекул деяких інших класів органічних речовин, в яких вони проявляють інші властивості, ніж знаходячись у складі карбоксила.
Жирні кислоти відрізняються між собою температурою плавлення і здатністю розчинятися у воді і органічних розчинниках. Збільшення числа вуглецевих атомів у молекулах насичених жирних кислот супроводжується підвищенням їх температури плавлення. Наприклад, tпл каприлової кислоти ( 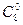 ) становить +16°С, лауринової (
) становить +16°С, лауринової ( 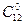 ) + 43,5°С, стеаринової (
) + 43,5°С, стеаринової (  ) + 69,6°С. Збільшення числа подвійних зв’язків у молекулах ненасичених жирних кислот призводить до зниження їх температури плавлення. Жирні кислоти з довгим ланцюгом практично не розчинні у воді. Їх натрієві і калієві солі утворюють у воді міцели.
) + 69,6°С. Збільшення числа подвійних зв’язків у молекулах ненасичених жирних кислот призводить до зниження їх температури плавлення. Жирні кислоти з довгим ланцюгом практично не розчинні у воді. Їх натрієві і калієві солі утворюють у воді міцели.
Доведено, що деякі ненасичені жирні кислоти не синтезуються в організмі людини і тварин або утворюються у недостатній кількості. Тому їх називають незамінними, або есенціальними кислотами.
До таких жирних кислот відносять лінолеву, ліноленову, арахідонову та деякі інші вищі жирні кислоти. Основним джерелом наповнення ними організму людини є льняна, конопляна, кукурудзяна і соняшникова олії.
Найбільшу групу ліпідів складають ацилгліцерини, власне вони є жирами і маслами. До складу жирів входять тригіцерини, дигліцерини, моногліцерини. Тригліцерини, в основному, містять залишки різних жирних кислот, але іноді містять залишки однакових жирних кислот.
Чисті ацилгліцерини – це безбарвні речовини без смаку і запаху. Забарвлення, смак і запах природних жирів залежить від домішок.
При вилученні ліпідів із олійної сировини в олію переходить велика група супутніх жиророзчинних речовин. Ця суміш носить назву сирого жиру.
Восками називають складні ефіри вищих спиртів і вищих жирних кислот. За фізико-хімічними властивостями воски близькі до жирів. Вони більш стійки проти дії світла, окислювачів, нагрівання, складніше піддаються гідролізу.
Природні воски, крім складних ефірів, містять певну кількість вільних вищих спиртів і вищих жирних кислот, а також невелику кількість вуглеводів, барвників та пахучих речовин. Загальна кількість цих домішок може досягти 50%.
Дата добавления: 2015-08-26; просмотров: 1567;
