L-аминокислота D-аминокислота
Рис. 1.4. L и D оптические изомеры α-аминокислот
Считают, что кислота относится к L-ряду, если в написании фишеровской проекции аминогруппа расположена слева (рис. 1.4).
Все природные аминокислоты, входящие в состав белков, относятся именно к L-ряду.
Вся белковая жизнь на земле – «левая». Есть и «исключения», но они только подтверждают правило. Оказывается, D-аминокислоты крайне редко, но все же встречаются в природе.
Например, они присутствуют в оболочке бактерии, которая является возбудителем сибирской язвы. Именно поэтому оболочка бактерии не разрушается ферментами, разрывающими белковые цепи L-аминокислот.
Из 20 α-аминокислот, входящих в состав белков:
1) 17 обладают одним ассиметричным атомом углерода;
2) одна не содержит ассиметричного атома углерода: глицин;
3) две имеют два ассиметричных атома углерода: изолейцин и треонин.
1.5.1.3. Классификация α-аминокислот
В настоящее время существуют различные классификации
α-аминокислот.
В зависимости от строения бокового радикала аминокислоты подразделяют на:
1) неполярные (гидрофобные), содержат неполярный гидрофобный радикал (линейную или разветвленную углеводородную цепочку или ароматическое кольцо);
2) полярные (гидрофильные) незаряженные,содержат полярный гидрофильный радикал (полярные группы: -OH; -NH2; -SH);
3) полярные заряженные, содержат заряженный боковой радикал (заряженные группы : -NH3+и-COO-).
Наиболее распространенные α-аминокислоты приведены на Рис. 1.5:
НЕПОЛЯРНЫЕ АМИНОКИСЛОТЫ 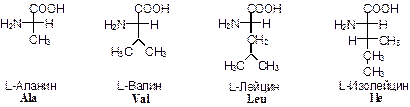
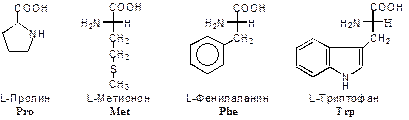
Дата добавления: 2015-07-22; просмотров: 2197;
