ГОРЕНИЕ И КАТАЛИТИЧЕСКОЕ ОКИСЛЕНИЕ
Как и другие углеводороды, алканы горят на воздухе сообразованием углекислого газа и воды:
СН4 + 2О2 = СО2 + 2Н2О + 882 кДж
C8H18 + 12,5O2 = 8CO2 + 9H2O + 5470 кДж
Количество выделяющейся при горении алканов теплоты очень велико, поэтому их использование в качестве энергоносителей так привлекательно. Однако надо помнить, что смеси метана и других газообразных алканов с воздухом взрывоопасны, и соблюдать осторожность при пользовании бытовым газом, бензином и т.д.
В обычных условиях алканы устойчивы к действию таких лабораторных окислителей, как перманганат и дихромат калия, хромовая смесь и т.д. В то же время реакции неполного каталитического окисления используются в промышленности для получения кислородсодержащих соединений – спиртов, альдегидов, карбоновых кислот.
Например, из бутана путем окисления кислородом воздуха в присутствии катализаторов получают уксусную кислоту:
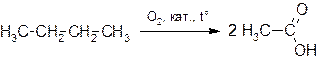
Дата добавления: 2015-08-21; просмотров: 1699;
