СТРОЕНИЕ МОЛЕКУЛ АЛКАНОВ
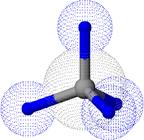
Каждый атом углерода в молекулах алканов образует четыре простые σ-связис атомами водорода или другими атомами углерода. Электронные орбитали атомов углерода находятся в состоянии sp3-гибридизации.Гибридные орбитали, а, значит, и связи каждого атома углерода направлены к вершинам тетраэдра (рис. 1).
 |
 а
а
| б |
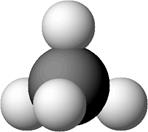
Рисунок 1. Модели молекул метана: а – полусферическая; б – шаростержневая (показано распределение электронной плотности).
Валентный угол в молекуле метана и его гомологов составляет 109,5◦. Поэтому углеродная цепь в молекулах алканов имеет зигзагообразную форму:
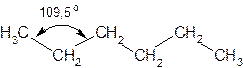
Вокруг σ-связей С-С возможно вращение, в результате которого молекулы могут принимать различные формы, называемые конформациями (рис. 2).
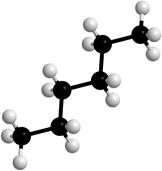
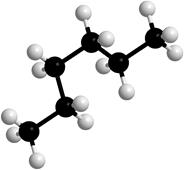
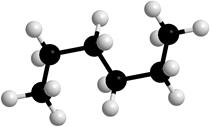
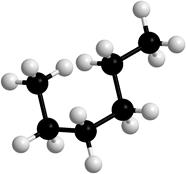
Рисунок 2. Модели молекулы гексана в разных конформациях.
Углеродный скелет молекул алканов может иметь как нормальное, так и разветвленное строение. В молекулах гомологов метана различают первичные, вторичные, третичные и четвертичные атомы углерода (см. приложение 1).
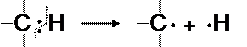
Связи С-С в молекулах алканов являются ковалентными неполярными, а связи С-Н – ковалентными полярными. Однако значения электроотрицательности атомов углерода и водорода близки и равны соответственно 2,5 и 2,1 по Полингу. Поэтому по свойствам связьС-Н близка к неполярной и проявляет склонность к гомолитическому разрыву с образованием свободных радикалов:
 .
.
Следовательно, для алканов характерны реакции, протекающие по радикальному механизму.
Дата добавления: 2015-08-21; просмотров: 1906;
