Извлечение галлия из растворов экстракцией
Для извлечения галлия из растворов в зависимости от его ионного состояния используют экстрагенты различных классов. Наибольшее изучена экстракция галлия из солянокислых растворов нейтральными экстрагентами. Галлий извлекается ими по сольватному механизму в виде комплексов GaCl3· nS или при высоких концентрациях соляной кислоты — по гидратно-сольватному в виде [H(H2О)mSn]GaCl4.
В России и за рубежом в промышленности галлий экстрагируют преимущественно из солянокислых растворов. Из растворов в других минеральных кислотах галлий экстрагируется очень плохо Для этой цели используется только трибутилфосфат. При экстракции из солянокислых растворов коэффициент распределения галлия (D) увеличивается при повышении концентрации НС1.
Введение в раствор других кислот (соляной в количестве, немного превышающем необходимое для образования HGaCl4), увеличивает коэффициенты распределения на несколько порядков. При этом экстрагируются чисто хлоридные комплексы, смешанные комплексы не образуются. В системе, имеющей наибольшее практическое значение H2SО4—НС1, замена части соляной кислоты на серную не снижает извлечения галлия и удешевляет технологический процесс. При экстракции из сернокислых растворов в промышленности необходимую концентрацию ионов СГ получают добавлением NaCl.
Для регулирования технологических свойств органической фазы (плотности, вязкости, поверхностного натяжения), влияющих на кинетику диффузионного переноса вещества из одной фазы в другую и скорость расслаивания фаз, в экстракционных процессах используют растворы экстрагентов в органических жидких веществах, которые сами не взаимодействуют с экстрагируемым веществом, но позволяют улучшить физико-химические свойства раствора. В промышленности в качестве такого растворителя (разбавителя) используют керосин.
Алюминий, не имеющий d-электронов, в отличие от Ga и In обладает малой способностью к комплексообразованию. Это свойство особенно характерно при взаимодействии алюминия с лигандами — слабыми комплексообразователями, к числу которых относятся ионы хлорид и нитрат. В результате при экстракции в присутствии соляной кислоты коэффициент распределения алюминия на много порядков меньше, чем для галлия. Вследствие этого хлорид и нитрат алюминия Достаточно широко используются в качестве высаливателей при экстракции многих элементов.
В технологических растворах кроме алюминия и галлия присутствуют и многие другие примеси (Fe, As, Сu, Zn и др.). Концентрации некоторых из них могут быть во много раз больше концентрации галлия. Одной из таких примесей является железо, которое может присутствовать в виде Fe(III), Fe(II) и их смесей. Железо(III) образует в солянокислых растворах комплексы HFeCl4 того же типа, что и HGaCl4; это в значительной степени определяет сходство их поведения при экстракции. Железо (II) в отличие от железа (III) экстрагируется плохо. При совместной экстракции с галлием FeCl2 действует как высаливатель. Для восстановления Fe(III) могут быть использованы железный скрап, стружка, порошки железа и алюминия и др.
Экстракция примесей, не отличающихся склонностью к образованию устойчивых хлорметаллатных комплексов (Ni, Mg, Са и др.), подавляется в присутствии больших концентраций хорошо экстрагирующимся железом(III). Крайне нежелательной примесью является мышьяк, присутствующий в растворах в виде As(III) и As(V). Из растворов с концентрацией НС1 > 6 моль/л и 0,13 г/л As хорошо экстрагируется AsCl3.
В качестве примера рассмотрим извлечение галлия экстракцией ТБФ при переработке зольных уносов выщелачиванием серной и соляной кислотами (рисунок 4.4). Зольные уносы, образующиеся при газификации и сжигании каменных углей, содержат галлия от 50 до 350 г/т. Их выщелачивают серной кислотой (~8 моль/л) при 120°С в течение 2 ч; при этом в раствор переводится до 96% галлия. Из макрокомпонентов переходят в раствор Al, Fe, Mg, Ti и микрокомпоненты Zn, Pb, Cd, Mo, Cu, As, Ge, Sb.
Экстракцию проводят 15%-ным раствором ТБФ в керосине, что Уменьшает его потери с водной фазой и улучшает очистку от примесей. Для экстракции раствор разбавляют соляной кислотой так, чтобы концентрация серной и соляной кислот составляла, соответственно ~4 и ~1,5 моль/л. Концентрация галлия в растворе от 10 до 80 мг/л (в среднем 30 мг/л). В результате однократной экстракции в органическую фазу извлекается 95—98% галлия. Из макрокомпонентов только железо переходит в экстракт в большом количестве, его концентрация в органической фазе— до 1,3 моль/л. Хорошо экстрагирующееся железо подавляет экстракцию микрокомпонентов, практически из них в экстракте присутствуют только As и Ge.
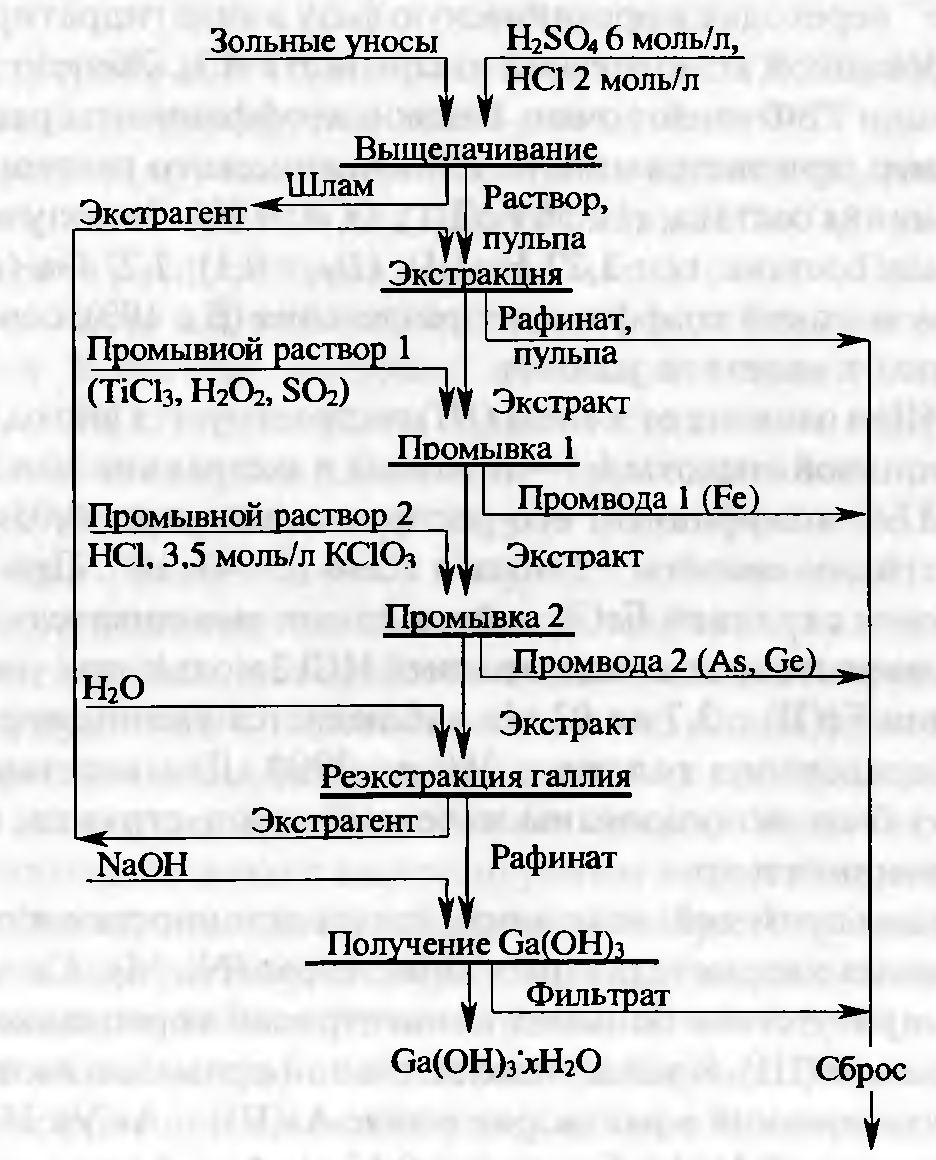
Рисунок 4.4 — Принципиальная схема извлечения галлия при переработке зольных уносов сжигания каменных углей.
Удаление из экстракта Fe, As и Ge достигается на стадии промывки. Первым удаляется железо промывкой экстракта селективным растворителем, содержащим восстановители (TiCl3 или Н2О2). В результате однократной промывки удаляется 99,9% железа. Для удаления мышьяка экстракт промывают соляной кислотой концентрацией 3,5 моль/л, содержащей окислитель, например КСlO3. За одну ступень удаляется более 90% мышьяка. Вместе с мышьяком удаляется и большая часть германия. Выделение галлия из экстракта осуществляется реэкстракцией водой при О:В > 1, что позволяет повысить концентрацию галлия в реэкстракте. Из реэкстракта можно получить электролизом металлический галлий или осадить гидроксид, в который извлекается до 85% галлия.
Извлечение галлия сорбцией. При низких концентрациях (< 30 мг/л) для извлечения галлия более эффективными могут оказаться сорбционные процессы из-за значительных потерь экстрагента. Для этих целей могут использоваться ионообменные материалы различных типов. Сорбцию галлия из солянокислых растворов, получаемых при кислотном растворении анодных сплавов, проводят на высокоосновном анионите АВ-16 или на низкоосновном АН-31. Сорбцию осуществляют из растворов с концентрацией соляной кислоты 3,7 моль/л. Поскольку Fe(III) сорбируется вместе с галлием, его предварительно восстанавливают. После сорбции анионит промывают НС1 5 моль/л и десорбируют галлий соляной кислотой той же концентрации. Достигается почти полное отделение галлия от алюминия, но сорбционная емкость анионитов по галлию мала (~2 мг/г). Заслуживает внимания сорбция галлия на неорганических ионообменниках, регенерация которых часто не требуется. В качестве таких сорбентов могут использоваться высокодисперсные порошки неорганических соединений, не разлагающихся в растворах, из которых проводится сорбция. Одним из таких материалов является активный диоксид марганца, который сорбирует галлий из растворов с рН ~2,0.
Дата добавления: 2015-06-22; просмотров: 2144;
