Совместное решение материального и теплового
балансов для стационарного адиабатического реактора РИС–Н
Математическая модель адиабатического реактора РИС-Н
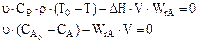 . (13.17)
. (13.17)
Система уравнений материального и теплового балансов представляет собой математическую модель реактора.
Определим значения степени превращения XА и температуры Т, достигаемые в реакторе. Естественно, что частные значения будут зависеть от конкретного вида кинетического уравнения. Скорость химической реакции зависит от концентрации CA и температуры T.
Рассмотрим самые простые варианты:
– необратимую реакцию первого порядка А 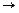 R;
R;
– обратимую реакцию первого порядка А 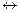 R.
R.
Предварительно преобразуем математическую модель реактора.
Ранее (см. раздел 2) получено:
 . (13.18)
. (13.18)
Уберем скорость химической реакции из уравнения теплового баланса (13.17). Представим произведение скорости химической реакции на объем, как
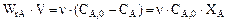 . (13.19)
. (13.19)
Тогда уравнение теплового баланса будет:
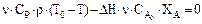 . (13.20)
. (13.20)
 Математическую модель реактора можно представить следующим образом:
Математическую модель реактора можно представить следующим образом:
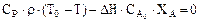 ; (13.21)
; (13.21)
 .
.
Для необратимой реакции первого порядка скорость химической реакции
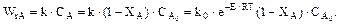 .(13.22)
.(13.22)
Подставив значение скорости химической реакции в математическую модель реактора (13.21), получим систему уравнений:


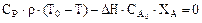 . (13.23)
. (13.23)
Аналитическое решение системы уравнений (13.23) затруднено, т.к. температура Т входит в уравнения в виде линейного члена и в составе комплекса. Для решения используем численные методы, т.к. уравнения являются трансцендентными.
Решим систему графическим методом.
Уравнение теплового баланса (13.23) преобразуем и получим:
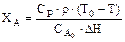 . (13.24)
. (13.24)
В координатах XA-Т это уравнение прямой линии, где отрезок, отсекаемый на оси абсцисс – начальная температура Т0. Наклон линии будет определять значение изменения энтальпии 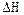 . Крутизну угла наклона можно изменить, меняя начальную концентрацию
. Крутизну угла наклона можно изменить, меняя начальную концентрацию 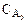 (рисунок 13.1).
(рисунок 13.1).
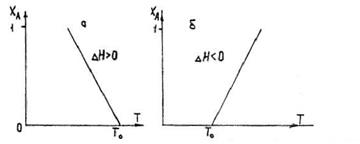
Рисунок 13.1 – Уравнение теплового баланса
реактора идеального смешения для эндотермических (а)
и экзотермических реакций (б)
Преобразуем зависимость:
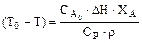 . (13.25)
. (13.25)
Принимаем, что степень превращения XA = 1, следовательно,
 . (13.26)
. (13.26)
Величина ΔТадиаб. показывает максимальное изменение температуры реакционной смеси, возможное в адиабатических условиях
 . (13.27)
. (13.27)
Для необратимой простой реакции
 . (13.28)
. (13.28)
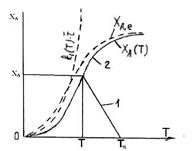
Решение системы уравнений материального и теплового балансов имеет различный вид для экзо- и эндотермических реакций (рисунки 13.2, 13.3).

Для эндотермической реакции возможно только одно решение, в то время как для экзотермической реакции, в зависимости от начальных температур Т01,Т02,Т03, возможно от одного до трех решений.
Если обратимая простая реакция, то
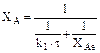 . (13.29)
. (13.29)
Для обратимой реакции степень превращения ХА фактически будет находиться ниже равновесной кривой, следовательно, для эндотермической реакции одно решение, а для экзотермической в зависимости от начальной температуры Т0, будет от одного до трех решений (рисунки 13.4, 13.5).

Дата добавления: 2015-06-17; просмотров: 1536;
