Тепловая устойчивость химических реакторов
При анализе совместного решения уравнений материального и теплового балансов адиабатического реактора идеального смешения для экзотермических реакций было отмечено, что возможны случаи, когда система имеет не одно, а несколько решений. Например, при пересечении прямой 2 и кривой 4 на рис. 8.4 (необратимая экзотермическая реакция первого порядка) система уравнений материального и теплового балансов имеет три решения, соответствующие точкам В, С и D. Решаемая графически система уравнений была составлена в предположении о стационарном режиме работы реактора, т. е. о неизменности во времени параметров процесса (в частности, температуры и степени превращения). Таким образом, наличие нескольких решений означает возможность множественности стационарных состояний.
На практике, конечно, из трех возможных решений будет реализовано одно. Желательно, чтобы работа реактора характеризовалась высокой степенью превращения исходного реагента, т. е. соответствовала точке D. Возможно ли это? Как при наличии нескольких стационарных состояний практически обеспечить наиболее выгодное состояние? Ответить на эти вопросы помогает анализ устойчивости стационарных состояний.
Устойчивость системы в стационарном состоянии определяется ее реакцией на возмущающее воздействие.
Стационарное состояние системы называется устойчивым, если небольшие кратковременные возмущающие воздействия не могут вывести систему за пределы небольшой области, окружающей исследуемый стационарный режим.
Если систему, находящуюся в устойчивом состоянии, отклонить от него, а затем предоставить ее самой себе, она самопроизвольно вернется в начальное состояние. Отклонение системы, находящейся в неустойчивом состоянии, вызовет после снятия возмущения ее самопроизвольный переход в другое, устойчивое состояние.
Для анализа устойчивости трех стационарных состояний В, С и D адиабатического реактора идеального смешения (см. рис. 6.4) используем сначала физические представления о природе процесса в реакторе. С этой целью преобразуем уравнения (6.15) и (6.17), умножив их на тепловой эффект реакции ∆Н.
Уравнение теплового баланса (6.15) примет вид
 (6.24)
(6.24)
Произведение теплоемкости на плотность реакционной смеси и ее температуру, отнесенное к начальной концентрации, представляет собой физическую теплоту реакционной смеси, приходящуюся на 1 моль (кмоль) исходного вещества, вошедшего в реактор. Для экзотермической реакции Т0 < Т,а получаемая в уравнении (6.24) величина g_ показывает, насколько больше физической теплоты будет вынесено из реактора покидающей его реакционной смесью, чем было внесено в реактор входным потоком. Так как g_ отнесено к 1 моль (кмоль) реагента А, эту величину можно назвать удельным отводом теплоты из реактора.
Уравнение (6.17) показывает, каков прирост степени превращения реагента при протекании химического процесса в реакторе. Если эту величину умножить на тепловой эффект экзотермической реакции ∆Н (кДж/кмоль) исходного реагента А, вступившего в реакцию, получают удельное выделение теплоты g+ в реакторе, приходящееся на 1 кмоль реагента А, вошедшего в реактор.
Так как величина ∆Н принята постоянной, то умножение на нее уравнений (6.15) и (6.17) изменит лишь масштаб на графике, используемом для численного решения системы уравнений материального и теплового балансов. Точки пересечения линий на рис. 6.5, а приобретают теперь новый физический смысл: они отвечают условиям равенства удельного теплоотвода и удельного тепловыделения, обеспечивающего стационарное состояние. При нарушении этого равенства, вызванном, например, кратковременным возмущением во входном потоке, будут преобладать либо g+,либо g_ и, следовательно, будет происходить самопроизвольное повышение или понижение температуры в аппарате.
Рассмотрим более подробно разные стационарные состояния при наличии решений системы уравнений материального и теплового балансов.
На рис. 6.7 в координатах g – T показана верхняя точка пересечения D,перенесенная с рис. 6.4. Пусть вследствие некоторого возмущения состояние теплового равновесия нарушится; например, в системе установится более высокая температура ТD+. В этом положении удельный теплоотвод g_ превышает удельный теплоотвод g+ и после снятия возмущения произойдет самопроизвольное снижение температуры до TD, т. е. система вернется в прежнее состояние равновесия. Если при нарушении равновесия температура в реакторе понизится до TD,то после снятия возмущения произойдет самопроизвольный разогрев до температуры TD вследствие того, что g+ > g_. Таким образом, точка D соответствует устойчивому стационарному состоянию адиабатического реактора идеального смешения.
Анализ состояния теплового равновесия в точке В (рис. 67, б)также позволяет сделать вывод, что это решение системы уравнений отвечает устойчивому стационарному состоянию.
Иным будет положение теплового равновесия средней точки пересечения С (рис. 6.7, в). Отклонение от состояния равновесия вправо по оси температур приведет к дальнейшему самопроизвольному разогреву, влево – к самопроизвольному понижению температуры. Следовательно, равновесие системы в точке С является неустойчивым.
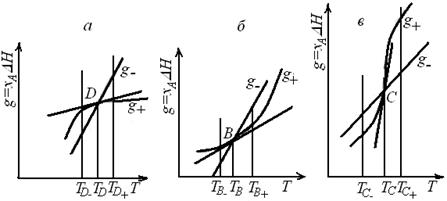
Рис. 6.7. Устойчивые (а, б)и неустойчивые (в)стационарные состояния
адиабатического реактора идеального смешения при проведении
экзотермической реакции
Следует отметить, что для устойчивых стационарных состояний производная dg+/dT (тангенс угла наклона касательной к кривой g+(Т)в точках пересечения) меньше, чем тангенс угла наклона линии g–(Т):

а для неустойчивых состояний

Эти неравенства могут быть использованы при анализе устойчивости работы реактора.
Проверка системы на устойчивость стационарного состояния связана с введением нестационарности (кратковременным нарушением состояния теплового равновесия, следовательно, непостоянством параметров во времени). Уравнение материального и теплового балансов проточного нестационарного реактора идеального смешения можно представить в таком виде:
 (6.25)
(6.25)
Такие системы дифференциальных уравнений поддаются графическому анализу, при котором зависимые переменные сА и Т считаются координатами так называемой фазовой плоскости. Используя уравнения типа (6.25), можно для фиксированных значений различных параметров определить каждую точку состояния системы на плоскости (сА, T).
Поскольку система сменяет во времени ряд состояний от начального до конечного, изображение их на плоскости (сА, Т) дает траекторию. Эти траектории (фазовые траектории) напоминают по своему виду траектории движения шара по различным плоскостям (см. рис. 6.8–6.10). Например, на рис. 6.8 точки А и С соответствуют устойчивому стационарному состоянию (сходимость в узел и спиралевидная сходимость в фокус), точка В – неустойчивому стационарному состоянию (расходящиеся траектории движения шара по поверхности седла).
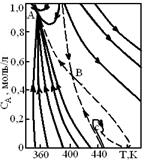
Рис. 6.8. Фазовая плоскость
с множественными стационарными состояниями
для проточного реактора с перемешиванием
Следует отметить, что стационарное состояние реактора может быть очень чувствительным к небольшим возмущениям входных параметров. Проанализируем, например, рис. 6.4 (случай тройного пересечения при совместном решении уравнений материального и теплового балансов для проводимой в реакторе экзотермической реакции). Небольшое изменение температуры реакционного потока на входе (смещение вправо прямой 1 или 2) может вызвать скачкообразное увеличение температуры в реакторе. Такую высокую чувствительность режима процесса к незначительным изменениям его параметров называют параметрической чувствительностью.
При выборе условий проведения экзотермической реакции обычно стремятся обеспечить единственное устойчивое стационарное состояние с высокой степенью превращения. Для этого можно увеличить или уменьшить температуру Т0(что вызовет сдвиг вправо прямой, отвечающей уравнению теплового баланса), или среднее время пребывания в реакторе 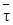 (при этом сдвигается влево кривая, отвечающая уравнению материального баланса). Такие решения иногда невыгодны экономически. В данных случаях для того, чтобы реактор самопроизвольно достигал верхней точки D (см. рис. 6.4), в момент пуска в ректоре нужно иметь температуру, отвечающую точке неустойчивого состояния С или чуть выше.
(при этом сдвигается влево кривая, отвечающая уравнению материального баланса). Такие решения иногда невыгодны экономически. В данных случаях для того, чтобы реактор самопроизвольно достигал верхней точки D (см. рис. 6.4), в момент пуска в ректоре нужно иметь температуру, отвечающую точке неустойчивого состояния С или чуть выше.
Дата добавления: 2015-06-17; просмотров: 3541;
