ПИГМЕНТЫ ФОТОСИНТЕЗА
План лекции:
1. Пигменты фотосинтеза. Хлорофиллы
2. Химические свойства хлорофилла
3. Физические свойства хлорофилла
4. Биосинтез хлорофилла
5. Условия образования хлорофилла
6. Каротиноиды
7. Фикобилины
1. Пигменты фотосинтеза. Хлорофиллы
Для того чтобы свет мог оказывать влияние на растительный организм и, в частности, быть использованным в процессе фотосинтеза, необходимо его поглощение фоторецепторами-пигментами. Пигменты— это окрашенные вещества. Пигменты поглощают свет определенной длины волны. Непоглощенные участки солнечного спектра отражаются, что и обусловливает окраску пигментов. Так, зеленый пигмент хлорофилл поглощает красные и синие лучи, тогда как зеленые лучи в основном отражаются. Видимая часть солнечного спектра включает длины волн от 400 до 700 нм. Вещества, поглощающие весь видимый участок спектра, кажутся черными.
Состав пигментов зависит от систематического положения группы организмов. У фотосинтезирующих бактерий и водорослей пигментный состав очень разнообразен (хлорофиллы, бактериохлорофиллы, бактериородопсин, каротиноиды, фикобилины). Их набор и соотношение специфичны для различных групп и во многом зависят от среды обитания организмов. Пигменты фотосинтеза у высших растений значительно менее разнообразны. Пигменты, сконцентрированные в пластидах, можно разделить на три группы: хлорофиллы, каротиноиды, фикобилины.
Важнейшую роль в процессе фотосинтеза играют зеленые пигменты —хлорофиллы. Французские ученые П.Ж. Пелетье и Ж. Кавенту (1818) выделили из листьев зеленое вещество и назвали eгo хлорофиллом (от греч. «хлорос» — зеленый и «филлон» — лист). В настоящее время известно около десяти хлорофиллов. Они отличаются по химическому строению, окраске, распространению среди живых организмов. У всех высших растений содержатся хлорофиллы а и b. Хлорофилл с обнаружен в диатомовых водорослях, хлорофилл d — в красных водорослях. Кроме того, известны четыре бактериохлорофилла (a, b, с и d), содержащиеся в клетках фотосинтезирующих бактерий. В клетках зеленых бактерий имеются бактериохлорофиллы с и d, в клетках пурпурных бактерий — бактериохлорофиллы а и b. Основными пигментами, без которых фотосинтез не идет, являются хлорофиллы для зёленых растений и бактериохлорофиллы для бактерий.
Впервые точное представление о пигментах зелёного листа высших растений было получено благодаря работам крупнейшего русского ботаника М.С. Цвета (1872—1919). Он разработал хроматографический метод разделения веществ и выделил пигменты листа в чистом виде. Хроматографический метод разделения веществ основан на их различной способности к адсорбции. Метод этот получил широкоё применение. М.С. Цвет пропускал вытяжку из листа через стеклянную трубку заполненную порошком — мелом или сахарозой (хроматографическую колонку). Отдельные компоненты смеси пигментов различались по степени адсорбируемости и передвигались с разной скоростью, в результате чего они концентрировались в разных зонах колонки. Разделяя колонку на отдельные части (зоны) и используя соответствующую систему растворителей, можно было выделить каждый пигмент. Оказалось, что листья высших растений содержат хлорофилл а и хлорофилл b, а также каротиноиды (каротин, ксантофилл и др.). Хлорофиллы, так же как и каротиноиды, нерастворимы в воде, но хорошо растворимы в органических растворителях. Хлорофиллы а и b различаются по цвету: хлорофилл а имеет сине-зеленый оттенок, а хлорофилл b — желто-зеленый. Содержание хлорофилла а в листе примерно в три раза больше, чем хлорофилла b.
2. Химические свойства хлорофилла
По химическому строению хлорофиллы — сложные эфиры дикарбоновой органической кислоты — хлорофиллина и двух остатков спиртов фитола и метилового. Эмпирическая формула — C55H72O5N4Mg. Хлорофиллин представляет собой азотсодержащее металлорганическое соединение, относящееся к магнийпорфиринам.
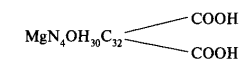
В хлорофилле водород карбоксильных групп замещен остатками двух спиртов — метилового СН3ОН и фитола С20Н39ОН поэтому хлорофилл является сложным эфиром. На рисунке 1, А дана структурная формула хлорофилла а.
Хлорофилл b отличается тем, что содержит на два атома водорода меньше и на один_ атом кислорода больше (вместо группы СН3 группа СНО (рис. 1, Б). В связи с этим молекулярная масса хлорофилла а — 893 и хлорофилла b — 907. В 1960 г. Р.Б. Вудворд осуществил полный синтез хлорофилла.
В центре молекулы хлорофилла расположен атом магния, который соединен с четырьмя атомами азота пиррольных группировок. В пиррольных группировках хлорофилла имеется система чередующихся двойных и простых связей. Это и есть хромофорная группа хлорофилла, обусловливающая поглощение определенных лучей солнечного спектра и его окраску. Диаметр порфиринового ядра составляет 10 нм, а длина фитольного остатка — 2 нм.
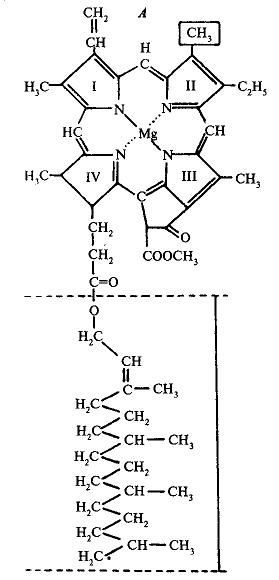
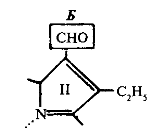
Рисунок 1 – Хлрофиллы а и b
Расстояние между атомами азота пиррольных группировок в ядре хлорофилла составляет 0,25 нм. Интересно, что диаметр атома магния равен 0,24нм. Таким образом, магний почти полностью заполняет пространство между атомами азота пиррольных группировок. Это придает ядру молекулы хлорофилла дополнительную прочность. Еще К.А. Тимирязев обратил внимание на близость химического строения двух важнейших пигментов: зеленого — хлорофилла листьев и красного — гемина крови. Действительно, если хлорофилл относится к магний порфиринам, то гемин — к железопорфиринам. Сходство это не случайно и служит еще одним доказательством единства всего органического мира.
Одной из специфических черт строения хлорофилла является наличие в его молекуле помимо четырех гетероциклов еще одной циклической группировки из пяти углеродных атомов — циклопентанона. В циклопентановом кольце содержится кетогруппа, обладающая большой реакционной способностью. Есть данные, что в результате процесса энолизации по месту этой кетогруппы к молекуле хлорофилла присоединяется вода.
Молекула хлорофилла полярна, ее порфириновое ядро обладает гидрофильными свойствами, а фитольный конец — гидрофобными. Это свойство молекулы хлорофилла обусловливает определенное расположение ее в мембранах хлоропластов. Порфириновая часть молекулы связана с белком, а фитольная цепь погружена в липидный слой.
Извлеченный из листа хлорофилл легко реагирует как с кислотами, так и со щелочами. При взаимодействии со щелочами происходит омыление хлорофилла в результате чего образуются, два спирта и щелочная соль кислоты хлорофиллина. В интактном живом листе от хлорофилла может отщепляться фитол под воздействием фермента хлорофиллазы. При взаимодействии со слабой кислотой извлеченный хлорофилл теряет зеленый цвет, образуется соединение феофитин, у которого атом магния в центре молекулы замещен на два атома водорода.
Хлорофилл в живой интактной клетке обладает способностью к обратимому фотоокислению и фотовосстановлению. Способность к окислительно-восстановительным реакциям связана с наличием в молекуле хлорофилла сопряженных двойных связей с подвижными
π-электронами и атомов азота с неподеленными электронами. Азот пиррольных ядер может окисляться (отдавать электрон) или восстанавливаться (присоединять электрон).
Исследования показали, что свойства хлорофилла, находящегося в листе и извлеченного из листа, различны, так как в листе он находится в комплексном соединении с белком. Это доказывается следующими данными:
Спектр поглощения хлорофилла, находящегося в листе, иной по сравнению с извлеченным хлорофиллом.
Хлорофилл невозможно извлечь абсолютным спиртом из сухих листьев. Экстракция протекает успешно, только если листья увлажнить или к спирту добавить воды, которая разрушает связь между хлорофиллом и белком.
Выделенный из листа хлорофилл легко подвергается разрушению под влиянием самых разнообразных воздействий (повышенная кислотность, кислород и даже свет).
Между тем в листе хлорофилл достаточно устойчив ко всем перечисленным факторам. Следует отметить, что хотя крупный русский ученый В. Н. Любименко и предлагал этот комплекс назвать хлороглобином, по аналогии с гемоглобином, связь между хлорофиллом и белком иного характера, чем между гемином и белком. Для гемоглобина характерно постоянное соотношение — на 1 молекулу белка приходится 4 молекулы гемина. Между тем соотношение между хлорофиллом и белком различно и претерпевает изменения в зависимости от типа растений, фазы их развития, условий среды (от 3 до 10 молекул хлорофилла на 1 молекулу белка). Связь между молекулами белка и хлорофиллом осуществляется путем нестойких комплексов, образующихся при взаимодействии кислотных групп белковых молекул и азота пиррольных колец. Чем выше содержание дикарбоновых аминокислот в белке, тем лучше идет их комплексирование с хлорофиллом (Т.Н.Годнее). Белки, связанные с хлорофиллом, характеризуются низкой изоэлектрической точкой (3,7—4,9). Молекулярная масса этих белков порядка 68 кДа. Вместе с тем хлорофилл может взаимодействовать и с липидами мембран.
Важным свойством молекул хлорофилла является их способность к взаимодействию друг с другом. Переход из мономерной в агрегированную форму возник в результате взаимодействия двух и более молекул при их близком расположении друг к другу. В процессе образования хлорофилла его состояние в живой клетке закономерно меняется. При этом и происходит его агрегация (А.А. Красновский). В настоящее время показано, что хлорофилл в мембранах пластид находится в виде пигмент-липопротеидных комплексов с различной степенью агрегации.
3. Физические свойства хлорофилла
Как уже отмечалось, хлорофилл способен к избирательному поглощению света. Спектр поглощения данного соединения определяется его способностью поглощать свет определенной длины волны (определенного цвета). Для того чтобы получить спектр поглощения К.А. Тимирязев пропускал луч света через раствор хлорофилла. Часть лучей поглощалась хлорофиллом, и при последующем пропускании через призму в спектре обнаруживались черные полосы. Было показано, что хлорофилл в той же концентрации, как в листе, имеет две основные линии поглощения в красных и сине-фиолетовых лучах. При этом хлорофилл а в растворе имеет максимум поглощения 429 и 660 нм, тогда как хлорофилл b — 453 и 642 нм. Однако необходимо учитывать, что в листе спектры поглощения хлорофилла меняются в зависимости от его состояния, степени агрегации, адсорбции на определенных белках. В настоящее время показано, что есть формы хлорофилла, поглощающие свет с длиной волны 700, 710 и даже 720 нм. Эти формы хлорофилла, поглощающие свет с большой длиной волны, имеют особенно важное значение в процессе фотосинтеза.
Хлорофилл обладает способностью к флуоресценции. Флуоресценция представляет собой свечение тел, возбуждаемое освещением и продолжающееся очень короткий промежуток времени (108—109 с). Свет, испускаемый при флюоресценции, имеет всегда большую длину волны по сравнению с поглощенным. Это Связано с тем, что часть поглощенной энергии выделяется в виде тепла. Хлорофилл обладает красной флуоресценцией.
4. Биосинтез хлорофилла
Синтез хлорофилла происходит в две фазы: темновую — до протохлорофиллида и световую — образование из протохлорофиллида хлорофиллида (рис. 2).Синтез начинается с превращения глутаминовой кислоты в δ-аминолевулиновую кислоту. 2 молекулы δ-аминолевулиновой кислоты конденсируются в порфобилиноген. Далее 4 молекулы порфобилиногена превращаются в протопорфирин IX. После этого в кольцо встраивается магний и получается протохлорофиллид. На свету и в присутствии НАДН образуется хлорофиллид: протохлорофиллид + 2Н+ + hv →хлорофиллид
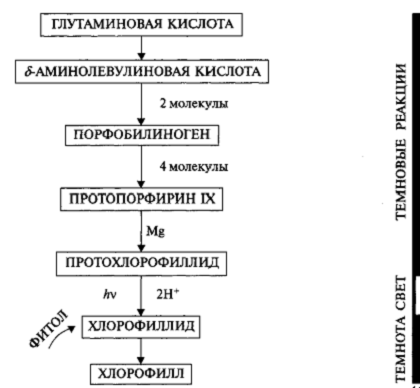
Рисунок 2 - Схема биосинтеза хлорофилла
I
Протоны присоединяются к четвертому пиррольному кольцу в молекуле пигмента. На последнем этапе происходит взаимодействие хлорофиллида со спиртом фитолом: хлорофиллид + фитол → хлорофилл.
Поскольку синтез хлорофилла — процесс многоэтапный, в нем участвуют различные ферменты, составляющие, по-видимому, полиферментный комплекс. Интересно заметить, что образование многих из этих белков-ферментов ускоряется на свету. Свет косвенно ускоряет образование предшественников хлорофилла. Одним из наиболее важных ферментов является фермент, катализирующий синтез δ-аминолевулиновой кислоты (аминолевулинатсинтаза). Важно отметить, что активность этого фермента также повышается на свету.
Содержание хлорофилла в листе колеблется незначительно. Это связано с тем, что идет непрерывный процесс разрушения старых молекул и образование новых молекул хлорофилла. Причем эти два процесса уравновешивают друг друга. При этом предполагается, что вновь образовавшиеся молекулы хлорофилла не смешиваются со старыми и имеют несколько иные свойства.
5. Условия образования хлорофилла
Исследования влияния света на накопление хлорофилла в этиолированных проростках позволили установить, что первым в процессе зеленения появляется хлорофилл а. Спектрографический анализ показывает, что процесс образования хлорофилла идет очень быстро. Так, уже через
1 мин после начала освещения выделенный из этиолированных проростков пигмент имеет спектр поглощения, совпадающий со спектром поглощения хлорофилла а. По мнению А.А. Шлыка, хлорофилл b образуется из хлорофилла а.
При исследовании влияния качества света на образование хлорофилла в большинстве случаев проявилась положительная роль красного света. Большое значение имеет интенсивность освещения. Существование нижнего предела освещенности для образования хлорофилла было показано в опытах В.Н. Любименко для проростков ячменя и овса. Оказалось, что освещение электрической лампой мощностью 10 Вт на расстоянии 400 см было пределом, ниже которого образование хлорофилла прекращалось. Существует и верхний предел освещенности, выше которого образование хлорофилла тормозится.
Проростки, выросшие в отсутствие света, называют этиолированными. Такие проростки характеризуются измененной формой (вытянутые стебли, неразвившиеся листья) и слабой желтой окраской (хлорофилла в них нет). Как было сказано выше, образование хлорофилла на заключительных этапах требует света.
Еще со времен Ю. Сакса (1864) известно, что в некоторых случаях хлорофилл образуется и в отсутствие света. Способность образовывать хлорофилл в темноте характерна для организмов, стоящих на нижней ступени эволюционного процесса. Так, при благоприятных условиях питания некоторые бактерии могут синтезировать в темноте бактериохлорофилл. Цианобактерии при достаточном снабжении органическим веществом растут и образуют пигменты в темноте. Способность к образованию хлорофилла в темноте обнаружена и у таких высокоорганизованных водорослей, как харовые. Лиственные и печеночные мхи сохраняют способность образовывать хлорофилл в темноте. Почти у всех видов хвойных при прорастании семян в темноте семядоли зеленеют. Более развита эта способность у теневыносливых пород хвойных деревьев. По мере роста проростков в темноте образовавшийся хлорофилл разрушается, и на 35—40-й день проростки в отсутствие света погибают. Интересно заметить, что проростки хвойных, выращенные из изолированных зародышей в темноте, хлорофилла не образуют. Однако достаточно присутствия небольшого кусочка нераздробленного эндосперма, чтобы проростки начинали зеленеть. Зеленение происходит даже в том случае, если зародыш соприкасается с эндоспермом другого вида хвойных деревьев. При этом наблюдается прямая корреляция между величиной окислительно-восстановительного потенциала эндосперма и способностью проростков зеленеть в темноте.
Можно сделать заключение, что в эволюционном плане хлорофилл первоначально образовался как побочный продукт темнового обмена. Однако в дальнейшем на свету растения, обладающие хлорофиллом, получили большее преимущество благодаря возможности использовать энергию солнечного света, и эта особенность была закреплена естественным отбором.
Образование хлорофилла зависит от температуры. Оптимальная температура для накопления хлорофилла 26—30°С. От температуры зависит лишь образование предшественников хлорофилла (темновая фаза). При наличии уже образовавшихся предшественников хлорофилла процесс зеленения (световая фаза) идет с одинаковой скоростью независимо от температуры.
На скорость образования хлорофилла оказывает влияние содержание воды. Сильное обезвоживание проростков приводит к полному прекращению образования хлорофилла. Особенно чувствительно к обезвоживанию образование протохлорофиллида.
Еще В.И. Палладии обратил внимание на необходимость углеводов для протекания процесса зеленения. Именно с этим связано то, что зеленение этиолированных проростков на свету зависит от их возраста. После 7—9-дневного возраста способность к образованию хлорофилла у таких проростков резко падает. При опрыскивании сахарозой проростки снова начинают интенсивно зеленеть.
Важнейшее значение для образования хлорофилла имеют условия минерального питания. Прежде всего необходимо достаточное количество железа. При недостатке железа листья даже взрослых растений теряют окраску. Это явление названо хлорозом. Железо — важный катализатор образования хлорофилла. Оно необходимо на этапе синтеза δ-аминолевулиновой кислоты, а также синтеза про-топорфирина. Большое значение для обеспечения синтеза хлорофилла имеет нормальное снабжение растений азотом и магнием, так как оба эти элемента входят в состав хлорофилла. При недостатке меди хлорофилл легко разрушается. Это, по-видимому, связано с тем, что медь способствует образованию устойчивых комплексов между хлорофиллом и соответствующими белками.
Исследование процесса накопления хлорофилла у растений в течение вегетационного периода показало, что максимальное содержание хлорофилла приурочено к началу цветения. Есть даже мнение, что повышение образования хлорофилла может быть использовано как индикатор, указывающий на готовность растений к цветению. Синтез хлорофилла зависит от деятельности корневой системы. Так, при прививках содержание хлорофилла в листьях привоя зависит от свойств корневой системы подвоя. Возможно, что влияние корневой системы связано с тем, что там образуются гормоны (цитокинины). У двудомных растений большим содержанием хлорофилла характеризуются листья женских особей.
6. Каротиноиды
Наряду с зелеными пигментами в хлоропластах и хроматофорах содержатся пигменты, относящиеся к группе каротиноидов. Каротиноиды — это желтые и оранжевые пигменты алифатического строения, производные изопрена. Каротиноиды содержатся во всех высших растениях и у многих микроорганизмов. Это самые распространенные пигменты с разнообразными функциями. Каротиноиды, содержащие кислород, получили название ксантофиллы. Основными представителями каротиноидов у высших растений являются два пигмента —
β-каротин (оранжевый) С40Н56 и ксантофилл (желтый) C40H56O2. Каротин состоит из 8 изопреновых остатков (рис. 3).
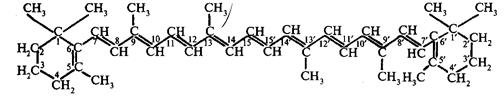
Рисунок 3 – Структура β-каротина
При разрыве углеродной цепочки пополам и образовании на конце спиртовой группы каротин превращается в 2 молекулы витамина А. Обращает на себя внимание сходство в структуре фитола — спирта, входящего в состав хлорофилла, и углеродной цепочки, соединяющей иононовые кольца каротина. Предполагается, что фитол возникает как продукт гидрирования этой части молекулы каротиноидов. Поглощение света каротиноидами, их окраска, а также способность к окислительно-восстановительным реакциям обусловлены наличием конъюгированных двойных связей, β-каротин имеет два максимума поглощения, соответствующие длинам волн 482 и 452 нм. В отличие от хлорофиллов каротиноиды не поглощают красные лучи, а также не обладают способностью к флуоресценции. Подобно хлорофиллу каротиноиды в хлоропластах и хроматофорах находятся в виде нерастворимых в воде комплексов с белками.
Уже тот факт, что каротиноиды всегда присутствуют в хлоропластах, позволяет считать, что они принимают участие впроцессе фотосинтеза. Однако не отмечено ни одного случая, когда в отсутствие хлорофилла этот процесс осуществляется. В настоящее время установлено, что каротиноиды, поглощая определенные участки солнечного спектра, передают энергию этих лучей на молекулы хлорофилла. Тем самым они способствуют использованию лучей, которые хлорофиллом не поглощаются.
Физиологическая роль каротиноидов не ограничивается их участием в передаче энергии на молекулы хлорофилла. По данным русского исследователя
Д.И. Сапожникова, на свету происходит взаимопревращение ксантофиллов (виолаксантин превращается в зеаксантин), что сопровождается выделением кислорода. Спектр действия этой реакции совпадает со спектром поглощения хлорофилла, что позволило высказать предположение об ее участии в процессе разложения воды и выделения кислорода при фотосинтезе.
Имеются данные, что каротиноиды выполняют защитную функцию, предохраняя различные органические вещества, в первую очередь молекулы хлорофилла, от разрушения на свету в процессе фотоокисления. Опыты, проведенные на мутантах кукурузы и подсолнечника, показали, что они содержат протохлорофиллид (темновой предшественник хлорофилла), который на свету переходит в хлорофилл а, но разрушается. Последнее связано с отсутствием способности исследованных мутантов к образованию каротиноидов.
Ряд исследователей указывают, что каротиноиды играют определенную роль в половом процессе у растений. Известно, что в период цветения высших растений содержание каротиноидов в листьях уменьшается. Одновременно оно заметно растет в пыльниках, а также в лепестках цветков. По мнению П. М. Жуковского, микроспорогенез тесно связан с метаболизмом каротиноидов. Незрелые пыльцевые зерна имеют белую окраску, а созревшая пыльца — желто-оранжевую. В половых клетках водорослей наблюдается дифференцированное распределение пигментов. Мужские гаметы имеют желтую окраску и содержат каротиноиды. Женские гаметы содержат хлорофилл. Высказывается мнение, что именно каротин обусловливает подвижность сперматозоидов. По данным В. Мевиуса, материнские клетки водоросли хламидомонады образуют половые клетки (гаметы) первоначально без жгутиков, в этот период они еще не могут передвигаться в воде. Жгутики образуются только после освещения гамет длинноволновыми лучами, которые улавливаются особым каротиноидом — кроцетином.
Образование каротиноидов.Синтез каротиноидов не требует света. При формировании листьев каротиноиды образуются и накапливаются в пластидах еще в тот период, когда зачаток листа защищен в почке от действия света. В начале освещения образование хлорофилла в этиолированных проростках сопровождается временным падением содержания каротиноидов. Однако затем содержание каротиноидов восстанавливается и даже повышается с увеличением интенсивности освещения. Установлено, что между содержанием белка и каротиноидов имеется прямая коррелятивная связь. Потеря белка и каротиноидов в срезанных листьях идет параллельно. Образование каротиноидов зависит от источника азотного питания. Более благоприятные результаты по накоплению каротиноидов получены при выращивании растений на нитратном фоне по сравнению с аммиачным. Недостаток серы резко уменьшает содержание каротиноидов. Большое значение имеет соотношение — Ca/Mg в питательной среде. Относительное увеличение содержания кальция приводит к усиленному накоплению каротиноидов по сравнению с хлорофиллом. Противоположное влияние оказывает увеличение содержания магния.
7. Фикобилины
Фикобилины— красные и синие пигменты, содержащиеся у цианобактерий и некоторых водорослей. Исследования показали, что красные водоросли и цианобактерий наряду с хлорофиллом а содержат фикобилины. В основе химического строения фикобилинов лежат четыре пиррольные группировки. В отличие от хлорофилла у фикобилинов пиррольные группы расположены в виде открытой цепочки (рис. 4). Фикобилины представлены пигментами: фикоцианином, фикоэритрином и аллофикоцианином. Фикоэритрин — это окисленный фикоцианин. Красные водоросли в основном содержат фикоэритрин, а цианобактерий — фикоцианин. Фикобилины образуют прочные соединения с белками (фикобилин-протеиды). Связь между фикобилинами и белками разрушается только кислотой. Предполагается, что карбоксильные группы пигмента связываются с аминогруппами белка. Необходимо отметить, что в отличие от хлорофиллов и каротиноидов, расположенных в мембранах, фикобилины концентрируются в особых гранулах (фикобилисомах), тесно связанных с мембранами тилакоидов.
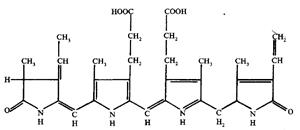
Рисунок 4 – Хромофорная группа фикоэритринов
Фикобилины поглощают лучи в зеленой и желтой частях солнечного спектра. Это та часть спектра, которая находится между двумя основными линиями поглощения хлорофилла. Фикоэритрин поглощает лучи с длиной волны 495— 565 нм, а фикоцианин — 550— 615 нм. Сравнение спектров поглощения фи-кобилинов со спектральным составом света, в котором проходит фотосинтез у цианобактерий и красных водорослей, показывает, что они очень близки. Это позволяет считать, что фикобилины поглощают энергию света и, подобно каротиноидам, передают ее на молекулу хлорофилла, после чего она используется процессе фотосинтеза.
Наличие фикобилинов у водорослей является примером приспособления организмов в процессе эволюции к использованию участков солнечного спектра, которые проникают сквозь толщу морской воды (хроматическая адаптация). Как известно, красные лучи, соответствующие основной линии поглощения хлорофилла, поглощаются, проходя через толщу воды. Наиболее глубоко проникают зеленые лучи, которые поглощаются не хлорофиллом, а фикобилинами.
ФОТОСИНТЕЗ (12 часов)
Дата добавления: 2015-06-10; просмотров: 28341;
