Опытные законы идеального газа
В молекулярно-кинетической теории пользуются моделью идеального газа, согласно которой считают, что:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
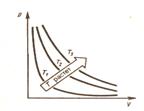 Закон Бойля-Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
Закон Бойля-Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
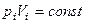 при Т=const, m=const
при Т=const, m=const
Кривая зависимости р от V при Т=const называется изотермой.
рис.15
Законы Гей-Люссака:1) Объем данной массы газа при постоянном давлении изменяется линейно с температурой:
V=V0(1+αt) при p=const, m=const
 Более удобный вид:
Более удобный вид: 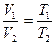 ,
,
Кривая зависимости V от Т называется изобарой.
рис.16
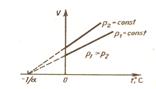
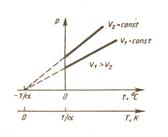
2) Давление данной массы газа при постоянном объеме линейно изменяется с температурой:
р=р0(1+αt) при V=const, m=const
 Более удобный вид:
Более удобный вид: 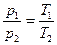 ,
,
где р0 и V0 – объем и давление при
0 0С, коэффициент α=1/273,15 К-1
Кривая зависимости р от Т называется изохорой.
рис.17
Закон Авогадро: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен 22,41.10-3м3/моль. NA=6,022.1023моль-1 – число молекул в одном моле вещества – постоянная Авогадро.
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов:
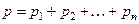 ,
,
где р1 , р2….. рn – парциальные давления, давления, которые оказывали бы отдельные газы смеси, если бы они занимали объем, равный объему смеси при той же температуре.
Русский ученый Д.И. Менделеев и французский Клапейрон получили уравнение состояния идеального газа, связывающее вместе три термодинамических параметра системы:
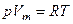
где Vm – молярный объем – объем одного моля газа, R – универсальная газовая постоянная, равная 8,31 Дж/(моль.К). Для произвольной массы газа уравнение записывается в виде:
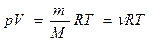
где М – молярная масса, 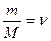 – количество вещества.
– количество вещества.
Существует еще одна форма записи этого уравнения:
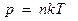
где n – концентрация молекул газа, 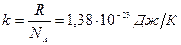 .
.
NA=6,022.1023моль-1 - число Авогадро
Дата добавления: 2015-05-30; просмотров: 1709;
