ФОТОСИНТЕЗ. Фотосинтез – это процесс трансформации поглощенной растением электромагнитной энергии солнечного света в химическую энергию органических соединений
Фотосинтез – это процесс трансформации поглощенной растением электромагнитной энергии солнечного света в химическую энергию органических соединений. Чтобы свет мог быть использованным в процессе фотосинтеза, необходимо его поглощение фоторецепторами – пигментами.
5.1. Пигменты
5.1.1. Хлорофиллы
У всех высших растений, водорослей и цианобактерий содержится хлорофилл a, хлорофилл b имеется у высших растений и зеленых водорослей. Хлорофилл с, лишенный фитола, содержится в бурых и диатомовых водорослях, хлорофилл d – в красных водорослях. Фотосинтезирующие зеленые бактерии имеют бактериохлорофиллы c и d, пурпурные бактерии - бактериохлорофиллы a и b.
У хлорофилла а четыре пиррольных кольца соединены между собой метиновыми мостиками (=СН-), образуя порфириновое кольцо. Кроме того, атомы азота пиррольных колец связаны с атомом магния. С порфириновым ядром соединено циклопентановое кольцо, образованное остатком кетопропионовой кислоты и содержащее активные карбонильную (С=О) и метилированную карбоксильную (О=С-О-СН3) группы. Структура, состоящая из порфиринового ядра и циклопентанового кольца, называется форбином. Боковая цепь, состоящая из пропионовой кислоты и непредельного спирта фитола, связана с атомом углерода IV пиррольного кольца (рис. 5.1). Хлорофилл, лишенный фитола, называется хлорофиллидом. Если атом магния замещен протоном, то такое соединение носит название феофитина. Активность хлорофиллов, также как и других пигментов, обусловлена наличием большого количества двойных связей с делокализованными электронами.
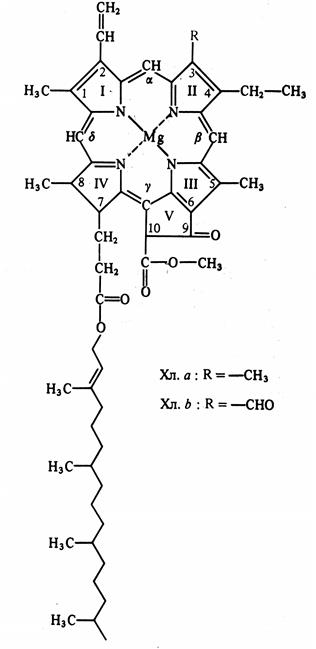
Рис. 5.1. Структурные формулы хлорофиллов a и b (по В. В. Полевому).
Хлорофиллы хорошо растворимы в органических растворителях (этиловом эфире, бензоле, хлороформе, ацетоне, этиловом спирте) и нерастворимы в воде. Хлорофиллы имеют максимумы поглощения света в красной и синей частях спектра. Растворы хлорофиллов обладают флуоресценцией и фосфоресценцией.
5.1.2. Каротиноиды
Каротиноиды – жирорастворимые пигменты, присутствующие в хлоропластах всех растений. Они входят в состав хромопластов в незеленых частях растений, например, корнеплодов моркови. К каротиноидам относят 3 группы соединений: 1) оранжевые или красные каротины, 2) желтые ксантофиллы, 3) каротиноидные кислоты. Каротины и ксантофиллы состоят из 8 остатков изопрена, которые образуют цепь конъюгированных двойных связей (рис. 5.2). Основные каротиноиды - b-каротин, лютеин, виолаксантин и неоксантин.
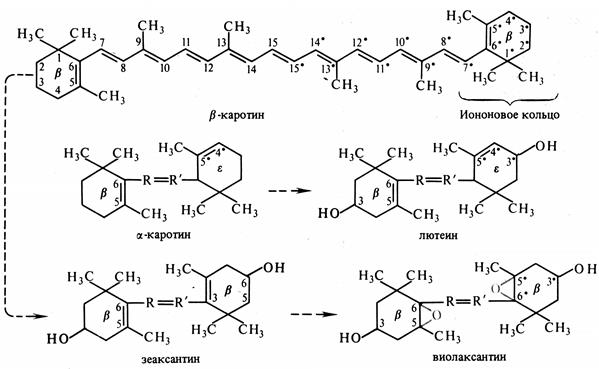
Рис. 5.2. Структурные формулы каротиноидов и последовательность их превращений (по В. В. Полевому).
Каротины и ксантофиллы растворимы в хлороформе, бензоле, сероуглероде, ацетоне. Каротины хорошо растворяются в эфирах, но плохо в спиртах, а ксантофиллы наоборот. Каротиноиды имеют максимумы поглощения в фиолетово-синей и синей частях спектра света. Они не способны к флуоресценции.
Главные функции каротиноидов: поглощение света в качестве дополнительных пигментов, защита молекул хлорофиллов от необратимого фотоокисления, тушение активных радикалов, участие в фототропизме, так как способствуют определению направления роста побега.
5.1.3. Фикобилины
Сине-зеленые и красные водоросли помимо хлорофилла а и каротиноидов содержат пигменты фикобилины. Их молекула состоит из 4 последовательных пиррольных колец (рис. 5.3). Фикобилины являются хромофорными группами глобулиновых белков фикобилипротеинов. Они делятся на 3 группы: 1) фикоэритрины – белки красного цвета, 2) фикоцианины – сине-голубые белки и 3) аллофикоцианины – синие белки. Все они обладают флуоресценцией и растворимы в воде.
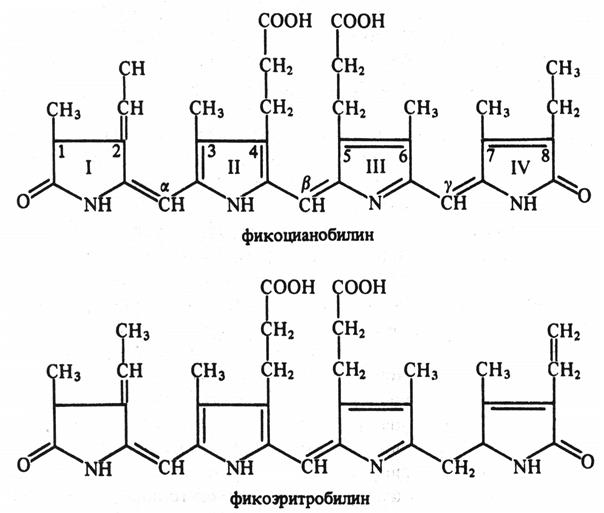
Рис. 5.3. Структурные формулы фикобилинов (по В. В. Полевому).
Фикобилины имеют максимумы поглощения в оранжевой, желтой и зеленой частях спектра света. Это позволяет водорослям полнее использовать свет, проникающий в воду. Вода обладает светопоглощающей способностью. На глубине около 30 м полностью исчезают красные лучи, около 180 м – желтые, 320 м – зеленые, а на глубину более 500 м не проникают синие и фиолетовые лучи. Фикобилины – это дополнительные пигменты, участвующие в светособирающем комплексе. Около 90 % энергии света, поглощенного фикобилинами, передается на хлорофилл а.
У растений имеется фикобилин фитохром. Он не участвует в фотосинтезе, но является фоторецептором красного и дальнего красного света и выполняет регуляторные функции в клетках растений.
5.2. Световая фаза фотосинтеза
Фотосинтез имеет две фазы – световую и темновую. В световой фазе молекулы пигментов поглощают фотоны, передают поглощенную энергию молекулам хлорофилла а, происходит трансформация энергии света в химическую энергию АТФ и восстановленного НАДФН, выделяется кислород в результате фоторазложения воды. Все эти процессы происходят на мембранах хлоропластов. При темновой фазе фотосинтеза в строме хлоропластов восстанавливается поглощенный СО2 с образованием углеводов и других органических соединений.
5.2.1. Поглощение света и возбуждение хлорофилла
Электрон представляет собой заряженную частицу, которая движется по орбите вокруг ядра атома. Электрон обладает вектором магнитного момента – спином, который отражает направление вращения электрона вокруг своей оси. В стабильном состоянии валентные электроны занимают самые низкие энергетические уровни и распределены по ним согласно принципу Паули: два электрона с антипараллельными спинами на каждой орбитали. Такое состояние молекулы называют основным синглетным состоянием S0. При поглощении молекулой пигмента фотона электрон переходит на более высокую орбиталь за счет энергии фотона. Если у возбужденного электрона сохраняется направление спина, то считают, что молекула находится в синглетном возбужденном состоянии S*. Если возбужденный электрон меняет спин, то такое возбужденное состояние называется триплетным Т*.
Поглощение молекулой хлорофилла кванта красного света приводит к синглетному возбужденному состоянию S*1. При поглощении кванта синего цвета с более высоким уровнем энергии электрон переходит на более высокую орбиталь S*2. Время жизни электрона на S*2 составляет не более 10-12 секунды. За такое короткое время энергия электронного возбуждения не может быть использована и электрон возвращается на S*1, потеряв немного энергии в виде тепла. Время жизни электрона в состоянии S*1 равно 10-9. Если молекула пигмента не участвует в фотохимической реакции, то электрон возвращается в стабильное состояние. При этом часть энергии теряется в виде тепла и излучается квант света с большей по сравнению с поглощенным фотоном длиной волны – явление флуоресценции.
Время жизни электрона в состоянии Т* равно 10-4-10-2 секунды. Из триплетного возбужденного состояния молекула может вернуться в стабильное состояние, излучив кроме тепла еще более длинноволновый, чем при флуоресценции, квант света. Это слабое свечение называют фосфоресценцией. Если молекула в возбужденном состоянии участвует в фотохимических реакциях с передачей электрона акцептору, то флуоресценции и фосфоресценции не происходит.
Для более полного использования падающего на листья света энергия фотонов улавливается 200-400 молекулами пигментов светособирающего (антенного) комплекса и передается к одной молекуле хлорофилла а, являющейся реакционным центром, которая и участвует в фотохимических реакциях. Передача энергии молекулами пигментов происходит по принципу индуктивного резонанса. Молекула пигмента, поглотившая фотон, создает переменное электрическое поле, которое усиливает колебания электрона в соседней молекуле. Это происходит из-за перекрытия частот колебаний и очень маленького расстояния между молекулами пигментов. Тем более, что при освещении листьев тилакоиды и граны сдвигаются и уплотняются, поэтому хлоропласты уменьшаются в объеме. Передача энергии молекулами пигментов идет с большой эффективностью. Так, от хлорофилла b к хлорофиллу а передается примерно 90 %, а от каротиноидов к хлорофиллу а – 40 % поглощенной энергии.
Совокупность молекул светособирающего комплекса и реакционного центра составляет фотосистему. Предположение о существовании в хлоропластах двух фотосистем высказал Р. Эмерсон в 1957 г, изучая влияние света на квантовый выход фотосинтеза у водоросли хлореллы. Квантовый выход фотосинтеза – это количество выделившегося кислорода или связанного углекислого газа на 1 квант поглощенной энергии. Он установил, что при одновременном освещении хлореллы коротковолновым (650 нм) и длинноволновым (700 нм) красным светом эффект выше, чем суммарный квантовый выход при воздействии красным светом этих длин в отдельности. Это явление получило название эффекта усиления Эмерсона. Позже предположение Р. Эмерсона о наличии двух фотосистем получило экспериментальное подтверждение.
5.2.2. Нециклический и циклический транспорт электронов
В фотосистеме II реакционный центр, состоящий из димера хлорофилла а с максимумом поглощения при 680 нм (П680), последовательно поглотив энергию, равную 2 квантам коротковолнового красного света, и перейдя в синглетное возбужденное состояние, передает 2 электрона феофитину. От феофитина электроны последовательно передаются на пластохиноны QA и QB, расположенные на другой стороне мембраны тилакоида, затем на две липидорастворимые молекулы пластохинона PQ. Он является переносчиком протонов и электронов, выполняющего в мембране роль челнока. Принимая 2 электрона и захватывая из стромы 2 Н+, 2 молекулы PQH2 диффундируют через липидную фазу мембраны. Электроны от 2 PQH2 поступают в цепь:
железосерный белок FeSr® цитохром f ® Cu-содержащий белок пластоцианин ® П700,
а протоны попадают в полость тилакоида.
Вакантные места в П+680 заполняются 2 электронами из содержащего Mn переносчика электронов, который восстанавливается с участием белкового комплекса S. Окисленный комплекс S связывает воду и восстанавливается за счет электронов воды. При фотоокислении воды комплексом S вторая пара протонов освобождается в полость тилакоида, а атом кислорода диффундирует из хлоропласта.
После возбуждения реакционного центра фотосистемы I - молекулы хлорофилла а с максимумом поглощения при 700 нм (П700), 2 квантами длинноволного красного света 2 электрона передаются мономерной форме хлорофилла а – А1 и затем переносчикам электронoв железосерным белкам А2 и АВ, ферредоксину на наружной стороне мембраны тилакоида, НАДФ-редуктазе. Этот фермент восстанавливает НАДФ в НАДФН. На вакантные места в П+700 переходят электроны с пластоцианина и нециклическая цепь транспорта электронов замыкается.
В мембранах хлоропластов может функционировать циклический транспорт электронов, когда действует только фотосистема I. Возбужденные молекулы П700 передают электроны на А1, железосерные белки А2 и АВ, переносящие электроны на другую сторону мембраны, ферредоксин, пластохинон, цитохром b6, железосерный белок FeSr, цитохром f, пластоцианин и П700 (рис. 5.4). Энергия, освобождающаяся при транспорте электронов, используется для фосфорилирования АДФ.
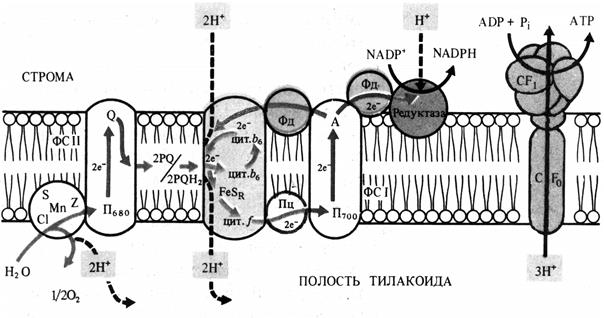
Рис. 5.4. Локализация электрон- и протонтранспортных реакций в тилакоидной мембране хлоропласта (по В. В. Полевому).
Механизм фотофосфорилирования АДФ объясняет теория П. Митчелла. Согласно этой теории, трансмембранный перенос пластохинонами электронов и протонов в одну сторону чередуется с переносом цитохромной системой в обратную сторону электронов. Поэтому по одну сторону мембраны накапливается избыток протонов и возникает электрохимический мембранный потенциал. Его энергия используется для синтеза АТФ при разрядке мембраны в результате транспорта протонов через мембрану посредством Н+-АТФазы, которая действует как АТФсинтетаза. Этот фермент выглядит как грибовидная частица на поверхности мембраны тилакоидов. Его молекула состоит из двух частей: головки, выступающей с наружной стороны мембраны и содержащей активный центр фермента, и ножки, погруженной в мембрану и представляющей канал, через который передвигаются протоны.
5.3. Темновая фаза фотосинтеза
5.3.1. С3-путь фотосинтеза или цикл Кальвина
Этот путь ассимиляции СО2 обнаружен у всех фотосинтезирующих растений. Он был назван циклом Кальвина в честь американского биохимика М. Кальвина, который с сотрудниками открыл и изучил его в 1946-1956 годах с помощью метода меченых атомов и хроматографии. Растения разное время подкармливали 14СО2 и хроматографировали экстракты. Радиоактивные изотопы по химическим свойствам не отличаются от стабильных. Принимая участие в реакциях, они помечают те соединения, в которые входят. Цикл состоит из трех этапов: карбоксилирования, восстановления, регенерации первичного акцептора СО2 и синтеза конечного продукта фотосинтеза (рис. 5.5).

Рис. 5.5. Цикл Кальвина (С3-путь фотосинтеза.
1 – фосфорибулокиназа, 2 – рибулозодифосфаткарбоксилаза, 3 - фофсфоглицераткиназа, 4 – триозофосфатдегидрогеназа, 5 – триозофосфатизомераза, 6 – альдолаза, 7 – фосфатаза, 8 – транскетолаза, 9 – альдолаза, 10 – фосфатаза, 11 – транскетолаза, 12 – рибозофосфатизомераза, 13 – фосфокетопентоэпимераза (по В. В. Полевому).
1. Карбоксилирование.Фосфорибулокиназа фосфорилирует при участии АТФ рибулозо-5-фосфат с образованием АДФ и рибулозо-1,5-дифосфата. Последний является акцептором СО2 и под действием рибулозодифосфаткарбоксилазы присоединяет СО2. В результате образуются 2 молекулы 3-фосфоглицериновой кислоты (3-ФГК).
2. Восстановление.Фосфоглицераткиназа при участии АТФ фосфорилирует 3-ФГК и образовавшаяся 1,3-дифосфоглицериновая кислота восстанавливается с помощью НАДФН и дегидрогеназы фосфоглицеринового альдегида до 3-фосфоглицеринового альдегида (3-ФГА).
3. Регенерация.После фиксации трех молекул СО2 и образования шести молекул 3-ФГА пять из них используются для синтеза рибулозо-5-фосфата, а одна молекула 3-ФГА – для образования глюкозы.
Триозофосфатизомераза превращает 3-ФГА в фосфодиоксиацетон. Затем альдолаза образует из 3-ФГА и фосфодиоксиацетона фруктозо-1,6-дифосфат. Он теряет один остаток фосфорной кислоты под влиянием фруктозо-1,6-дифосфатазы и превращается во фруктозо-6-фосфат. Транскетолаза переносит гликолевый альдегид от фруктозо-6-фосфата на 3-ФГА с образованием эритрозо-4-фосфата и ксилулозо-5-фосфата. Альдолаза присоединяет фосфодиоксиацетон к эритрозо-4-фосфату с образованием седогептулозо-1,7-дифосфата. Он дефосфорилируется фосфатазой и под влиянием транскетолазы соединяется с 3-ФГА. Продуктами этой реакции являются ксилулозо-5-фосфат и рибозо-5-фосфат. Две молекулы ксилулозо-5-фосфата при участии рибулозофосфатэпимеразы и одна молекула рибозо-5-фосфата под действием рибозофосфатизомеразы превращаются в три молекулы рибулозо-5-фосфата.
Шестая молекула 3-ФГА используется для синтеза фруктозо-1,6-дифосфата при повторении цикла. Из двух молекул фруктозо-1,6-дифосфата образуются фруктозо-6-фосфат и глюкозо-1-фосфат. Последний, взаимодействуя с уридинтрифосфатом, дает уридинфосфоглюкозу. Она и фруктозо-6-фосфат образуют сахарозофосфат, который после дефосфорилирования превращается в сахарозу. Следовательно, для образования одной молекулы сахарозы необходимо прохождение четырех циклов Кальвина. Крахмал синтезируется из уридинфосфоглюкозы под влиянием амилосинтетазы.
Среди продуктов фотосинтеза обнаружены аминокислоты. При недостатке НАДФН 3-ФГК превращается не в 3-ФГА, а в пировиноградную кислоту. Она, присоединяя аммиак, образует аланин. Из пировиноградной кислоты в цикле Кребса образуются органические кислоты, которые в ходе реакций аминирования и переаминирования дают аминокислоты.
5.3.2. С4-путь фотосинтеза или цикл Хетча-Слэка
Австралийскими учеными М. Хетчем и К. Слэком был описан С4-путь фотосинтеза, характерный для тропических и субтропических растений (сахарный тростник, кукуруза и др.). Листья этих растений содержат хлоропласты двух типов: обычные в клетках мезофилла и крупные хлоропласты, не имеющие гран и фотосистемы II, в клетках обкладки, окружающих проводящие пучки.
В цитоплазме клеток мезофилла фосфоэнолпируваткарбоксилаза присоединяет СО2 к фосфоэнолпировиноградной кислоте, образуя щавелевоуксусную кислоту. Она транспортируется в хлоропласты, где восстанавливается до яблочной кислоты при участии НАДФН. В присутствии ионов аммония щавелевоуксусная кислота превращается в аспарагиновую кислоту. Яблочная и (или) аспарагиновая кислоты переходят в хлоропласты клеток обкладки, декарбоксилируются до пировиноградной кислоты и СО2. СО2 включается в цикл Кальвина, а пировиноградная кислота переносится в клетки мезофилла, где превращается в фосфоэнолпировиноградную кислоту (рис. 5.6). Такой механизм позволяет растениям фотосинтезировать при закрытых из-за высокой температуры устьицах. Кроме того, продукты цикла Кальвина образуются в хлоропластах клеток обкладки, окружающих проводящие пучки. Это способствует быстрому оттоку фотоассимилятов и тем самым повышает интенсивность фотосинтеза.
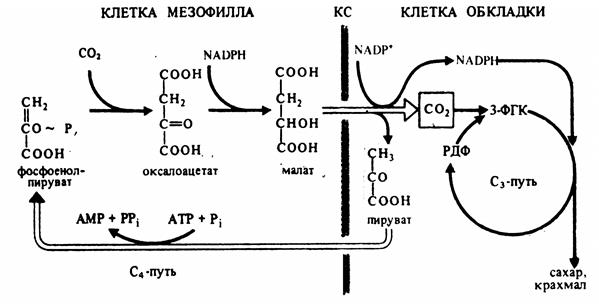
Рис. 5.6. Цикл Хэтча и Слэка (С4-путь фотосинтеза).
КС – клеточная стенка (по В. В. Полевому).
5.3.3. Фотосинтез по типу толстянковых (суккулентов)
У суккулентов (кактусов и растений сем. толстянковых (Crassulaceae) процессы фотосинтеза разделены не в пространстве, как у других С4-растений, а во времени. Этот тип фотосинтеза получил название CAM (crassulation acid metabolism)-путь. Устьица днем обычно закрыты, что предотвращает потерю воды в ходе транспирации, и открыты ночью. В темноте СО2 поступает в листья, где фосфоэнолпируваткарбоксилаза присоединяет его к фосфоэнолпировиноградной кислоте, образуя щавелевоуксусную кислоту. Она восстанавливается НАДФН-зависимой малатдегидрогеназой до яблочной кислоты, которая накапливается в вакуолях. Днем яблочная кислота переходит из вакуоли в цитоплазму, где декарбоксилируется с образованием СО2 и пировиноградной кислоты. СО2 диффундирует в хлоропласты и включается в цикл Кальвина (рис. 5.7).
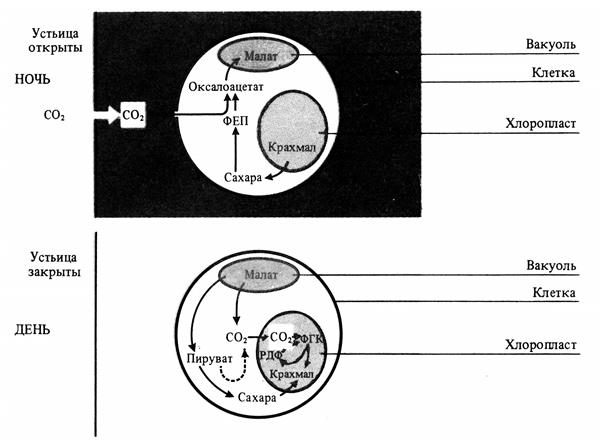
Рис. 5.7. Метаболизм органических кислот при фотосинтезе по типу толстянковых (САМ-метаболизм) (по В. В. Полевому).
5.3.4. Фотодыхание
Фотодыхание – это активируемый светом процесс выделения СО2 и поглощения О2. Так как первичным продуктом фотодыхания является гликолевая кислота, оно еще называется гликолатным путем. Фотодыхание усиливается при низком содержании СО2 и высокой концентрации О2 в воздухе. В этих условиях рибулозодисфаткарбоксилаза хлоропластов катализирует не карбоксилирование рибулозо-1,5-дифосфата, а его расщепление на 3-фосфоглицериновую и 2-фосфогликолевую кислоты. Последняя дефосфорилируется с образованием гликолевой кислоты.
Гликолевая кислота из хлоропласта переходит в пероксисому, где окисляется гликолатоксидазой до глиоксиловой кислоты. Образующаяся при этом перекись водорода разлагается каталазой, присутствующей в пероксисоме. Глиоксиловая кислота аминируется, превращаясь в глицин. Глицин транспортируется в митохондрию, где из двух молекул глицина синтезируется серин и освобождается СО2.
Серин может поступать в пероксисому и под действием аминотрансферазы передает аминогруппу на пировиноградную кислоту с образованием аланина, а сам превращается в гидроксипировиноградную кислоту. Последняя при участии НАДФН восстанавливается в глицериновую кислоту. Она переходит в хлоропласты, где включается в цикл Кальвина (рис. 5.8).
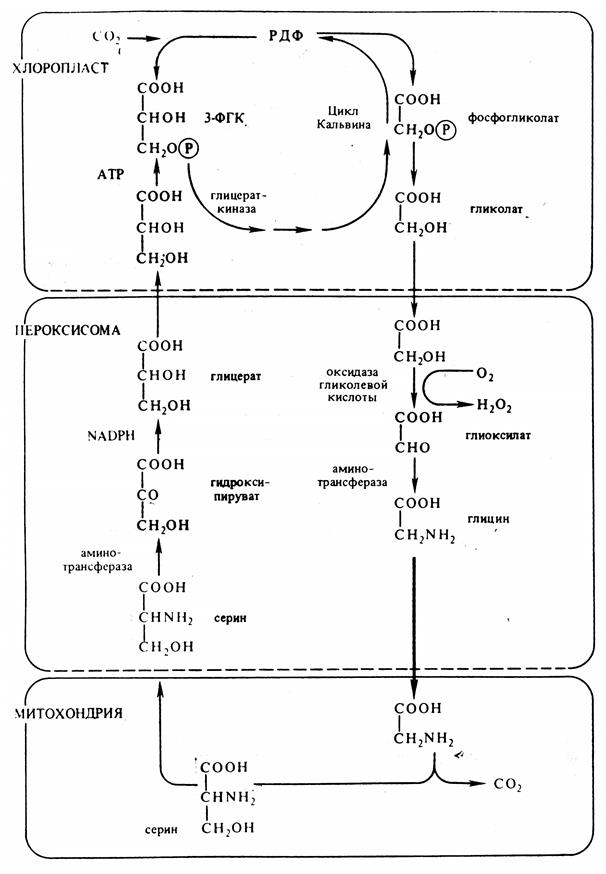
Рис. 5.8. Фотодыхание (по В. В. Полевому).
У растений С4-типа выделяющийся при фотодыхании углекислый газ реагирует в клетках мезофилла с фосфоэнолпировиноградной кислотой с образованием щавелевоуксусной и яблочной кислот. Яблочная кислота переходит в клетки обкладки, где служит донором СО2.
5.4. Влияние внутренних и внешних факторов на фотосинтез
Фотосинтез осуществляется в полуавтономных органеллах – хлоропластах. Однако он в значительной мере контролируется процессами, происходящими в растении, и факторами внешней среды.
Отток ассимилятов. Накопление фотоассимилятов в хлоропластах и в околопластидном пространстве приводит к ингибированию ферментов, участвующих в фотосинтезе.
Содержание хлорофилла.С увеличением содержания в клетке хлорофилла увеличивается интенсивность фотосинтеза.
Возраст листа и растения.В ходе роста листа интенсивность фотосинтеза увеличивается. После окончания роста листа она постепенно снижается. У многих однолетних растений интенсивность фотосинтеза достигает максимума в фазу бутонизации и цветения, а затем снижается.
Свет.Имеется нижний порог освещенности, при котором растения начинают фотосинтезировать. Затем зависимость интенсивности фотосинтеза от освещенности имеет логарифмический характер с последующим выходом на плато. Угол наклона кривой зависимости интенсивности фотосинтеза от освещенности зависит от влияния других факторов. Так, у светолюбивых растений она выходит на плато при значительно более высокой освещенности, чем у теневыносливых растений. Уровень освещения, при котором поглощение СО2 в ходе фотосинтеза равно выделению СО2 в процессе дыхания, называется компенсационным пунктом.
Важен и спектральный состав света. При освещении красным светом образуются преимущественно углеводы, синим - амино- и органические кислоты.
Температура.При низкой освещенности фотосинтез идет с одинаковой скоростью при 15 и 25оС. Это объясняется тем, что при низкой освещенности интенсивность фотосинтеза зависит от скорости световых реакций. При высокой освещенности интенсивность фотосинтеза лимитируется скоростью темновых реакций и Q10 примерно равен 2. Для большинства растения С3-типа оптимальная температура 20-25оС, для растений С4-типа она равна 25-40оС. При температуре выше оптимальной интенсивность фотосинтеза снижается из-за инактивации хлоропластов и закрытия устьиц.
Содержание СО2 в воздухе.Повышение содержания СО2 с 0,03 % до 0,3 % вызывает увеличение интенсивности фотосинтеза. Дальнейшее возрастание концентрации СО2 до 1 % не сказывается на фотосинтезе, но более высокий уровень СО2 в воздухе приводит к депрессии фотосинтеза. Высокие концентрации СО2 особенно неблагоприятны при высокой освещенности, так как происходит ингибирование темновых реакций. Влияние содержания углекислого газа на фотосинтез зависит от вида растения.
Снабжение водой.При большом водном дефиците интенсивность фотосинтеза снижается из-за закрытия устьиц, что уменьшает поступление СО2 в листья, снижает транспирацию и приводит к повышению температуры листа. Кроме того, обезвоживание изменяет конформацию и, следовательно, активность ферментов.
Содержание кислородав воздухе, в среднем, равно 21 %. Повышение концентрации или отсутствие кислорода для фотосинтеза неблагоприятны. Кислород снижает активность рибулозодифосфаткарбоксилазы.
Минеральное питание.Исключение любого элемента минерального питания отрицательно сказывается на фотосинтезе. Особенно важны такие элементы как фосфор, магний, железо, марганец, медь, калий и азот. На всех этапах фотосинтеза участвуют фосфорилированные соединения. Калий активирует процессы фосфорилирования и участвует в открывании устьиц. Магний входит в состав хлорофиллов, активирует реакции карбоксилирования и восстановления НАДФ. Железо необходимо для синтеза хлорофиллов. Марганец участвует в фоторазложении воды. Медь входит в состав пластоцианина. Азот необходим для формирования хлоропластов и образования пигментов.
5.5. Значение фотосинтезирующих организмов для биосферы
Выделяют пять основных аспектов планетарной роли фотосинтезирующих организмов.
Накопление органической массы. В процессе фотосинтеза наземные растения образуют до 170 млрд. тонн, а растения мирового океана – до 70 млрд. тонн биомассы в год в пересчете на сухое вещество, используемой гетеротрофными организмами.
Обеспечение постоянства содержания СО2 в воздухе. Связывание СО2 в ходе фотосинтеза в значительной мере компенсирует его выделение в результате других процессов (дыхание, брожение, деятельность вулканов, производственная деятельность человечества).
Препятствие развитию парникового эффекта. Часть солнечного света отражается от поверхности Земли в виде тепловых инфракрасных лучей. СО2 поглощает инфракрасное излучение и тем самым сохраняет тепло на Земле. Повышение содержания СО2 в атмосфере может способствовать увеличению температуры, то есть создавать парниковый эффект. Это приведет к затоплению прибрежных зон из-за поднятия уровня мирового океана в результате таяния ледников в горах и на полюсах. Однако высокое содержание СО2 в воздухе активирует фотосинтез и, следовательно, концентрация СО2 в воздухе опять уменьшится.
Накопление кислорода в атмосфере. Первоначально в атмосфере Земли кислорода было очень мало. Сейчас его содержание составляет 21 % по объему воздуха. В основном, этот кислород является продуктом фотосинтеза. Ежегодно растения и другие фотосинтезирующие организмы поставляют в атмосферу примерно 120 млрд. тонн кислорода.
Озоновый экран. Озон (О3) образуется в результате фотодиссоциации молекул кислорода под действием солнечной радиации на высоте около 25 км. Озон задерживает большую часть ультрафиолетовых лучей, губительных для всего живого.
Дата добавления: 2015-05-26; просмотров: 2512;
